Podmienky výskytu, metódy detekcie a metódy prevencie sklonu k medzikryštalickej korózii zvarových spojov vysokolegovaných ocelí
Strana 1
Medzikryštalická korózia nehrdzavejúce ocele najčastejšie sa prejavuje v prostrediach s oxidačnými vlastnosťami.
Medzikryštalickú koróziu nehrdzavejúcich ocelí je možné zistiť aj elektrochemicky - anodickým leptaním počas 5 minút pri prúdovej hustote 0 65 A / cm2 a 20 10 C v 60 % roztoku kyseliny sírovej s 0 5 % hexamínu alebo iného inhibítora korózie. Metóda anodického leptania, ktorá spočíva v anodickej polarizácii skúmanej oblasti povrchu ocele, má tú výhodu, že umožňuje rýchlo (1 5 - 5 minút) určiť náchylnosť ocele na medzikryštalickú koróziu priamo na pol. - hotové a hotové zvárané výrobky. Použitie tejto metódy umožňuje vykonávať medzioperačné testovanie náchylnosti kovu na medzikryštalickú koróziu a zodpovedajúcu tepelné spracovanie eliminovať túto tendenciu.
Najčastejšie je medzikryštalická korózia nehrdzavejúcich ocelí spojená s precipitáciou karbidov chrómu pri teplotách popúšťania pozdĺž hraníc zŕn, v dôsledku čoho koncentrácia chrómu v tuhom roztoku v blízkosti karbidov prudko klesá.
Najčastejšie je medzikryštalická korózia nehrdzavejúcich ocelí spojená s precipitáciou karbidov chrómu počas popúšťania pozdĺž hraníc zŕn, v dôsledku čoho koncentrácia chrómu v tuhom roztoku v blízkosti karbidov prudko klesá.
Za príčinu medzikryštalickej korózie nehrdzavejúcich ocelí sa považuje zrážanie karbidov chrómu Cr23C6 alebo (Cr, Fe)23Ce pozdĺž hranice zŕn pri zahrievaní v rozmedzí teplôt 450 - 850 C. Keďže pri týchto teplotách dochádza k rýchlej difúzii uhlíka. je vyšší ako u chrómu, tvorba karbidov pozdĺž hranice zŕn zaberá všetok uhlík zliatiny a chróm sa nachádza len na hranici zŕn. To vedie k ochudobneniu hranice zŕn o chróm a zníženiu schopnosti prejsť do pasívneho stavu. Preto sa v korozívnom prostredí hranica zŕn rozpúšťa.
Povaha medzikryštalickej korózie nehrdzavejúcich ocelí je v súčasnosti nedostatočne študovaná a existujúce teórie nie vo všetkých prípadoch vysvetľujú ich náchylnosť na medzikryštalickú koróziu.
Na elimináciu medzikryštalickej korózie nehrdzavejúcich ocelí je potrebné zabrániť zrážaniu karbidov chrómu pozdĺž hraníc zŕn. To sa dosiahne znížením obsahu uhlíka v oceli; legovaná oceľ s karbidotvornými prvkami (titán, tantal, niób), ktoré tvoria horšie rozpustné karbidy ako karbidy chrómu; vykonávanie tepelného spracovania za podmienok, ktoré zabraňujú tvorbe karbidov chrómu.
| Vplyv koncentrácie vanadičnanu na rýchlosť korózie ocele 1H18N9Т v roztokoch HN03 pri 100 C. | Vplyv teploty na rýchlosť korózie ocele 1H18Н9Т v roztokoch HN03 obsahujúcich 1% VOj. |
Medzikryštálová korózia (ICC) sa považuje za jeden z najnebezpečnejších typov deštrukcie kovov, pretože vo väčšine prípadov sa nedá určiť vizuálne.
1
Opísaný typ korózie sa týka deštrukcie kovov, ktorá sa spravidla pozoruje pozdĺž hraníc kryštálov (inak nazývaných zrná). To vedie k tomu, že materiál stráca svoju pevnosť a ťažnosť. MCC je typ lokálnej korózie. Zvyčajne má negatívny vplyv na zliatiny a kovy, ktoré sú náchylné na pasivitu. Patria sem nehrdzavejúce ocele (chróm a chróm-nikel), kompozície na báze niklu a hliníka.
Medzikryštalická korózia je spôsobená delamináciou pevného roztoku, čo vedie k vzniku špeciálnych fáz pozdĺž hraníc zŕn, v ktorých je nadmerné množstvo jedného alebo druhého prvku kovovej zliatiny. Navyše v zónach susediacich s hranicami kryštálov je objem takéhoto prvku minimálny. Pod vplyvom určitého prostredia s agresívnymi vlastnosťami sa na anódach pozoruje rozpúšťanie vyčerpaných alebo obohatených oblastí.
Medzikryštalická korózia
V podstate MCC, ako je zrejmé z popisu jeho mechanizmu, je elektrochemická reakcia vedúca k rýchlej deštrukcii kovových konštrukcií a výrobkov. Najčastejšie sa to pozoruje u zliatin s vysokým obsahom chrómu. V prostrediach s vysokým oxidačným indexom je korózia, ktorú popisujeme, spôsobená tým, že nasýtené fázy sa rozpúšťajú podľa selektívneho princípu. V situáciách, keď fázy obsahujú legujúce prísady (meď, vanád, molybdén, mangán, volfrám), sa proces rozpúšťania urýchľuje.
Hlavné faktory ICC sú tieto:
- vysoká teplota prostredia a doba vystavenia kovu v ňom;
- prítomnosť legujúcich prísad v zliatine, ktoré sú náchylné na nadmernú pasiváciu;
- agresivita operačného prostredia.
Interkryštalická deštrukcia môže mať rôznu rýchlosť. Záleží na tom, aký konkrétny potenciál daný kov má. Zrýchlenie toku MCC je zvyčajne pevne stanovené na nasledujúcich hodnotách: 0,35 V (potenciál tzv. aktívneho-pasívneho pohybu); 1,15 až 1,25 V (transpasívna zóna).
2
Zliatiny duralu sú vysoko citlivé na MCC. Mechanizmus ich zničenia je nasledujúci. CuAl2, intermetalická zlúčenina, sa vyzráža na hraniciach kryštálov. Zničí sa a uvoľní sa vodík. Na tejto intermetalickej zlúčenine nie je žiadny ochranný film (kvôli neprítomnosti oxidačnej látky v roztoku), takže sa celkom rýchlo rozpúšťa.
Vo väčšine prípadov sa medzikryštalická korózia duralových výrobkov pozoruje v oblastiach, kde sú mikroskopické póry a malé trhliny. Menej často sa ničenie začína v jamkách. Tvoria sa medzi kryštálovými hranicami. V tomto prípade je vývoj korózie uľahčený skutočnosťou, že vo vnútri jamiek je zaznamenané určité okyslenie elektrolytu. Z týchto dôvodov je žiaduce chrániť duralové výrobky (ako mnohé iné zliatiny na báze hliníka) pred zničením zhutnením ich štruktúry.

MK duralových výrobkov
Bežným typom MCC je korózia nožov. Označuje sa na zvarových spojoch. Zlomenina noža sa považuje za lokálnu, vyskytuje sa medzi švom a základným kovom. Vo väčšine prípadov sú zvárané spoje vystavené takémuto zničeniu: zliatiny s vysokým obsahom molybdénu; kovové kompozície, ku ktorým sa pridáva titán; chrómniklové vysoko uhlíkové ocele.
Pri zváraní takýchto zliatin dochádza k interakcii medzi studeným a zahriatym kovom na 1300°. V tavenine sa rozpúšťajú karbidy titánu alebo chrómu. Keď sa ochladí, nevytvárajú sa žiadne nové karbidy, uhlík zostáva v pevnej fáze a karbidy chrómu sa vyzrážajú (vo veľmi veľkých množstvách). Ak je atmosféra, v ktorej sa takéto procesy vyskytujú, agresívna, pozoruje sa (postupné) rozpúšťanie prvkov obsiahnutých v zliatine v úzkom úseku zvarového spoja na medzikryštalickej úrovni.
Zraneniu nožom možno predchádzať nasledujúcimi spôsobmi:
- vyhnúť sa nadmernému zahrievaniu v tepelne ovplyvnenej oblasti počas zvárania;
- používajte výlučne chrómniklové kompozície s nízkym obsahom uhlíka;
- použiť špeciálne žíhanie (hovorí sa mu stabilizácia), pri ktorom prechádzajú karbidy chrómu do tuhého roztoku.
3
Odolnosť austeniticko-feritických, austenitických, austeniticko-martenzitických, feritických a iných ocelí odolných voči korózii voči MCC, ako aj nanesený kov a zvárané spoje týchto zliatin sa určuje podľa GOST 6032. V krajinách SNŠ platí od roku 2005.
V súlade s touto normou sú k dispozícii nasledujúce skúšobné metódy pre medzikryštalickú koróziu:
- AMU. Analýzy sa vykonávajú v prítomnosti medi (kovovej) v roztoku síranu meďnatého a kyseliny sírovej.
- AMUF. Technika je podobná prvej, ale predpokladá prítomnosť nielen medi (kovu), ale aj fluoridu draselného alebo sodíka.
- VU. Testy v kyseline sírovej v prítomnosti oxidu železitého.
- DU. Vzorky sa analyzujú na odolnosť proti korózii v kyseline dusičnej (65 %).

Analýza vzorky na odolnosť proti korózii v kyseline dusičnej
Okrem toho sa v niektorých prípadoch testy vykonávajú v kompozícii pozostávajúcej zo zinkového prášku a kyseliny sírovej. Využíva sa aj technika leptania (anodických) kovov v inhibovanej kyseline sírovej. Ďalej sa na všetky tieto techniky pozrieme podrobnejšie. Najprv si však povedzme, ako by sa mali pripraviť vzorky na testovanie odolnosti voči MCC. Prírezy pre nich sú vyrezané z:
- axiálna oblasť dlhých výrobkov;
- povrchy z oceľového plechu;
- axiálna oblasť potrubných polotovarov a;
- telesá alebo presahy výkovkov;
- axiálna zóna zvarového kovu;
- povrchové plochy naneseného kovu.
Obrobky musia mať také geometrické parametre, aby bolo možné pripraviť taký počet vzoriek, aký si vyžadujú skúšobné podmienky. Ten môže byť plochý, prstencový, segmentovaný, vo forme rúrok alebo valcový. Vzorky podľa GOST sa vyrábajú z obkladovej vrstvy, ale až po úplnom odstránení prechodových a hlavných vrstiev z výrobku.
Nestabilizované zliatiny obsahujúce maximálne 0,03 % uhlíka, kompozície s nióbom a titánom ako aditívami, ako aj stabilizované ocele by sa mali testovať na obrobkoch, ktoré prešli procedúrou predhrievania (odborníci to nazývajú provokovanie). Špecifická testovacia metóda sa vyberá na základe rôznych ukazovateľov. Zvyčajne sa berie do úvahy prevádzkový účel zliatiny a jej chemické zloženie.
4
Medzikryštalická korózia najčastejšie postihuje tieto zliatiny: 03Х17Н14М3, 03Х18Н12, 08Х21Н6М2Т, 08Х17Т, 06Х18Н11, 01Х25ТБУ-VI, 08,101Н 5Х25Т, 12Х18Н12Т, 12Х18Н9, 10Х17Н13М3Т, 01-015Х18Т-VI, 03Х18Н11, 12Х18Н9Т, 03Х16Н1М5М a 426Н1Х5М. iní .
Výrobky a štruktúry z nich vyrobené sa analyzujú na odolnosť voči medzikryštalickému lomu pomocou metód AMU a AMUF. Tieto techniky sú v podstate rovnaké. Druhá je zrýchlená verzia testovania AMU. Analýza vzoriek pomocou takýchto technológií zahŕňa ponorenie obrobkov do pripravených roztokov (ich zloženie sme uviedli vyššie) a ich uchovávanie po určitú dobu.

Ponorenie kovu do roztoku kyseliny
Potom sa vzorky vyberú a ohnú pod uhlom 85–95° alebo do tvaru písmena Z. Potom sa pomocou lupy alebo špeciálnej metalografickej technológie zisťuje prítomnosť korózie. Ak pri skúmaní vzoriek pod lupou (7-12x zväčšenie) nie sú na obrobkoch viditeľné žiadne praskliny, znamená to, že výrobky majú požadovanú odolnosť proti medzikryštalickému lomu. Upozorňujeme, že na okrajoch obrobkov sú povolené mikrotrhliny.
Metalografická technika sa používa v situáciách, keď vzorky nemožno ohnúť v požadovanom uhle z dôvodu ich malých geometrických parametrov. Pri tejto kontrole sa z obrobku vyreže asi 2 cm dlhá časť. Poznámka! Rovina rezu musí byť kolmá na povrch obrobku. Tenký rez sa potom leptá a analyzuje pri 200-násobnom zväčšení (použije sa mikroskop).
Ak sa počas takejto skúšky na vzorke zaznamená deštrukcia hraníc kovových kryštálov s hĺbkou nie väčšou ako 30 mikrónov, obrobok sa považuje za odolný voči korózii. V opačnom prípade (hĺbka deštrukcie je väčšia), zliatina je údajne náchylná na MCC.
5
Na testovanie odolnosti voči MCC ocelí 02Kh25N22AM2, 03Kh17N14M3, 03Kh18N1102Kh18N11, 03Kh24N6AM3 a 03Kh18N12 sa používa metóda DU. Analýza sa vykonáva takto:
- vzorky odmastite (používa sa organické rozpúšťadlo), ponorte ich do destilovanej vody, vysušte a odvážte;
- spracované obrobky vložte do sklenenej banky so spätným chladičom (porcelánové lode alebo sklenené guľôčky sú predbežne umiestnené na dne nádoby);
- naplňte vzorky kyselinou dusičnou (65%), ktorá by mala pokrývať produkty o 1,5 cm;
- priveďte roztok do varu.
Celkové trvanie takéhoto testu je 5 cyklov po 48 hodinách. Celú tú dobu sú obrobky v kyseline, ktorá vrie rovnomerne (bez uvoľňovania oxidov a vyparovania). Vzorky sa potom odoberú a vyhodnotí sa náchylnosť na koróziu použitím skôr opísanej metalografickej techniky.
Kovový polotovar v kyseline
Technológia VU sa používa na analýzu produktov vyrobených zo zliatin KhN30MDB, 06KhN28MDT, 03Kh21N21M4GB a 03KhN28MDT. Pri tomto teste sa vzorky varia 48 hodín v kyseline sírovej a potom sa výsledky vyhodnotia pomocou metódy AMU. Testy s použitím zinkového prášku a kyseliny sírovej (metóda B) sa považujú za menej spoľahlivý analóg technológie VU. Vzorky v tejto analýze sa uchovávajú vo vriacom roztoku počas 144 hodín.
Kovové výrobky, ktoré sa testujú na odolnosť voči MCC pomocou technológií AMU a AMUF, sa často predbežne analyzujú pomocou metódy B. Zvyčajne sa používa na analýzu dielov vyrobených flexibilným lisovaním za tepla alebo zváraním zo zliatin 12H18H12Т, 03H18H11, 08H18H10, 12H,18Н19Т , 06H18H11, 12H18H10Т a 04H18H10.
Testovanie metódou B sa vykonáva na špeciálnej inštalácii pozostávajúcej z katódy (jej funkciu vykonáva olovená nádoba), zdroja prúdu (konštanta), reostatu a ampérmetra. Dodávame, že takáto analýza sa nevykonáva pre kov zvarového spoja.
Význam výskumu odolnosti voči MCC nespočíva len v stanovení životnosti výrobkov vyrobených z konkrétnej triedy ocele, ale aj v presnom určení mechanizmu medzikryštalického lomu. Preto sa takýmto testom vždy venuje zvýšená pozornosť. Koniec koncov, umožňujú nám vyvíjať nové metódy.
Proces medzikryštalickej korózie pevných kovov v kvapalnom kovovom médiu nebol špecificky študovaný. Niektoré pravdepodobné mechanizmy tohto procesu, ktorých existencia je potvrdená nepriamymi experimentálnymi pozorovaniami, sú uvedené nižšie.
1. Jedným z dôvodov medzikryštalickej korózie je vyššia úroveň potenciálnej energie atómov nachádzajúcich sa v medzikryštalických zónach v porovnaní s atómami vo vnútri kryštalitov. V dôsledku toho je rozpúšťacia aktivačná energia pre tieto atómy menšia ako pre zvyšok. V súlade s tým sa zvyšuje pravdepodobnosť ich uvoľnenia do roztoku ωt. Už skôr sa ukázalo, že konštanta rýchlosti rozpúšťania pre proces riadený prvým stupňom sa rovná α = ωтρ "/n∞. Zvýšenie pravdepodobnosti vstupu atómov medzikryštalických zón do roztoku tekutého kovu teda znamená, že rýchlosť rozpúšťania týchto úsekov kovovej štruktúry je vyššia ako rýchlosť rozpúšťania susedných V dôsledku toho sa čelo korózie v podmienkach izotermického a neizotermického rozpúšťania pozdĺž hraníc kovových zŕn prehĺbi, t.j. dôjde k medzikryštalickej korózii. V niektorých prípadoch je postup rozpúšťania pozdĺž hraníc zŕn taký veľký, že spôsobuje oddelenie celých zŕn od matrice, čo je charakteristická korózia niklu v tekutom lítiu pri 1000 °C prípad, je znázornený na obr.
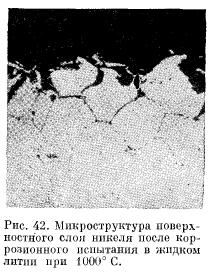
Odhadnime hĺbku medzikryštalickej korózie kovu spôsobenej rozdielom v rýchlosti rozpúšťania atómov z tela zrna a medzikryštalických zón. Pre izotermické rozpúšťanie je v tomto prípade počet atómov prechádzajúcich do roztoku tekutého kovu za jednotku času určený závislosťou podobnou rovnici (1):
kde index „z“ znamená, že zodpovedajúca charakteristika sa týka rozpúšťania z povrchu zrna a index „g“ – rozpúšťania z medzikryštalickej zóny. Ak vezmeme do úvahy, ako predtým, že N-nVl, získame diferenciálnu rovnicu
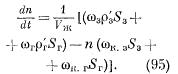
Riešením rovnice (95) a použitím počiatočnej podmienky: t=0, n=0 a pomeru pri nasýtení dn/dt = 0 nájdeme kinetickú rovnicu pre izotermické rozpúšťanie s prihliadnutím na vplyv medzikryštalických zón v nasledujúcom tvare:
Na určenie hĺbky všeobecnej (lз) a medzikryštalickej (lg) korózie napíšeme diferenciálnu rovnicu
kde ρз a ρг sú objemová hustota kryštalitov a interkryštalických zón. Riešenie tejto rovnice sa získa pomocou rovnosti (96) a počiatočnej podmienky t=0, lз=0, lг=0:
Aby sme získali pomer hĺbky medzikryštálovej a všeobecnej korózie, napíšeme pre ňu nasledujúci približný výraz:
kde symbol a označuje, ako predtým, konštantu rýchlosti rozpúšťania rovnajúcu sa ωт*ρ"/n∞ a nг∞ je tá časť koncentrácie roztoku, ktorá sa dosiahne v dôsledku rozpustenia kovu medzikryštalických zón. Odčítanie ( 99) z (98) nájdeme:
Rozdeľme rovnicu (100) číslom (99), pričom zanedbáme druhý člen na pravej strane rovnice (99), ktorý je zjavne podstatne menší ako prvý. Potom získame požadovaný vzťah vo formulári
Z rovnice (101) vyplýva, že medzikryštalická korózia s časom narastá.
Najzaujímavejšia je maximálna hodnota pomeru lg/lz, ktorá sa dosiahne na konci procesu rozpúšťania. Z (101) zistíme, že keď je roztok nasýtený, t.j. pri t→∞, tento pomer sa rovná
Hodnotu (lg/lz)max možno odhadnúť nasledujúcim spôsobom. Ako prvú aproximáciu môžeme zvážiť ng∞/n∞≈αгSг/αзSз; ďalej, ak vezmeme do úvahy, že α=ω*ρ"/n∞ a ρ"=α*ρ, kde α je medziatómová vzdialenosť, dostaneme (lг/lз)max≈ωг/ωз. Pravdepodobnosť prechodu atómov z povrchu zrna do roztoku je vyjadrená závislosťou ωз = v exp (-Qр/RT). Vzhľadom na to, že aktivačná energia rozpúšťania z medzikryštalitových zón je menšia ako z tela kryštalitov o množstvo ich prebytočnej energie ΔQg, pravdepodobnosť, že atómy z týchto oblastí prejdú do roztoku, bude ωg=v*exp [-( Qр-ΔQg)/RT] , Pomocou týchto výrazov získame (lg/lз)max≈exp (ΔQg/RT).
Vykonávame numerický odhad pomeru hĺbky medzikryštalickej korózie k celkovej pre γ-železo. Priemerná voľná energia jeho hraníc zŕn je podľa práce 8040 cal/g*atóm. Ak to vezmeme do úvahy, zistíme, že pri teplote 800 °C je pomer (lg/lz)max približne rovný 40. V dôsledku toho môže byť hĺbka medzikryštalickej korózie v železe takmer 40-krát väčšia ako hĺbka všeobecnej korózie. . Treba však poznamenať, že pri výraznom prehĺbení čela korózie pozdĺž hraníc zŕn bude proces rozpúšťania brzdený difúziou rozpustených atómov cez tekutý kov vo výslednom úzkom a dlhom kanáli, ktorý možno považovať za zvýšenie hrúbky hraničného filmu v tejto oblasti. Takýto proces prirodzene obmedzí hĺbku medzikryštalickej korózie.
Pomer hĺbky medzikryštalickej korózie k hĺbke všeobecnej korózie za podmienok tepelného prenosu hmoty možno získať pomocou rovnice prenosu hmoty vo forme
kde Δt je čas potrebný na to, aby prúd tekutého kovu prešiel horúcou zónou. Keďže hmotnosť kovu preneseného do studenej zóny počas času t sa rovná ΔP=S*Rpm*t, kde S je povrch, z ktorého sa rozpúšťanie v horúcej zóne vyskytuje, potom na základe rovnosti (103) dostaneme
Prejdime teraz k obr. 43, ktorý ukazuje kinetické krivky rozpúšťania kovov kryštalitov a interkryštalických zón. Z diagramov je zrejmé, že počiatočné (ϗ*nн∞+nк) a konečné (nв) koncentrácie roztoku v horúcej zóne sú rovnaké pre kryštality aj interkryštalické zóny, ale hodnota Δt je pre ne rozdielna, ktorý je spojený s rôznymi hodnotami αg a αz . Berúc do úvahy, že plocha týchto úsekov štruktúry sa tiež líši, že ΔP=ρSl, a pomocou pomeru beca kovu rozpusteného z intergranulárnych zón a z kryštalitov zistíme
Keďže ρз≥ρг a Δtз≥Δtг, potom lг/lз≥1, t. j. k medzikryštalickej korózii dochádza aj v podmienkach tepelného prenosu hmoty. Ak je nв výrazne menšie ako nв∞, potom môžete použiť približnú rovnosť Δtг/Δtз=αз/αг (pozri obr. 43). Na základe posledného vzťahu má rovnica (105) tvar lg/lз≈ρз/ρг*αг/αз. V dôsledku toho je intenzita medzikryštalickej korózie v tomto prípade určená pomerom rýchlostných konštánt rozpúšťania kovu medzikryštalických zón a kryštalitov. Je zaujímavé poznamenať, že intenzita deštrukcie kovu pozdĺž hraníc kryštalitov počas tepelného prenosu hmoty sa rovná maximálnej hodnote pomeru lg/lz počas izotermického rozpúšťania. To znamená, že môžeme použiť skôr urobený odhad tohto pomeru, z ktorého vyplýva, že hĺbka medzikryštalickej korózie, napríklad železa pri 800 °C, môže byť približne 40-krát väčšia ako hĺbka všeobecnej korózie. Zároveň je potrebné zdôrazniť, že ak sa intenzita (lg/lz) medzikryštalickej korózie v čase mení len málo, potom sa rozdiel medzi hĺbkou medzikryštalickej a všeobecnej korózie neustále zvyšuje. Hĺbka všeobecnej korózie za podmienok prenosu hmoty je teda určená rovnicou
a hĺbka medzikryštalickej korózie pre prípad uvažovaný vyššie je rovná
odkiaľ nasleduje
V tomto prípade sa teda rozdiel medzi hĺbkou medzikryštalickej a všeobecnej korózie s časom zvyšuje podľa lineárneho zákona. Takýto vývoj medzikryštalickej korózie však nemôže byť neobmedzený. Ako už bolo uvedené, maximálna hĺbka medzikryštalickej korózie je určená momentom prechodu na riadenie procesu rozpúšťania v kanáloch tvorených susednými kryštálmi mechanizmom difúzie.
K deštrukcii hraníc zŕn v dôsledku zvýšenej energie tu nachádzajúcich sa atómov môže dôjsť počas procesu rozpúšťania, ako aj za izotermických podmienok po dosiahnutí nasýtenia roztoku. V druhom prípade dôjde ku korózii prostredníctvom energetického prenosu hmoty. To niekedy vysvetľuje vplyv tekutých kovov na pevné kovy počas dlhodobých izotermických testov, hoci roztok už dávno dosiahol rovnovážnu koncentráciu.
Je potrebné poznamenať, že prenos energie hmoty má lokálny charakter a pokrýva len malé plochy povrchu. Táto vlastnosť sa vysvetľuje skutočnosťou, že hnacou silou prenosu je energetický gradient dU/dx, kde x je vzdialenosť pozdĺž povrchu. kov Proces energetického prenosu hmoty je kombináciou procesov rozpúšťania, difúzie v povrchovom filme tekutého kovu a kryštalizácie. Rýchlosť difúzie je v tomto prípade určená rovnicou podobnou (78):
kde D je koeficient difúzie v tekutom kove; S je plocha povrchu, cez ktorú dochádza k difúzii; f - koeficient proporcionality. Je zrejmé, že ak je vzdialenosť medzi oblasťami s rôznymi atómovými energiami dostatočne veľká, energetický gradient bude malý a rýchlosť difúzie bude zanedbateľne nízka. Výsledkom je, že proces presunu medzi týmito oblasťami prakticky nenastane.
2. Medzikryštalická korózia zliatin môže byť spojená so selektívnou koróziou. Tento účinok by sa mal pozorovať v dvoch prípadoch. Ak je ľahko rozpustný prvok horofilný, potom prirodzene jeho preferenčné rozpúšťanie spôsobí deštrukciu medzikryštalitových zón vo väčšej miere ako samotné kryštality, kde je počiatočná koncentrácia tohto prvku oveľa nižšia. Príkladom takéhoto efektu sa zdá byť selektívne rozpúšťanie niklu z austenitických ocelí. Je známe, že ocele tejto triedy zvyčajne podliehajú medzikryštalickej korózii v tekutých kovoch a tento efekt je obzvlášť výrazný pri skúšaní ocelí s obsahom olova a bizmutu. Ak vezmeme do úvahy, že nikel je horofilný prvok v zliatinách železa, potom možno tento efekt vysvetliť.
Druhý prípad medzikryštalickej korózie selektívne sa rozpúšťajúcich zliatin je možný, keď je ľahko rozpustný prvok rovnomerne rozložený v matrici. Podmienkou, ktorá zabezpečuje lokálnu deštrukciu zliatiny pozdĺž hraníc zŕn, je v tomto prípade vyššia rýchlosť difúzie ľahko rozpustného prvku pozdĺž hraníc zŕn ako v celom ich objeme. Medzikryštalická korózia chrómových ocelí pozorovaná v tekutom bizmute je zjavne spojená s prevládajúcou hraničnou difúziou chrómu, keďže podľa práce nie je v zliatinách na báze železa horofilný. V niektorých zliatinách môže byť ľahko rozpustný prvok horofilný a môže mať vyšší koeficient hraničnej difúzie, čo by malo viesť k výraznému zvýšeniu medzikryštalickej korózie zliatiny v tekutom kove.
V prípade chemickej interakcie tekutého kovu so zložkou alebo zložkami zliatiny možno tiež pozorovať intenzívnu medzikryštalickú deštrukciu spôsobenú vyššie uvedenými dôvodmi.
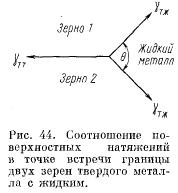
3. K deštrukcii pevných kovov pozdĺž hraníc zŕn v tekutom kovovom prostredí môže dôjsť pri určitom pomere voľnej povrchovej energie hranice dvoch zŕn a voľnej energie rozhrania tuhá látka-kvapalný kov.
Uvažujme podmienku rovnováhy povrchových napätí v mieste, kde sa stretáva hranica dvoch zŕn s tekutým kovom (obr. 44). Označme γtt povrchové napätie hranice dvoch zŕn a γtj povrchové napätie hranice každého zrna s tekutým kovom (budeme predpokladať, že γtj nezávisí od orientácie zrna). Nech ďalej θ je dihedrálny uhol medzi kontaktnými povrchmi dvoch susedných zŕn s tekutým kovovým médiom. Potom rovnovážny stav v súlade s diagramom na obr. 44, bude
V závislosti od pomeru hodnôt povrchového napätia bude teda povrchový reliéf pevného kovu v mieste, kde vystupuje hranica zŕn, odlišný. Ak podmienku rovnováhy spĺňa malá ostrý roh, potom by sa v tomto prípade mala pozorovať medzikryštalická korózia. A s poklesom dihedrálny uhol medzikryštalická korózia sa zvýši. Pri θ=0 médium prenikne hlboko do pevného kovu pozdĺž hraníc zŕn a rozdelí ho na jednotlivé zrná. V druhom extrémnom prípade pri θ = 180° nedôjde k medzikryštalickej korózii. Uhlový interval 90°≤θ≤180° možno považovať za prípad tvorby malých rýh pozdĺž hraníc zŕn, ktoré sa nachádzajú na leštenom povrchu pevného kovu po krátkom rozpustení v tekutom kove. Je zrejmé, že spodná hranica (90°) je ľubovoľná, pretože aj pri nižších hodnotách dihedrálneho uhla je medzikryštalická korózia malá. Zdá sa, že obzvlášť nebezpečný rozsah hodnôt 0 by sa mal považovať za 0. Vzhľadom na extrémnu zložitosť experimentálneho stanovenia voľnej povrchovej energie pevných látok a energie rozhrania pevná látka-kvapalina sú tieto hodnoty známe len pre veľmi málo materiálov. Neexistujú ani dostatočne spoľahlivé metódy na ich teoretický výpočet. Preto vyššie uvedené úvahy nemožno aplikovať na kombinácie kovov, ktoré sú predmetom záujmu v našom prípade. Pre ilustráciu opísaného efektu poukazujeme na interkryštalický prienik bizmutu do medi a absenciu poškodenia hraníc zŕn pri ponorení medi do olova. Vzhľadom na takmer úplné zmáčanie medi bizmutom (kontaktný uhol je blízky nule) a slabé zmáčanie olovom je rozdiel v pôsobení týchto tekutých kovov zrejmý. Pridaním zinku a cínu do bizmutu, ktoré zvyšujú energiu rozhrania meď-bizmut, bola eliminovaná medzikryštalická korózia medi pri 600°C.
Je potrebné poznamenať, že v prípade súčasného výskytu rôznych druhov korózie sa hodnoty povrchových energií hranice dvoch zŕn a medzifázovej hranice môžu v priebehu času výrazne meniť, čo spôsobí zodpovedajúcu zmenu v dihedrálnej oblasti. uhol. Energia hranice medzi dvoma zrnami sa môže meniť v dôsledku selektívnej korózie alebo hraničnej difúzie tekutého kovu. Medzifázová energia môže meniť svoju hodnotu v dôsledku tvorby tuhého roztoku alebo intermetalickej zlúčeniny na povrchu kovu, ako aj v dôsledku zmien v zložení tekutého kovového média.
Medzikryštalická korózia, spôsobená určitým pomerom povrchových energií, môže nastať tak počas procesu rozpúšťania, ako aj po nasýtení roztoku prostredníctvom energetického prenosu hmoty.
4. V prítomnosti nečistôt v tekutom kove sa pozoruje intenzívna deštrukcia pevných kovov pozdĺž hraníc zŕn. Najtypickejším príkladom je medzikryštalická korózia materiálov v tekutom sodíku obsahujúcom výraznú prímes kyslíka. Nehrdzavejúce chrómové a chrómniklové ocele a zliatiny na báze niklu teda podliehajú medzikryštalickej korózii v sodíku s prímesou 0,5 % hmotn. kyslíka pri 700 °C.
Príčina tohto vplyvu kyslíka spočíva v chemickej interakcii iónov kyslíka alebo oxidu sodného so zložkami zliatiny umiestnenými v interkryštalických zónach. Kvôli malým objemom, v ktorých k tejto interakcii dochádza, a malému množstvu reakčných produktov neboli procesy medzikryštalickej korózie v tekutých kovoch s prímesami doteraz skúmané.
5. Medzikryštálovú koróziu možno pozorovať aj pri interakcii alkalických kovov s oxidmi, sulfidmi, fosfidmi a karbidy, ktoré sa v pevných kovoch nachádzajú hlavne pozdĺž hraníc zŕn. Takéto procesy budú diskutované v nasledujúcej kapitole. Jednou z chýb austeniticko-martenzitických a austeniticko-feritických ocelí je ich sklon k prehrievaniu pri zváraní a krehnutiu postihnutej zóny. Je to spôsobené rastom zŕn v dôsledku prehriatia feritovej fázy vytvorenej v blízkosti zóny fúzie. Krehkosť podporuje aj premena uhlíkom obohateného austenitu (pri vysokých teplotách je austenit znovu obohatený uhlíkom) na martenzit, keď sa zvar ochladzuje. Treba mať na pamäti, že vo zvarových spojoch austeniticko-feritických a austeniticko-martenzitických ocelí je možný vývoj vodíka pozdĺž hraníc zŕn. Aby sa tomu zabránilo, zvarový spoj sa temperuje 1-2 hodiny pri teplote 150 °C.
Vysokolegované ocele a zliatiny majú spravidla koeficient lineárnej rozťažnosti zvýšený až 1,5-krát pri zahrievaní a koeficient tepelnej vodivosti znížený 1,5-2-krát v porovnaní s nízkouhlíkovými oceľami. Väčšina týchto ocelí je náchylná na horúce alebo studené praskanie počas zvárania, čo sťažuje zabezpečenie požadovaných vlastností zvarových spojov. Pri oblúkovom zváraní vysokolegovaných ocelí by mali byť kovové povrchy chránené pred postriekaním kovom a troskou, pretože poškodzovaním povrchu môžu spôsobiť koróziu alebo koncentrácie napätia, ktoré oslabujú štruktúru. Na ochranu pred postriekaním pri zváraní sa na kovový povrch susediaci so švom nanáša ochranný povlak (organokremičitý lak, základný náter VL-02, VL-023 atď.).
Martenzitické ocele s vysokým obsahom chrómu (20X13, 14H17Н2 atď.), Martenziticko-feritické ocele (12X13, 14H12Н2МФ atď.) sú kaliteľné ocele, ktoré sú náchylné na tvorbu studených trhlín. V menšej miere sem patria feritické ocele (12X17, 08X17T, 08X18T1 atď.). Aby sa zabránilo praskaniu, používa sa predbežné alebo súčasné zahrievanie, ktoré je potrebné najmä pri zvýšení obsahu uhlíka v oceli a jej hrúbke. Po zváraní sa martenzitické, martenziticko-feritické a niekedy feritické ocele podrobia vysokému popúšťaniu pri teplote 680-720 °C a žiaruvzdorné (20X13, 12X13 atď.) - pri teplote 730-750 °C . Temperovanie zlepšuje štruktúru, mechanické vlastnosti a odolnosť proti korózii.
Je potrebné vziať do úvahy, že korózna odolnosť ocelí, ktoré neobsahujú titán alebo niób, sa pri zahrievaní nad 500 ° C postupne znižuje, preto sa tieto prvky zavádzajú do ocele a dodatočne sa legujú molybdénom, vanádom a inými prísadami, napr. martenzitická oceľ 18X1SHNFB; martenziticko-feritický 18Х12ВМБФР; feritické 15X25T atď. Na zváranie martenzitických, martenziticko-feritických a feritických ocelí sa používajú elektródy, ktorých tyče a povlaky poskytujú nanesený kov, ktorý je chemickým zložením blízky základnému kovu, napríklad martenzitická oceľ triedy 15X11 VMF je zvárané elektródami E12X11NVMF triedy KTI-10; martenziticko-feritická oceľ triedy 12X13 - elektródy E12X13 triedy UONII-13/ShZ atď. Ak sú konštrukcie vyrobené z ocele tejto triedy vystavené statickému zaťaženiu a švy nepodliehajú vysokým požiadavkám na pevnosť, možno zváranie vykonať austenitickými alebo austeniticko-feritickými elektródami, napríklad feritická oceľ 15H25Т je zváraná elektródami E02H20H14Г2M2 OZL. -20 a temperovanie po zváraní sa nesmie vykonávať.
Pri zváraní sa používa režim nízkeho tepelného príkonu, aby sa zabránilo rastu zŕn a krehnutiu tepelne ovplyvnenej zóny. Povlak elektród používaných na zváranie ocelí s vysokým obsahom chrómu by nemal obsahovať plynotvorné látky. Organické zlúčeniny a ochrana plynu by sa mala vykonávať v dôsledku disociácie uhličitanov a uvoľneného CO (oxidu uhoľnatého). Rovnako ako pri zváraní stredne legovaných ocelí, požiadavky na kvalitu montáže a čistenie kovu pred zváraním zostávajú rovnaké a ešte sa sprísňujú. Vysokochrómové ocele uvažovaných tried sa zvárajú aj v argónovom prostredí s volfrámovou elektródou. Táto metóda sa odporúča spojiť diely do hrúbky 5-6 mm s následným tepelným spracovaním; Koreňové švy z hrubšej ocele je vhodné zvárať volfrámovou elektródou, ktorá zaisťuje dobré vytvorenie zadnej guľôčky, zostávajúce vrstvy švu sa vykonávajú pomocou ručného zvárania elektrickým oblúkom alebo iným spôsobom.
Austenitické chrómniklové ocele sú obzvlášť citlivé na zvýšenie obsahu uhlíka a síry, ako aj iných prvkov, ktoré tvoria eutektiká s nízkou teplotou topenia.
MEDZIKRŠTALITOVÁ KORÓZIA
Spolu s uvažovanými typmi korózie pri zváraní ocelí sa rozlišuje aj medzikryštalická (štrukturálna) korózia.
Medzikryštalická korózia je proces fyzikálnej a chemickej deštrukcie kovu pozdĺž hraníc kryštalitov (zŕn) vplyvom agresívneho prostredia, pri ktorom agresívne prostredie preniká hlboko do kovu pozdĺž hraníc zŕn a narúša kovovú väzbu medzi zrnami. Aplikácia aj malého zaťaženia na takýto kov vedie k jeho zničeniu pozdĺž hraníc zŕn. Austenitické nehrdzavejúce ocele sú najviac náchylné na medzikryštalickú koróziu, ale môže sa to vyskytnúť aj v oceliach s vysokým obsahom chrómu, ako aj vo zvaroch feritických, semiferitických a martenzitických tried.
Austenitické ocele, napríklad oceľ 12H18N9Т, sú náchylné na medzikryštalickú koróziu po relatívne dlhom zahrievaní v teplotnom rozsahu 450-850°C. Táto tendencia závisí od veľkého množstva faktorov a najmä od chemického zloženia ocele a dĺžky trvania jeho pobyt pri kritických teplotách.
Vplyv uhlíka na koróznu odolnosť ocele typu 18-9 sa začína prejavovať, keď je jeho obsah vyšší ako 0,02-0,03%. Tento kritický obsah je však možné zvýšiť skrátením doby expozície pri kritických teplotách alebo vyššou rýchlosťou ohrevu a chladenia.
Zo všetkých existujúcich teórií o príčine medzikryštalickej korózie austenitických ocelí je najpravdepodobnejšia teória o separácia karbidov chrómu pozdĺž hraníc zŕn, sprevádzané úbytkom chrómu v oblastiach kovu susediacich s hranicami zŕn. Austenit vo vysoko legovanej austenitickej oceli je pevný roztok chrómu, niklu, mangánu, uhlíka a iných prvkov v železe. Uhlík má obmedzenú rozpustnosť v austenite; pri izbovej teplote nepresahuje stabilný obsah uhlíka v tuhom roztoku austenitu 0,02 až 0,03 %. Pri vyššom obsahu uhlíka v oceli a jej rýchlom ochladzovaní (kalení) je fixovaný v austenite vo forme presýteného nestabilného tuhého roztoku. Oceľ je zároveň imúnna voči medzikryštalickej korózii (obr. 1).
Následné zahrievanie kovu v kritickom teplotnom rozsahu však vedie k uvoľneniu prebytočného uhlíka z tuhého roztoku na hraniciach zŕn vo forme karbidov chrómu Cr4C.
V dôsledku precipitácie karbidov bohatých na chróm klesá obsah chrómu v hraničných vrstvách austenitových zŕn pod 12 % a ukazuje sa ako nedostatočný na udržanie koróznej odolnosti v podmienkach vystavenia agresívnemu prostrediu. Rozdielne obsahy chrómu v samotnom zrne a jeho hraničnej vrstve vplyvom agresívneho prostredia (elektrolytu) vedú k vzniku galvanických mikročlánkov, kde samotné zrno slúži ako katóda a chrómom ochudobnené medzné vrstvy slúžia ako anóda, čo koreluje, čo spôsobuje proces intenzívnej medzikryštalickej korózie v týchto oblastiach zrna .
Ryža. 1. Schéma distribúcie chrómu po zrne austenitickej ocele, náchylnej na medzikryštalickú koróziu: a- v stabilizovanom stave (bez korózie); b- po zahriatí v kritickom teplotnom rozsahu a pri vystavení agresívnemu prostrediu (prítomnosť korózie): 1 - konvenčný tvar austenitového zrna; 2 - karbidy chrómu na hraniciach zŕn; 3 - hraničné oblasti spojené chrómom; 4 - čiary distribúcie chrómu na zrne austenitu.
Na obr. Obrázok 2 ukazuje závislosť medzikryštalickej korózie ocele od teploty a času. Krivka znázorňuje vzťah medzi teplotou ohrevu zvarových spojov ocele typu 18-9 a ich náchylnosťou na medzikryštalickú koróziu.
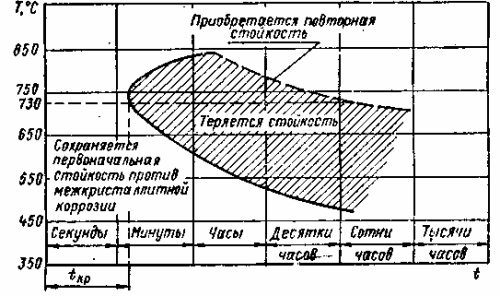
Ryža. 2. Závislosť náchylnosti austenitickej ocele k medzikryštalickej korózii od teploty a doby trvania tejto ocele pri danej teplote (tcr - čas minimálnej stability austenitu)
Ako vyplýva z tejto závislosti, keď sa teplota ohrevu ocele zvýši na 730 °C, kritický čas na to, aby sa oceľ stala citlivou na medzikryštalickú koróziu, sa skráti z niekoľkých hodín na zlomky minúty. Pri dosiahnutí 800-850°C sa náchylnosť na medzikryštalickú koróziu vôbec nevyskytuje. Vysvetľuje sa to rozdielnou rýchlosťou dvoch vzájomne opačných procesov – uvoľňovania karbidov chrómu a difúzie chrómu z centrálnej časti austenitového zrna na jeho okraj. Keď sa teplota zvýši zo 450 na 730 °C, rýchlosť zrážania uhlíka z presýteného roztoku a tvorba karbidov chrómu prebieha rýchlejšie ako rýchlosť difúzie chrómu. V dôsledku toho sa oceľ v kratšom čase stáva náchylnou na medzikryštalickú koróziu. Ďalšie zvýšenie teploty zo 730 na 850 °C vedie k čoraz zrýchlenejšej difúzii chrómu aj z centrálnych oblastí austenitových zŕn a lokálne úbytky chrómu v okrajových oblastiach zŕn neprebiehajú tak rýchlo ako pri nižších teploty. Navyše pri týchto teplotách už ovplyvňuje proces koagulácie a rozpúšťania karbidov v austenite. Z rovnakého dôvodu vedie dlhšia expozícia ocele pri danej teplote k obnoveniu dočasne stratenej odolnosti voči medzikryštalickej korózii (prerušovaná čiara) a pri teplotách 850 °C a vyšších sa náchylnosť na medzikryštalickú koróziu vôbec nevyskytuje.
Zvýšenie obsahu uhlíka v austenitických oceliach zintenzívni tvorbu karbidov chrómu a zvýši sa sklon k medzikryštalickej korózii. V menšej miere ovplyvňujú náchylnosť k medzikryštalickej korózii austenitizačné prvky: nikel a dusík; Keď sa obsah týchto prvkov v austenitických oceliach zvýši, aby sa znížila náchylnosť ocele na koróziu, mal by sa v nej znížiť obsah uhlíka.
Zvýšenie koncentrácie chrómu v austenitickej oceli znižuje stupeň vyčerpania chrómu v okrajových oblastiach a zvyšuje odolnosť ocele voči korózii. Zavedenie molybdénu do ocele zvyšuje odolnosť ocele proti korózii, pretože inhibuje proces oddeľovania karbidov chrómu a tiež preto, že je aktívnym feritizátorom." A oceľ s austeniticko-feritickou štruktúrou (3-5% feritu) je menej náchylná na medzikryštalickú koróziu ako čisto austenitická, pretože v tomto prípade sa pozoruje zjemnenie zŕn a zvýšenie počtu zŕn v kove, čo vedie k zvýšeniu celkovej dĺžky povrchu zŕn a množstva uhlík uvoľnený vo forme karbidov sa výrazne zníži.
Ferit obsahuje viac chrómu ako austenit, takže hoci je chróm vyčerpaný zrážaním karbidov, vo ferite je stále dostatok chrómu, aby odolal medzikryštalickej korózii. Feritové zrná sa nachádzajú vo vnútri austenitových zŕn a ich malá časť je umiestnená pozdĺž hraníc, čo zabraňuje vplyvu agresívneho prostredia na hranice austenitových zŕn.
Titán a niób sú súčasťou austenitických ocelí na potlačenie škodlivých účinkov uhlíka. Tieto prvky, ktoré majú väčšiu afinitu k uhlíku ako chróm, tvoria karbidy ("TiC, NbC), zabraňujúce tvorbe a zrážaniu karbidov chrómu Cr4C. Požadovaný obsah titánu a nióbu v oceli je:
Ti = (5-4-6) C;
Nb = (8 - 10) C,
kde C je obsah uhlíka v hliníkovej oceli.
Titán a niób sú aktívne feritizátory, čo tiež pomôže znížiť sklon k medzikryštalickej korózii.
Na stanovenie mikroštruktúry zvarového kovu chrómniklovej ocele môžete použiť štruktúrne diagramy.
V dôsledku dlhodobých štúdií bolo možné stanoviť účinnosť pôsobenia jedného alebo druhého prvku na štruktúru zvaru v porovnaní s pôsobením hlavných legujúcich nečistôt austenitických ocelí: hlavného feritotvorného prvku chróm a hlavný prvok tvoriaci austenit nikel. Na základe získaných údajov a pôsobenia hlavných prvkov ako jednoty sme skonštruovali Schefflerov štruktúrny diagram pre zvary (obr. 3), kde ekvivalent niklu je daný pozdĺž ordináty a ekvivalent chrómu je znázornený pozdĺž úsečka.
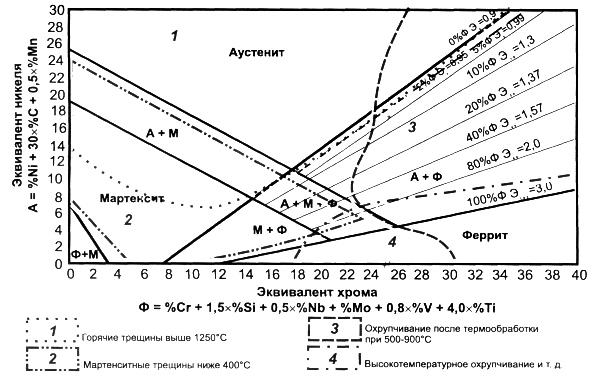
Krehkosť a medzikryštalická korózia
Medzikryštalická korózia je charakterizovaná selektívnou deštrukciou pozdĺž hraníc kovových kryštalitov (zŕn) (obr. 5.91). Nerezové ocele, najmä austenitická trieda, a niektoré neželezné zliatiny sú náchylné na tento typ korózie. Charakteristická je medzikryštalická korózia chrómniklové ocele v podmienkach chladenia zariadení po regenerácii katalyzátorov, niektoré prvky zariadenia na čistenie plynu monoetanolamínu.
Nožová korózia by mala byť podľa charakteru a mechanizmu poškodenia materiálu klasifikovaná aj ako druh medzikryštalickej korózie - deštrukcia tepelne ovplyvnenej zóny susediacej so zvarom konštrukčných prvkov vyrobených z austenitického chrómniklu a iných vysokolegovaných materiálov. ocele. Autor: vzhľad obrysy medzikryštalickej zlomeniny pripomínajú rez ostrým nožom. Korózia noža sa šíri hlboko do kovu vysokou rýchlosťou a výrazne závisí od technológie zvárania.
Ryža. 5,91. Medzikryštalická korózia ocele 12Х18Н10Т z boku vnútorný povrch bezšvové potrubie 0108 x 6 mm vo vzdialenosti (a) a v blízkosti (b) zóny prasknutia potrubia hydrogenačného produktu zariadenia na pyrokondenzát, x 200
Náchylnosť na medzikryštalickú koróziu sa určuje v súlade s GOST 6032-72.
Chemické a petrochemické zariadenia vyrobené z nehrdzavejúcej ocele sú často vystavené medzikryštalickej korózii. Obzvlášť intenzívne sa vyskytuje v prvkoch zariadení vystavených plastickej deformácii: eliptické a guľové dná, ohyby, kolená, zvarové spoje atď.
Pomerne často sa medzikryštalická korózia v nehrdzavejúcich oceliach typu X18N10 vyskytuje vo zvitkoch rúrových pecí používaných na ohrev produktov katalytického krakovania ropy. Cievky sú obmývané spalinami s teplotami do 1200°C v radiačnej časti a do 700°C v konvekčnej časti. Ako palivo v peci sa používajú uhľovodíkové plyny obsahujúce 1,2-4,5 % S. Spaliny spolu s CO a N0 obsahujú S03 až 1426 mg/m3.
Analýza príčin medzikryštalickej korózie ukazuje, že jej výskyt je spojený s vystavením prostrediu kyseliny sírovej, ku ktorému dochádza počas spúšťania a odstavovania pece. Časté prerušenia v surovinách, ktoré spôsobujú zvýšenie frekvencie zastavovania a spúšťania pecí, prispievajú k rozvoju medzikryštalickej korózie. Vzniká anhydrid kyseliny sírovej, ktorý sa spája s vodnou parou kyselina sírová, usadzujúce sa na potrubiach vo forme hygroskopických síranov.
Podľa údajov bol vo zvarovom spoji zvitku (s priemerom 219 mm a hrúbkou steny 10 mm) sálavej časti pece po 2520 hodinách prevádzky zistený únik média do priestoru pece. . V sedimente na cievke dosiahol obsah S042- 22,12 %. Po odstránení výstuže inštalačného zvaru je viditeľná sieť trhlín po celej ploche naneseného kovu. V tomto prípade otvor trhliny nepresiahol 0,3 mm a dĺžka bola 1,5-3 mm. Hĺbka súvislej medzikryštalickej korózie na vnútornom povrchu základného kovu konvenčnej pecnej cievky dosiahla 1,1-1,3 mm.
Medzikryštalická korózia je nebezpečná, pretože v prítomnosti zvyškových zváracích napätí a tepelných cyklov štart-stop sa rozvinie do korózneho praskania pod napätím.
Príčina medzikryštalickej korózie austenitických nehrdzavejúcich ocelí je spojená s tvorbou precipitátov na hranici zŕn karbidov obohatených chrómom. o vysoké teploty Nerezové ocele klasického zloženia (18% Cr, 9% Ni) sú schopné rozpúšťať veľké množstvo intersticiálnych prvkov (C a N). Avšak pod 900 °C rozpustnosť týchto prvkov prudko klesá. Pri tradičnom spracovaní ocele do tuhého roztoku po kalení 
Ryža. 5,92. Zrážanie karbidov chrómu Cr23C6 pozdĺž hraníc zŕn a podzŕn v oceli 08Х18Н10Т po zahriatí na 650 °С, 100 h TEM x 16000
Presýtený tuhý roztok obsahuje značné množstvo uhlíka a dusíka. V dôsledku následnej tepelnej expozície pri 450-700°C vznikajú na hraniciach zŕn chrómom obohatené precipitáty M23C6 (obr. 5.92). Za týchto podmienok sa ukáže, že časti zŕn susediace s precipitátmi na hraniciach zŕn sú ochudobnené o chróm a sú náchylné na rozpúšťanie v určitých vodných roztokoch.
V rúrach prehrievača vyrobených z austenitickej nehrdzavejúcej ocele 12Х18Н10Т s teplotou pary 570 °С dochádza v dôsledku prehriatia vonkajšieho povrchu k redistribúcii chrómu. V týchto oblastiach sa tvoria karbidy s vysokým obsahom chrómu pri súčasnom úbytku chrómu v objeme hraničného zrna menej ako 12 %, čo spôsobuje oxidáciu ocele. V dôsledku toho sa pevnosť steny rúrky v makroreze prudko znižuje a dochádza k intergranulárnej deštrukcii, počnúc od vykurovacej plochy.
Najnebezpečnejšie teploty sú 500-550°C, pri ktorých nerezová oceľ typu X18N10T, bez ohľadu na chemické zloženie a teplotu kalenia, sa stáva náchylnou na medzikryštalickú koróziu (senzibilizuje). V senzibilizovanej oceli je medzikryštalická korózia obzvlášť viditeľná počas odstávok v hydrorafinačných jednotkách.
Navrhuje sa jednoduchá schéma na vytvorenie jamy (depresie) na oceli. Rýchlosť oxidácie na holom kovovom povrchu môže byť o niekoľko rádov vyššia ako na povrchu pokrytom ochranným pasivačným filmom. o
Za určitých podmienok je obsah kyslíka v roztoku vo vnútri jamy značne znížený katódovou reakciou. Z tohto dôvodu nie je zvýšenie koncentrácie kovových iónov v roztoku vyvážené zvýšením koncentrácie OH- podľa reakcie
2H20 + 02 + 4е - "40Н",
a roztok si zachováva nadbytočný kladný náboj.
Chloridové ióny majú obzvlášť silný vplyv na sklon k selektívnej korózii s tvorbou bodovej korózie. Chloridy kovov hydrolyzujú vodu, čo vedie k zníženiu pH roztoku:
M "C1- + n2o - M OH- + H+ + C1".
Znížené pH a zvýšená aktivita chloridového iónu v roztoku vo vnútri priehlbiny (jamky) spôsobujú ďalšie zvýšenie rýchlosti oxidácie kovu. Tento rast spôsobuje ďalšie zvýšenie prítoku chloridových iónov do jamy a proces sa stáva autokatalytickým.
Periodickými kontrolami pomocou ultrazvukovej kontroly sa zistilo, že v štyroch zváraných nádržiach s objemom 40 m3 vyrobených z ocele X18N9 na skladovanie zlúčenín kyseliny dusičnej je najvyšší stupeň medzikryštalickej korózie zistený na spojoch pozdĺžnych a obvodových zvarov. Táto korózia sa vyvíja iba v zóne kontaktu kovu s plynnou fázou pracovného produktu. Nožová a bodová korózia existuje v kove, ktorý prichádza do styku s plynnou aj kvapalnou fázou pracovného produktu. Zároveň sa najsilnejší nárast prevádzkových defektov pozoruje v kontajneroch v horúcom podnebí (obr. 5.93, a). Hĺbka defektov rastie monotónne takmer konštantnou rýchlosťou (8-9) 105 m/rok pre nádrže v miernom podnebí a (24-35) 10"5 m/rok pre nádrže prevádzkované v horúcom klimatickom pásme (obr. 5,93, b).
Fenomén korózneho praskania nehrdzavejúcich ocelí v prostredí s obsahom chloridov je charakterizovaný vývojom lomu podľa mechanizmu krehkého transgranulárneho štiepenia. Takýto obraz deštrukcie bol zaznamenaný pri štúdiu ocele 12H18N10Т po testovaní korózneho praskania vo vriacom 30% vodnom roztoku MgCl2. Pri poklese úrovne ťahových napätí z 0,7 na 0,2 o0 2 v lome výrazne narastá podiel krehkých transkryštalických štiepnych faziet so sieťou sekundárnych trhlín. Štiepne fazety majú vlnitý vzor charakteristický pre kovy s bcc mriežkou. 
Ryža. 5,93. Zmeny priemernej rýchlosti medzikryštalickej korózie (a) a hĺbky defektov (b) v kontajneroch prevádzkovaných v horúcich (o) a miernych ( ) klimatických zónach
Charakteristickým znakom vlnkového vzoru v kove s fcc mriežkou je zmena smerov krokov štiepenia nielen na hranici zŕn, ale aj vo vnútorných objemoch zŕn. Na povrchu faziet sa objavujú cikcaky - rímsy prúdového vzoru. Táto zmena smeru riečiska je spôsobená priesečníkom roviny porušenia medzi nízkymi uhlami a dvojitými hranicami.
