पाण्याची कडकपणा आणि त्याचे निर्मूलन. आयए उपसमूहातील धातूंसाठी कार्ये आणि व्यायाम
पृष्ठ 1
उकळत्या पाण्यातून तात्पुरती कडकपणा दूर केली जाते. उकळल्यावर हायड्रोकार्बोनेट नष्ट होते आणि असमाधानकारकपणे विद्रव्य कार्बोनेट तयार होतात. जेव्हा सोडियम कार्बोनेट, कॅल्शियम हायड्रॉक्साईड पाण्यात प्रवेश केला जातो तेव्हा पाण्याचे एकूण कठोरता दूर होते. या प्रकरणात, चुन्याने कार्बोनेट कडकपणा दूर केला जातो, आणि सोडाद्वारे कार्बनयुक्त कठोरपणा दूर केला जातो.
तात्पुरते कडकपणा काढून टाकण्याव्यतिरिक्त, चुना सर्व मॅग्नेशियम आणि लोह पाण्यापासून खाली आणते आणि सेंद्रीय आणि अजैविक कोलोइड्सच्या जमावास प्रोत्साहित करते.
अशुद्धी साफ केल्यावर, तात्पुरती कडकपणा आणि डीएरेशन काढून टाकल्यानंतर, मेक-अप पाणी उष्मा एक्सचेंजर (2) मध्ये दिले जाते, जेथे ते गरम केले जाते 335 के. हीटिंग नेटवर्क
पाण्याची कमतरता दूर करण्यासाठी, बंद फिरणार्\u200dया पाणीपुरवठा यंत्रणेत नुकसानाची पूर्तता करण्यासाठी (पुनर्भरण) करण्यासाठी तसेच फिरणार्\u200dया पाण्याच्या संपर्कात उष्णता-एक्सचेंजिंग आणि पृष्ठभागावर थंड होणार्\u200dया पृष्ठभागावर खनिज गळती रोखण्यासाठी नरमाईचा वापर केला जातो. बर्\u200dयाच प्रकरणांमध्ये, मेक-अप पाणी परिसंचरण पाण्यामध्ये कॅल्शियम आयन आणि बायोकार्बोनेट्स जमा होण्याचे मुख्य स्त्रोत आहे, जे उच्च बाष्पीभवन गुणांक असलेल्या सिस्टममध्ये फिरणार्\u200dया पाण्याच्या स्थिर रचनामध्ये व्यत्यय आणू शकते.
तात्पुरती कडकपणा दूर करण्यासाठी पाण्याचे मऊ करणे, अभिकर्मकांचा परिचय करून रासायनिक पद्धतीने केले जाते, जे चुना, गंधकयुक्त किंवा हायड्रोक्लोरिक acidसिड म्हणून वापरले जातात. रासायनिक पद्धती तुलनेने उथळ पाण्याने मऊ होतात. मुलायमतेच्या उच्च प्रमाणात, कॅशन एक्सचेंज पद्धती वापरल्या जातात, त्यातील सार म्हणजे त्यामध्ये असलेल्या सोडियमच्या कॅशन्सची देवाणघेवाण करण्यासाठी विशिष्ट पदार्थांच्या क्षमतेचा वापर पाण्यात कडकपणाच्या क्षारांच्या केशनसाठी केला जातो.
पाण्याचे रासायनिक पृथक्करण करण्यासाठी वनस्पतींमध्ये वापरल्या जाणार्\u200dया एनोव्हिटिक फिल्टरच्या पुनरुत्पादनासाठी पाण्याचे तात्पुरते कडकपणा दूर करण्यासाठी कॉस्टिक सोडाचा वापर औष्णिक उर्जा संयंत्रांमध्ये केला जातो.
कास्टिकिक सोडा थर्मल पॉवर प्लांट्समध्ये पाण्याचे तात्पुरते कडकपणा दूर करण्यासाठी आणि रासायनिक पृथक्करण वनस्पतींमध्ये वापरले जाणारे ionनीओनिक फिल्टर पुन्हा निर्माण करण्यासाठी वापरले जाते.
त्याचप्रमाणे तात्पुरते ताठरपणा दूर करण्यासाठी आवश्यक असलेल्या सीए (ओएच) 2 ची देखील गणना केली पाहिजे.
का, मॅग्नेशियम लवणांमुळे तात्पुरते ताठरपणा दूर करण्यासाठी, कॅल्शियम क्षारांमुळे तात्पुरते कडकपणा दूर करण्यापेक्षा जास्त चुना आवश्यक आहे.
म्हणूनच, बंद (शुद्धी-मुक्त) पाणीपुरवठा यंत्रणेचे रिचार्ज करण्यासाठी, मेक-अप पाण्याचे तुलनेने खोल मऊ करणे आणि तात्पुरते कडकपणा दूर करणे आवश्यक आहे.
अल्कधर्मी अभिकर्मकांच्या थोड्या प्रमाणात प्रमाणात पाण्यामुळे पाण्याच्या चुंबकीय उपचारांची कार्यक्षमता वाढते, जरी क्षारीय अभिकर्मकांचा परिचय, उदाहरणार्थ, 10% पेक्षा जास्त प्रमाणात चुना - - १ 195 9 in मध्ये KhIEI येथे केलेल्या अभ्यासानुसार तात्पुरते कडकपणा दूर करण्यासाठी आवश्यक असलेल्यांपैकी २०%, प्रमाणात निर्मिती कमी करते. 8 ते 10 वेळा.
अशा परिस्थितीत, बायकार्बोनेट्समुळे उद्भवलेल्या सहा-हाडांचे पाणी काढून टाकले जाते. म्हणून, या ताठरपणास तात्पुरते किंवा बायकार्बोनेट असे म्हणतात. म्हणून, तात्पुरते कडकपणा दूर करण्यासाठी, पाणी उकळण्यासाठी पुरेसे आहे.
सतत कडकपणाचे मीठ, उदाहरणार्थ, सीएसीएल, सीएएसओ 4 इत्यादी गरम झाल्यावर पाण्यामधून काढले जात नाहीत. ते पाण्याच्या बाष्पीभवन दरम्यान क्षीण होते, ते उपकरणांच्या भिंतींवर दाट प्रमाणात काढणे कठीण होते. कठोर पाण्याचा वापर फक्त अशा परिस्थितीत केला जाऊ शकतो जेव्हा त्याच्या वापराच्या अटींमुळे घन वर्षाव होण्याची शक्यता नसते, उदाहरणार्थ, रेफ्रिजरेटरमध्ये जेथे थंड पाण्याचे तापमान तपमानावर गरम होत नाही जे तात्पुरते कडकपणा दूर करण्यास मदत करते. बॉयलर वनस्पतींमध्ये, जेथे पाणी केवळ गरम होत नाही तर बाष्पीभवन देखील होते, केवळ तात्पुरतेच नाही तर सतत कठोरता देखील अस्वीकार्य आहे. म्हणूनच, त्यांच्यासाठी पाणी प्रामुख्याने कॅल्शियम आणि मॅग्नेशियम ग्लायकोकॉलेटपासून विशेष वनस्पतींमध्ये असलेल्या रसायनाद्वारे शुद्ध केले जाते.
मनपा शैक्षणिक संस्था
"माध्यमिक शाळा क्रमांक 1
वैयक्तिक विषयांच्या सखोल अभ्यासासह
पत्ता: बेल्गोरोड प्रदेश,
पाण्याची कडकपणा चाचणी
आणि ते दूर करण्याचे मार्ग
विद्यार्थी 11 "अ" वर्ग सामंजस्य करार "सरासरी
माध्यमिक शाळा क्रमांक 1
सखोल अभ्यासासह
स्वतंत्र आयटम
पत्ता: बेल्गोरोड प्रदेश,
वैज्ञानिक सल्लागार :,
रसायनशास्त्र शिक्षक
माध्यमिक शाळा क्रमांक 1
सखोल अभ्यासासह
स्वतंत्र आयटम
नॉव्ही ओस्कोल, बेल्गोरोड प्रदेश
पत्ता: बेल्गोरोड प्रदेश,
नॉव्ही ओस्कोल,
नॉव्ही ओस्कोल
१. परिचय ……………………………………………………………………….
२. पाण्याची कडकपणा आणि निर्मूलन करण्याच्या पद्धती …………………………… .4
Water पाणी का कठीण होते .....................................
Life मानवी जीवनात पाण्याच्या कठोरतेचे मूल्य ...................................... 4
Sti कडकपणा दूर करण्याचे मार्ग ……………………………………… ... 5
Water. पाण्याच्या कडकपणाचा अभ्यास आणि त्यापासून मुक्त होण्याच्या पद्धती .............. ... 8
Con. निष्कर्ष आणि निष्कर्ष
Re. संदर्भांची यादी
परिचय
ज्याने विज्ञानांचा अभ्यास केला, परंतु त्या लागू करत नाहीत,
जो नांगरला, पण पेरला नाही अशा माणसासारखेच आहे.
साडी
20 व्या शतकाच्या 80 च्या दशकात, पॉल चॅपियस ब्रॅगची पुस्तके निरोगी जीवनशैलीच्या प्रगतीवर दिसून आली. आणि जरी बरेच विद्वान त्यांच्या मते विवादास्पद मानतात, परंतु पॉल ब्रॅगची पुस्तके लक्ष देण्यास पात्र आहेत. त्यांच्या पुस्तकातील एक भाग (कठोरपणाचा माझा पहिला प्रयोग) पाण्याच्या कडकपणाच्या समस्येसाठी समर्पित आहे, जेथे त्याच्या आठवणींमध्ये लेखक आपल्या आजोबांच्या आजाराचे वर्णन करतात, ज्यामुळे त्याच्या रक्तवाहिन्या कडक पाण्यामुळे भयानक झाल्या आणि त्यांच्या भागांमध्ये राहणारी स्त्री ( दुर्दैवी महिलेला दगडी स्त्री म्हणून संबोधले जात असे, कारण तिच्या शरीरावर मोठ्या संख्येने क्षारांद्वारे अक्षरशः भयानक धमकी दिली होती). ती स्त्री कठोर पाण्यामुळे बळी पडलेल्यांपैकी एक होती. दुर्दैवी अवयव अशा पाण्यात असलेल्या मोठ्या प्रमाणात अजैविक पदार्थांच्या प्रक्रियेचा सामना करण्यास अयशस्वी ठरले आणि ते तिच्या शरीरात खूप सक्रियपणे जमा होऊ लागले.
कॅल्शियम संयुगे मूत्रपिंड दगड आणि पित्त मूत्राशयच्या रूपात आपल्या शरीरात वर्षाव करतात.
आज, पाण्याची प्रक्रिया ही एक लबाडी आणि लाड नाही, उलट एक महत्वाची गरज आहे. वस्तुस्थिती अशी आहे की मैल, तृतीय-पक्ष स्मॅक, गंध, तसेच ढगाळ उपस्थिती यासारख्या अप्रिय घटनेमुळे केवळ खूपच गैरसोय होत नाही तर बर्\u200dयाच रोग देखील होतात. कमी-गुणवत्तेचे पाणी क्षारांच्या साठवणुकीस प्रोत्साहित करते, शरीराच्या वृद्धत्वाच्या प्रक्रियेस गती देते, आणि बर्\u200dयाच रोगांच्या तीव्र अवस्थेत संक्रमण होण्याचे कारण बनते. याव्यतिरिक्त, क्लोरीनमध्ये असंख्य पदार्थ असतात ज्यामुळे कर्करोग होऊ शकतो. परंतु पाणी हा सर्व जीवनाचा आधार आहे आणि एकच जीव पाण्याशिवाय करु शकत नाही. उदाहरणार्थ, एखाद्या व्यक्तीमध्ये 60-65% इतके पाणी असते. म्हणून, स्वच्छ पाणी प्रत्येक व्यक्तीसाठी महत्त्वपूर्ण आहे. दुर्दैवाने, आमच्या काळातील नैसर्गिक पाणी प्राथमिक उपचारांशिवाय वापरासाठी पूर्णपणे अनुपयुक्त आहे, ज्याचे पाण्याच्या विविध विश्लेषणाद्वारे पुष्टी आहे. प्रत्येकाला ठाऊक आहे की पाण्याचे शुद्धीकरण करणार्\u200dया गाळण्या स्टेशनांना मोठ्या दुरुस्तीची फार पूर्वीपासून गरज भासली आहे आणि ज्या पाणीपुरवठा यंत्रणेद्वारे आमच्या घरात पाणी जाते तेथील बदली आवश्यक आहे.
आमच्या कामाचे उद्दीष्ट आमच्या गावात पाण्याच्या कडकपणाच्या पातळीचा अभ्यास करणे हे होते.
पाण्याची कडकपणा आणि त्याच्या निर्मूलनासाठी पद्धती
पाणी का कठीण होते?
कॅल्शियम आणि त्याचे संयुगे शरीरासाठी अत्यंत आवश्यक आहेत: सर्वकाही, हे कॅल्शियम ऑर्थोफॉस्फेट सीए 3 (पी 0) 2 पासून आहे जे मानवांमध्ये आणि प्राण्यांच्या हाडे आणि दात असतात. ते विरघळणारे कॅल्शियम संयुगे तयार करतात, जे शरीरात रक्त वाहतात. कॅल्शियम केटेशन्स Ca2 + चे आभार, रक्त गोठण्यास, गुठळ्या तयार करण्यास, जखमांवर जखम आणि रक्तस्त्राव थांबविण्यास सक्षम आहे.
कॅल्शियम संयुगे केवळ उपयुक्तच नाहीत तर अत्यंत हानिकारक देखील आहेत - उदाहरणार्थ जेव्हा ते सामान्य पाण्याला कडकपणा देतात. दैनंदिन जीवनात, "कडकपणा" हा शब्द पहिल्या दृष्टीक्षेपात फक्त घन पदार्थांवरच लागू केला जाऊ शकतो: एक पार्क बेंच किंवा स्वयंपाकघरातील स्टूल घन असू शकते. तथापि, पाणी देखील कठीण आहे.
पाण्यामध्ये प्रवेश करणारे मॅग्नेशियम आणि कॅल्शियम ग्लायकोकॉलेटचा मुख्य स्रोत म्हणजे चुनखडी, जिप्सम आणि डोलोमाइट्सचे साठे जे नैसर्गिक पाण्यामुळे कमी होतात.
कमी खारट पाण्यामध्ये, बहुतेक कॅल्शियम आयन. खनिजतेच्या पदवीमध्ये वाढ झाल्यामुळे, कॅल्शियम आयनची सामग्री वेगाने कमी होते आणि क्वचितच 1 ग्रॅम / एलपेक्षा जास्त आहे. खनिज पाण्यात मॅग्नेशियम आयनची सामग्री अनेक ग्रॅम पर्यंत पोहोचू शकते, आणि मीठ पाण्यात अनेक ग्रॅम दहापट.
पाण्याची कडकपणा - त्यात क्षारीय पृथ्वीच्या धातूंचे विरघळलेले लवणांच्या सामग्रीशी संबंधित पाण्याचे रासायनिक आणि भौतिक गुणधर्मांचे मिश्रण, मुख्यत: कॅल्शियम आणि मॅग्नेशियम. अशा क्षारांच्या उच्च सामग्रीसह पाण्याला कठोर पाणी असे म्हणतात, कमी सामग्रीसह - मऊ. हायड्रोकार्बोनेट्सद्वारे तयार केलेले तात्पुरते कडकपणा (कार्बोनेट) आणि इतर क्षारांच्या अस्तित्वामुळे कायमस्वरुपी कडकपणा (नॉन-कार्बोनेट) असतात. पाण्यात कॅल्शियम आणि मॅग्नेशियम बायकार्बोनेट्स (सीए (एचसीओ 3) 2; एमजी (एचसीओ 3) 2) च्या अस्तित्वामुळे तात्पुरती कडकपणा आहे. सल्फेट्स, सीए आणि एमजी क्लोराईड्स (सीएएसओ 4, सीएसीएल 2, एमजीएसओ 4, एमजीसीएल 2) च्या पाण्यात उपस्थिती असल्यामुळे सतत पाण्याची कडकपणा होतो.
मानवी जीवनात पाण्याच्या कडकपणाचे मूल्य
पाण्याची कडकपणा ही कॅल्शियम आयन सीए 2 + आणि मॅग्नेशियम एमजी 2 + पाण्यात विरघळल्याची बेरीज आहे.
कॅल्शियम आणि मॅग्नेशियम आयन सजीव प्राण्यांचे जास्त नुकसान करीत नाहीत, परंतु पाण्यात त्यांची मोठ्या प्रमाणात उपस्थिती अवांछनीय आहे, कारण असे पाणी घरगुती गरजा योग्य नसते.
कठोर पाण्यात, कपडे, मांस आणि भाज्या धुताना साबण आणि पावडरचा वापर वाढतो आणि पोटातील हालचाल कमी होते. पाणीपुरवठा यंत्रणा आणि पाणी तापविण्याच्या उपकरणांसाठी कठोर पाणी अयोग्य आहे.
कठोरता प्रति लिटर (एमईक्यू / एल) मिलीग्राम समतुल्य मध्ये मोजली जाते. अनुज्ञेय ताठरपणाच्या मूल्यांसाठी उद्योगांचे मानके वापरल्या गेलेल्या उपकरणांवर अवलंबून असतात. थोडक्यात, 1 एमएक / एल किंवा त्याहून अधिक कठोरतेसह कठोर पाणी मानले जाते.
कडकपणा ही पाण्याची गुणवत्ता ही सर्वात सामान्य समस्या आहे. मूलतः, "हार्ड वॉटर" हा शब्द धुण्यास कठीण असलेल्या पाण्यावर लागू झाला.
कडक पाणी, धुऊन झाल्यावर त्वचा कोरडे होते, साबण वापरताना त्यामध्ये फेस खराब तयार होत नाही. कठोर पाण्याच्या वापरामुळे बॉयलर्सच्या भिंतींवर, पाईप्स इत्यादीमध्ये गाळ (स्केल) दिसून येतो त्याच वेळी, खूप मऊ पाण्याच्या वापरामुळे पाईप्सची गंज वाढू शकते, कारण या प्रकरणात हायड्रोकार्बोनेटद्वारे acidसिड-बेस बफरिंग पुरवले जात नाही. (तात्पुरते) कडक होणे. कडक किंवा मऊ पाण्याचे सेवन करणे आरोग्यासाठी घातक नसते, परंतु उच्च कडकपणामुळे मूत्रमार्गात दगड तयार होण्यास हातभार लागतो आणि कमी - पुरावा असूनही हृदय व रक्तवाहिन्यासंबंधी रोगाचा धोका कमी होतो.
नैसर्गिक पाण्याची कडकपणा मोठ्या प्रमाणात बदलू शकते आणि वर्षभर अस्थिर असते. पाण्याचे बाष्पीभवन झाल्यामुळे कडकपणा वाढतो, पावसाळ्यात कमी होतो तसेच बर्फ आणि बर्फ वितळण्या दरम्यान कमी होतो.
ताठरपणा दूर करण्याचे मार्ग
भेद करा एकूणच कडकपणा, जे बनलेला आहे तात्पुरते आणि स्थिर.
उकळणे.
तात्पुरते कडकपणा (डिस्पोजेबल किंवा कार्बोनेट) पाण्यात Ca (HCO3) 2 आणि Mg (HCO3) 2 बायकार्बोनेटच्या अस्तित्वामुळे होते. कार्बनची कडकपणा काढून टाकणे सोपे आहे उकळत्या पाण्यातज्यामध्ये Ca2 + आणि Mg2 + अघुलनशील प्रीसिपीट्स तयार करण्यासाठी काढले आहेत:
Ca (HCO3) 2 CaCO3 CO + CO2 + H2O
मिलीग्राम आयन बेसिक कार्बोनेटच्या स्वरूपात किंवा मॅग्नेशियम हायड्रॉक्साईडच्या स्वरूपात (पीएच\u003e 10.3 येथे) वर्षाव करतात.
2Mg2 + + OH) 2CO3 CO + CO2 + H2O
(ओएच- आयन पाण्याबरोबर आयनांच्या परस्परसंवादामुळे तयार होतात: आणि गरम झाल्यावर समतोल उजवीकडे वळते).
कार्बोनेट कडकपणा कमी करण्यासाठी मर्यादित पद्धत ज्यामध्ये पाण्याचा उपचार केला जातो चुनासीए (ओएच) 2. चुन्याच्या परिचयानंतर होणाring्या प्रतिक्रियांना आण्विक स्वरूपात लिहिले जाऊ शकते:
Ca (HCO3) 2 + Ca (OH) 2 → 2CaCO3 ↓ + H2O
मिलीग्राम (НСО3) 2 + Са (ОН) 2 → मिलीग्राम (ОН) 2 ↓ + 2СаСО3 + Н2О
जेव्हा पाणी उकळले जाते तेव्हा सतत कठोरता (पुन्हा न मिळवता येण्यायोग्य किंवा नॉन-कार्बोनेट) राखली जाते, कारण सतत कडकपणा सल्फेट्स, क्लोराईड्स आणि सीए आणि एमजीच्या इतर लवणांच्या पाण्यामुळे होते. परिमाणवाचक, ते वेळेची कठोरता वजा Ca2 + आणि Mg2 + आयनच्या एकाग्रतेइतकेच आहे. सहसा कार्बोनेट कडकपणा कमी करण्यासाठी वापरला जातो. कॅल्सीन सोडा (Na2CO3):
MgSO4 + Na2CO3 → MgCO3 ↓ + Na2SO4
जोडताना चुना आणि सोडा आपण कार्बोनेट आणि नॉन-कार्बोनेट कठोरपणापासून मुक्त होऊ शकता ( चुना-सोडा पद्धत).
सर्व कठोरता देखील दूर केली जाते परिचय सोडियम फॉस्फेट, सोडियम टेट्राबोरेट ऑर्थोफॉस्फेट कार्बोनेटपेक्षा कमी विद्रव्य असल्याने पाण्याचा मऊ बनवण्यासाठी त्यांचा वापर अधिक सोयीस्कर आहे:
3CaSO4 + 2Na3PO4 → Ca3 (PO4) 2 ↓ + 3Na2SO4
पाणी मऊ करण्याचे आधुनिक मार्ग यावर आधारित आहे वापरत आहे आयन एक्सचेंज रेजिन - आयन एक्सचेंजर्स (कॅशन एक्सचेंजर्स आणि आयन एक्सचेंजर्स). केशन एक्सचेंजर सिंथेटिक आयन-एक्सचेंज रेजिन असतात - एल्युमिनोसिलिकेट्स, उदाहरणार्थः
त्यांची रचना सशर्तपणे Na2R सामान्य सूत्रानुसार व्यक्त केली जाऊ शकते, जिथे ना + हे एक अत्यधिक मोबाइल केशन आहे आणि आर - एक केटेशन एक्सचेंजर कण आहे ज्यामध्ये नकारात्मक शुल्क आकारले जाते.
जेव्हा केटेशन एक्सचेंज राळच्या थरातून कठोर पाणी वाहते तेव्हा प्रतिक्रियांनुसार केटेशनची देवाणघेवाण होते:
Ca2 + + Na2R → 2Na + + CaR
Mg2 + + + Na2R → 2Na + + MgR
अशाप्रकारे, सीए 2 + आणि एमजी 2 + आयन सोल्यूशनपासून केशन एक्सचेंज रेझलपर्यंत जातात. केशन एक्सचेंज राळ पुनर्संचयित करण्यासाठी, ते एनएसीएलच्या एकाग्र सोल्यूशनने धुऊन आहे:
CaR + 2NaCl → CaCl2 + Na2R
वॉशिंगनंतर, पाण्यापासून ताठरपणा दूर करण्यासाठी पुन्हा कॅशन एक्सचेंज रेझिनचा वापर केला जाऊ शकतो.
उलट ऑस्मोसिस. ही पद्धत semipermeable पडदा (सहसा पॉलीमाईड) च्या माध्यमातून पाण्याचा मार्ग आधारित आहे. कडकपणाच्या क्षारांसह, इतर बहुतेक क्षार देखील काढून टाकले जातात. साफसफाईची कार्यक्षमता 99.9% पर्यंत पोहोचू शकते. घरगुती पिण्याच्या पाण्याचे शुद्धीकरण प्रणालीमध्ये या पद्धतीचा सर्वात मोठा वापर आढळला आहे. या पद्धतीचा गैरसोय म्हणून, रिव्हर्स ऑस्मोसिस झिल्लीला पुरविला जाणा water्या पाण्याची प्राथमिक तयारी लक्षात घेणे आवश्यक आहे.
इलेक्ट्रोडायलिसिस हे विद्युत् क्षेत्राच्या कृतीतून पाण्यापासून लवण काढून टाकण्यावर आधारित आहे. विरघळलेल्या पदार्थांचे आयन काढून टाकणे विशेष पडद्यामुळे होते. रिव्हर्स ऑस्मोसिस तंत्रज्ञानाप्रमाणेच इतर क्षारही काढले जातात, कडकपणा आयन व्यतिरिक्त.
औष्णिक पद्धत. वॉटर हीटिंगच्या आधारावर, केवळ तात्पुरते (कार्बोनेट) कडकपणा काढून टाकते. दररोजच्या जीवनात अनुप्रयोग शोधतो. उद्योगात उदाहरणार्थ, औष्णिक उर्जा संयंत्रांमध्ये याचा वापर केला जातो.
अभिकर्मक मऊ करणे. ही पद्धत सोडा किंवा पाण्यात चिकटलेला चुना घालण्यावर आधारित आहे. या प्रकरणात, कॅल्शियम आणि मॅग्नेशियम ग्लायकोकॉलेट अघुलनशील संयुगात जातात आणि परिणामी, वर्षाव होतो. ही पद्धत तुलनेने जास्त पाण्याच्या वापरावर न्याय्य आहे, कारण ती बर्\u200dयाच विशिष्ट अडचणींच्या समाधानाशी संबंधित आहे: गाळ फिल्टर, रेजेन्टची अचूक डोस.
कॅशनेशन आयन-एक्सचेंज ग्रॅन्युलर लोडिंग (बर्\u200dयाचदा आयन-एक्सचेंज रेजिन) च्या वापरावर आधारित ही पद्धत आहे. पाण्याशी संपर्क साधल्यानंतर असा संपर्क कठोरपणाच्या लवण (कॅल्शियम आणि मॅग्नेशियम) चे कॅशन्स शोषून घेतो. त्या बदल्यात, आयनिक स्वरूपावर अवलंबून सोडियम किंवा हायड्रोजन आयन देऊन. या पद्धतींना अनुक्रमे ना-कॅशन आणि एच-कॅशन म्हणतात. नियमानुसार, पाण्याचे कडक होणे सिंगल-स्टेज सोडियम केटेशनसह 0.05-0.1 एमईक्यू / एल पर्यंत कमी होते, दोन-टप्प्यासह - 0.01 एमएक / एल पर्यंत.
उत्कृष्ट अभिकर्मक पाण्याचे सर्वसाधारण कडकपणा दूर करण्यासाठी सोडियम ऑटोफॉस्फेट ना 3 पीओ 4: 3 सीए (एचसीओ 3) 2 + 2 एनए 3 पीओ 4 सीए 3 (पीओ 4) 2 ↓ + 6 एनएएचसीओ 3 एमजीएसओ 4 + 2 ना 3 पीओ 4 → एमजी 3 (पीओ 4) 2 ↓ + 3 ना 2 एसओ 4 वायर्सॉस्पीय व्हर्लॉजिकल सोल्यूशियम आहे चांगले पाणी मऊ करणे. उद्योगात, आयन-एक्सचेंज फिल्टर्स वापरुन, कॅल्शियम आणि मॅग्नेशियम आयन सोडियम आणि पोटॅशियम आयनऐवजी मऊ पाणी तयार करतात. पिण्याच्या पाण्यासाठी घरातील फिल्टरमध्ये पाण्याचे काही प्रमाणात नरम होते. फिल्टर केलेले पाणी कमी प्रमाणात देते. डिस्टिलेशन (डिस्टिलेशन) द्वारे पाणी पूर्णपणे शुद्ध केले जाऊ शकते.
आज उत्कृष्ट आहेत पाणी फिल्टर जे समस्या न घेता अपार्टमेंटमध्ये स्थापित केले जातात आणि उच्च-गुणवत्तेच्या पाण्याचे उपचार करण्यासाठी एक उत्कृष्ट साधन म्हणून काम करतात. कदाचित आज बरेच लोक सुपरमार्केटमध्ये बाटलीबंद शुद्ध पाणी विकत घेण्यास प्राधान्य देतात. अशा पाण्याची निवड खरोखरच प्रचंड आहे, परंतु त्याच्या गुणवत्तेबद्दल 100% खात्री असणे शक्य आहे काय? कदाचित नाही! म्हणूनच शुद्धीकरणासाठी विशेषतः डिझाइन केलेल्या फिल्टरच्या मदतीने जल शुध्दीकरण हा एक आधुनिक व्यक्ती जो त्याच्या आरोग्याबद्दल आणि आपल्या प्रियजनांच्या आरोग्याची काळजी घेतो त्याचे सर्वात चांगले समाधान आहे. जल शुध्दीकरण प्रणाली खूप वैविध्यपूर्ण आहेत. नियमानुसार, ते भिन्न आहेत: कार्यप्रदर्शन, काही पॅरामीटर्स, जल शुध्दीकरणाची डिग्री तसेच डिझाइन. वॉटर फिल्टर्स उत्तम प्रकारे स्वच्छ पाणी पितात आणि त्यास पिण्यासाठी उपयुक्त ठरतात, त्यामध्ये अॅल्युमिनियम, लोह, मॅंगनीज, क्लोरीन आणि सर्व प्रकारच्या नायट्रेट्सची सामग्री कमी करतात. याव्यतिरिक्त, जल शुध्दीकरणासाठी फिल्टर अप्रिय गंध, चव दूर करण्यास तसेच पाण्यात असलेल्या जंतू आणि जीवाणूपासून मुक्त होण्यास मदत करते. अशा प्रणालीद्वारे शुद्ध केलेले पाणी कमी कठोर होते, तथापि, ते मानवी शरीरासाठी आवश्यक उपयुक्त पदार्थ गमावत नाही. आपले घर न सोडता अमर्यादित प्रमाणात शुद्ध पाणी मिळविण्यासाठी वॉटर फिल्टर्स ही एक उत्तम संधी आहे. योग्यरित्या निवडलेला फिल्टर हा स्वच्छ पाण्याच्या समस्येवर उत्कृष्ट उपाय असेल, आरोग्यास सुधारेल आणि आपली दीर्घायुष्य वाढवेल.
पाण्याच्या कडकपणाचा आणि त्याच्या निर्मूलनाच्या पद्धतींचा अभ्यास
सीए 2 + आणि एमजी 2 + आयनच्या उपस्थितीमुळे पाण्याची कडकपणा आहे. नैसर्गिक पाण्यात त्यांची सामग्री जितके जास्त असेल (खडबडीत खडक आणि मातीतून जाणारे पाणी), त्याची कडकपणा जास्त असेल.
प्रमाणानुसार, पाण्याचे कडकपणा एक लिटर पाण्यात (मेक / एल) समाविष्ट असलेल्या सीए 2 + आणि एमजी 2 + आयनच्या मिलियक्वाइलेंट्सची बेरीज म्हणून दर्शविले जाते. कडकपणाचे एक मिलिएव्हिव्हॅलेंट 20.34 मिलीग्राम / सीए 2 + आयनच्या एल किंवा एमजी 2 + आयनच्या 12.16 मिलीग्राम / एलच्या सामग्रीशी संबंधित आहे.
म्हणून, समस्या सोडवताना आपण हे सूत्र वापरू शकता:
(मिमीोल - समतुल्य / एल),
कुठे मी - पाण्याचे कडक होणे किंवा पाण्याची कडकपणा दूर करण्यासाठी वापरल्या जाणार्\u200dया पदार्थाचा वस्तुमान; मिलीग्राम;
मा- या पदार्थाचे समकक्ष वस्तुमान, जी / मोल;
व्ही- पाण्याचे प्रमाण, एल
कठोरपणाने, सर्व नैसर्गिक पाण्याचे विभागले गेले आहेत मऊ(एकूण कडकपणा 2 मिमी / एल पेक्षा कमी) आणि कठीणकडकपणाची सरासरी डिग्री (2-10 मिमीोल / एल) आणि कडकपणाची उच्च डिग्री (10 मिमीोल / एलपेक्षा जास्त) सह.
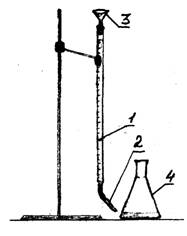
1 - ब्युरेट
2 - ड्रॉपर
3 - फनेल
आकृती 1 - प्रायोगिक सेटअप
कामगिरीचा अनुभव
तीन फ्लास्कमध्ये, मोठ्या प्रमाणात ग्रॅज्युएटेड सिलेंडरसह 100 मिली पाणी मोजा. पाण्याने प्रत्येक फ्लास्कमध्ये मिथाइल ऑरेंज इंडिकेटरचे 2-3 थेंब घाला. टायट्रेशन 0.1 एन. एक बुरेट वापरुन हायड्रोक्लोरिक acidसिड द्रावण. बुरेटमध्ये levelसिडची पातळी शून्य विभागात सेट करा. द्रावणाचा रंग पिवळ्या ते नारंगी-गुलाबी होईपर्यंत हायड्रोक्लोरिक acidसिड ड्रॉपच्या दिशेने घाला. टायट्रेशनमध्ये गेलेल्या acidसिडचे प्रमाण नोंदवा. टायटोरेशनची पुन्हा पुन्हा पुन्हा पुनरावृत्ती करा. टेबलमध्ये डेटा प्रविष्ट करा.
गणना सूत्रानुसार केली जाते:
![]() (मिमीोल - समतुल्य / एल),
(मिमीोल - समतुल्य / एल),
हायड्रोक्लोरिक acidसिडची सामान्य एकाग्रता कुठे आहे;
Vcp ( एचसीएल) - सरासरी खंड एचसीएल टायटोरेशनसाठी गेले;
पाणी - टायट्रेशनसाठी घेतलेल्या पाण्याचे प्रमाण.
आम्ही टेबलच्या रूपात तयार केलेला प्राप्त डेटा.
पाण्याचे नमुना
शीर्षक वापरले
फिल्टर केलेल्या पाण्याचे टायट्रेशन करण्यासाठी वापरले जाते
नळाचे पाणी - रसायन मंत्रिमंडळ
नळापासून पाणी - यष्टीचीत. विमानचालन
नळापासून पाणी - यष्टीचीत. ऑक्टोबर
स्तंभातून पाणी - पी. कोस्टल
नळापासून पाणी - यष्टीचीत. पोक्रोव्हस्की
विहिरीचे पाणी - यष्टीचीत. पोक्रोव्हस्की
नळापासून पाणी - यष्टीचीत. बेल्गोरोड
नळापासून पाणी - यष्टीचीत. सैनिक
सोडा पाणी "सुंदर"
शाळेच्या प्रयोगशाळेच्या परिस्थितीमध्ये आम्ही कडकपणासाठी विविध स्त्रोतांकडून घेतलेल्या पाण्याचा अभ्यास केला. कडकपणा निश्चित करण्यासाठी, मिथाइल नारिंगीच्या सूचकांच्या उपस्थितीत हायड्रोक्लोरिक acidसिडसह नैसर्गिक पाण्याचे टायट्रेशन वापरले गेले. पाण्याच्या नमुन्याची कार्बोनेट कडकपणा घरगुती फिल्टरद्वारे (एक्वाफोर वापरला जात होता) पास करण्यापूर्वी आणि नंतर निश्चित केला गेला.
कार्याचा परिणाम म्हणून, खालील निष्कर्ष घेण्यात आलेः
1) नोव्ही ओस्कॉल शहरातील पाणी कठीण आहे (डब्ल्यू \u003d 7-10.5). बरेच लोक खासगी क्षेत्रात राहतात आणि विहिरींचे पाणी वापरतात आणि हे पाणी फारच कठीण आहे.
2) पाणीपुरवठ्यात प्रवेश करणारे पाणी शुद्धीकरण आणि मऊ करणे (एल \u003d 6-7) च्या अधीन आहे, म्हणूनच, हे मध्यम कठोरता मानले जाऊ शकते (जीओएसटीच्या मते, पिण्याच्या पाण्याची एकूण कठोरता 7 मिमी / लीपेक्षा जास्त नसावी).
3) पाणी मऊ करण्याचा सर्वात सोपा मार्ग म्हणजे पारंपारिकपणे उकळणे.
)) प्रयोगांनी असे सिद्ध केले आहे की घरगुती फिल्टर देखील पाण्याने मऊ होतात. तर, विहिरीवरुन विहिरीच्या संशोधनासाठी घेतलेले पाणी. पोक्रोव्हस्की (कडकपणा 10.5 मिमीोल / एल), फिल्टरिंग नंतर, फक्त 2 मिमीोल / एलची कडकपणा होती, जो शारीरिक पद्धतीपेक्षा (3.5 मिमीएमएल / एल) अगदीच कमी आहे. अशाप्रकारे, आपले घर न सोडता अमर्यादित प्रमाणात शुद्ध पाणी मिळविण्याची उत्कृष्ट फिल्टर म्हणजे वॉटर फिल्टर्स.
संदर्भांची यादी
1.,. स्वच्छताविषयक संशोधनाच्या तंत्रासह व्यावहारिक स्वच्छताविषयक व्यायामासाठी मार्गदर्शक. - एम .: "औषध", 19
2. आणि. रासायनिक विश्लेषणाची मूलभूत तत्त्वे. विद्यार्थ्यांसाठी अभ्यास मार्गदर्शक. - एम .: "ज्ञानज्ञान", 1971. - 192 पी.
3 .. अजैविक रसायनशास्त्र: पाठ्यपुस्तक. तंत्रज्ञानासाठी विशेष विद्यापीठे. - एम .: उच्च. शाळा., 1989 .-- 432 पी.
4.,. आम्ही आमच्या शहराच्या वातावरणाचे परीक्षण करतोः 9-10 श्रेणी: शाळेची कार्यशाळा. - एम .: मानवता. एड व्हीलाडोस सेंटर, 2001. - 112 पी.
5. रसायनशास्त्र: रेफ्री. ed./V. श्रोएटर, के.-एच. लॉटेन्स्लेगर, एच. बिब्राक एट अल .: प्रति. त्यासह. एम.: रसायनशास्त्र, 1989. - प्रति. संपादन: जीडीआर, 1986.- 648 पी.
परिवर्तन साखळी
1. कॅल्शियम कार्बोनेट कॅल्शियम ऑक्साइड कॅल्शियम हायड्रॉक्साइड कॅल्शियम कार्बोनेट कॅल्शियम नायट्रेट.
2. मॅग्नेशियम सल्फेट मॅग्नेशियम नायट्रेट मॅग्नेशियम ऑक्साईड मॅग्नेशियम एसीटेट.
3. कॅल्शियम क्लोराईड कॅल्शियम सल्फेट कॅल्शियम सल्फाइड कॅल्शियम सल्फेट कॅल्शियम हायड्रॉक्साइड कॅल्शियम ऑक्साइड कॅल्शियम हायड्रोकार्बोनेट.
4. मॅग्नेशियम मॅग्नेशियम ऑक्साइड मॅग्नेशियम हायड्रॉक्साइड मॅग्नेशियम क्लोराईड मॅग्नेशियम हायड्रॉक्सोकार्बोनेट मॅग्नेशियम सल्फेट मॅग्नेशियम हायड्रॉक्साइड.
5. मॅग्नेशियम सल्फाइड मॅग्नेशियम ऑक्साईड ... मॅग्नेशियम हायड्रॉक्साईड ... मॅग्नेशियम नायट्रेट.
6. कॅल्शियम कॅल्शियम हायड्रॉक्साईड कॅल्शियम कार्बोनेट कॅल्शियम ऑक्साइड कॅल्शियम कार्बाइड कॅल्शियम हायड्रॉक्साइड कॅल्शियम हायड्रोकार्बोनेट.
सेटलमेंटची कामे
पातळी अ
1. पाण्यासह 13.7 ग्रॅम धातूचा संवाद 2.24 लिटर गॅस सोडतो (एन. ए.). धातू ओळखा. परिणामी द्रावणामध्ये सोडियम सल्फेटपेक्षा जास्त प्रमाणात मिसळल्यास कोणते द्रुतगती तयार होते आणि कोणत्या प्रमाणात तयार होते?
समाधान
एम आयए आणि आयआयए उपसमूह पाण्याबरोबर संवाद दरम्यान गॅस (एच 2) सोडला जातो.
समतुल्य कायद्यानुसार:
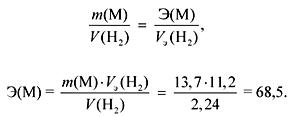
जर एम आयए उपसमूह झाला तर
ए आर (एम) \u003d ई व्हॅलेन्सी \u003d 68.5 (अशी धातू नाही).
जर एम IIa उपसमूह झाला तर
ए आर (एम) \u003d ई व्हॅलेन्सी \u003d 137 (बा)
बा + 2 एच 2 ओ \u003d बा (ओएच) 2 + एच 2,
बा (ओएच) 2 + ना 2 एसओ 4 \u003d बासो 4 + 2 एनओओएच,
(बासो 4) \u003d (बा (ओएच) 2) \u003d (बा) \u003d\u003d ०० मिली,
मी(बासो 4) \u003d एम\u003d 0.1 233 \u003d 23.3 ग्रॅम.
उत्तर. धातू - बा; मी(बासो 4) \u003d 23.3 ग्रॅम.
2. गाळाची निर्मिती पूर्ण करण्यासाठी कॅल्शियम बायकार्बोनेटच्या 10% द्रावण (घनता 1 ग्रॅम / सेमी 3) च्या 81 ग्रॅममध्ये 0.5 एम कॅल्शियम हायड्रॉक्साईड द्रावणाचे किती प्रमाण घालावे? गाळाचे वस्तुमान निश्चित करा.
उत्तर. 100 मिली सीए (ओएच) 2, सीएसीओ 3 च्या 10 ग्रॅम.
3. पोटॅशियम सल्फेट आणि क्रोमेट यांचे मिश्रण असलेल्या 23.3 ग्रॅम द्रावणास बेरियम क्लोराईडच्या अति प्रमाणात परिणाम झाला. वर्षाव फिल्टर करून, धुऊन, त्यानंतर हायड्रोक्लोरिक acidसिडचा एक अतिरिक्त पदार्थ जोडला गेला. पर्जन्यवृष्टीचा काही भाग विरघळला गेला, उर्वरित भाग फिल्टर, धुऊन वाळवला गेला. कोरडे झाल्यानंतर पर्जन्य वस्तुमान 23.3 ग्रॅम होते. प्रारंभिक मिश्रणाची रचना निश्चित करा.
उत्तर. के 2 एसओ 4 चे 17.4 ग्रॅम आणि के 2 सीआरओ 4 चे 5.9 ग्रॅम.
4. 1: 3: 4 (सूचीच्या क्रमानुसार) घटकांचे रवाळ प्रमाण असलेले कॅल्शियम, कॅल्शियम ऑक्साईड आणि कॅल्शियम कार्बाईड यांचे मिश्रण आहे. अशा प्रकारच्या 35 ग्रॅम मिश्रणासह किती प्रमाणात पाण्याचे रासायनिक संवाद होऊ शकते?
उत्तर. 17.568 मि.ली.
5. 100 डिग्री सेल्सियस पाण्यात स्ट्रॉन्टियम हायड्रॉक्साईडची विद्राव्यता 28 ग्रॅम आहे आणि 25 डिग्री सेल्सियस आहे - 100 ग्रॅम पाण्यात प्रति 1 ग्रॅम. 100 डिग्री सेल्सिअस तापमानात भरलेल्या स्ट्रॉन्शियम हायड्रॉक्साईडच्या 200 ग्रॅम सोल्यूशन 25 डिग्री सेल्सियस पर्यंत थंड केले गेले. द्रावण थंड झाल्यावर स्ट्राँटिअम हायड्रॉक्साईड ऑक्टिहायड्रेटचा द्रव्यमान शोधा.
उत्तर. 93.08 ग्रॅम सीआर (ओएच) 2 8 एच 2 ओ.
पातळी बी
1. गॅसची उत्क्रांती थांबविल्याशिवाय क्रिस्टलीय मॅग्नेशियम कार्बोनेटचा एक विशिष्ट घटक कॅलसिन केला गेला. नंतरचे फ्लशिंग बाटल्यांवर केंद्रित सल्फ्यूरिक acidसिड आणि चुन्याच्या पाण्याने गेले. पहिल्या फ्लास्कचे वस्तुमान 1.8 ग्रॅमने वाढले आणि दुसर्\u200dया 2 ग्रॅममध्ये वर्षाव कोसळला. प्रारंभिक क्रिस्टलीय हायड्रेट आणि त्याचे वस्तुमान यांचे संयोजन निर्धारित करा.
उत्तर. एमजीसीओ 3 5 एच 2 ओ पेंटायड्रेट; 3.48 ग्रॅम
2. 100 ग्रॅम वजनाच्या मिश्रणामध्ये कार्बोनेट, बायकार्बोनेट आणि कॅल्शियम नायट्रेटचे दाणे प्रमाण 1: 2: 3 (सूचीच्या क्रमाने) आहे. या मिश्रणाचे वायू विघटन उत्पादने 1200 डिग्री सेल्सिअस तपमानावर आणि सामान्य दाबाचे कोणते प्रमाण घेतील?
समाधान
मिश्रणाच्या घटकांच्या कुजलेल्या प्रतिक्रियेचे समीकरणः
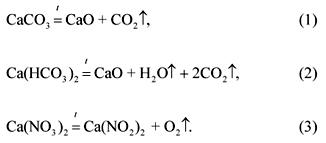
समस्येच्या स्थितीनुसारः
(CaCO 3): (Ca (HCO 3) 2): (Ca (NO 3) 2) \u003d 1: 2: 3.
चला (CaCO 3) \u003d x तीळ
नंतर (सीए (एचसीओ 3) 2) \u003d 2 x;
(सीए (क्रमांक 3) 2) \u003d 3 x;
100x + 162 2x +164 3x \u003d100,
x 0.109 मोल.
येथे पी \u003d 101.3 केपीए आणि टी वायूमय अवस्थेत \u003d 1200 डिग्री सेल्सियस ते सोडले जाते:
समीकरणानुसार सीओ 2 (1):
1 (सीओ 2) \u003d (सीसीओ 3) \u003d x \u003d 0.109 मोल;
समीकरणानुसार एच 2 ओ, सीओ 2 (2):
2 (एच 2 ओ) \u003d (सीए (एचसीओ 3) 2) \u003d 2 x \u003d 0.218 मोल,
2 (सीओ 2) \u003d 2 (सीए (एचसीओ 3) 2) \u003d 4 x \u003d 0.436 मोल;
हे 2 समीकरणानुसार (3):
3 (ओ 2) \u003d (सीए (नाही 3) 2) \u003d 3 x \u003d 0.327 मोल.
वायू विघटन उत्पादनांची एकूण संख्या:
0.109 + 0.218 + 0.436 + 0.327 \u003d 1.09 मोल (एन. ए.).
आदर्श वायूंच्या स्थितीच्या समीकरणातून आपल्याला खंड आढळतोः
पीव्ही = आरटी,
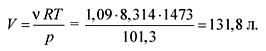
उत्तर. व्ही \u003d 131.8 लिटर
3. समान प्रमाणात डिव्हॅलेंट मेटल हायड्रॉक्साईड आणि कार्बोनेटचे मिश्रण केले गेले. घन अवशेषांचे वस्तुमान प्रारंभिक मिश्रणांच्या वस्तुमानापेक्षा 1.775 पट कमी होते. या अवशेषात 5% गंधकयुक्त आम्ल सोल्यूशनच्या मोठ्या प्रमाणात 10 वेळा जोडले गेले. परिणामी सोल्यूशनमध्ये पदार्थांच्या मोठ्या प्रमाणात अंश मोजा.
उत्तर. 6% एमजीएसओ 4.
4. जेव्हा पाण्याचे समान द्रव्यमान तुकड्यांसह हायड्रिड आणि नायट्राइडच्या दुभाजक धातूच्या मिश्रणाने उपचार केले जाते तेव्हा 2.658 च्या हायड्रोजन घनतेसह गॅस मिश्रण तयार होते. यौगिकांमध्ये समाविष्ट केलेली धातू सेट करा (गणना करताना संख्येस गोल करू नका!).
उत्तर. कॅल्शियम
5. 350 ग्रॅम वजनाच्या कॉपर (II) सल्फेटच्या 16% सोल्यूशनमध्ये 16 ग्रॅम मॅग्नेशियम प्लेट टाकली गेली. प्लेट काढून टाकल्यावर, द्रावणामध्ये असलेल्या लवणांचे द्रव्यमान समान नसले. प्लेटची वस्तुमान किती वेळा वाढवली?
उत्तर. 4.5 वेळा.
गुणवत्ता कार्ये
1. यापैकी कोणता पदार्थ मॅग्नेशियम हायड्रॉक्साईडशी संवाद साधेल: हायड्रोक्लोरिक acidसिड, नायट्रिक acidसिड, कार्बन डाय ऑक्साईड, सोडियम क्लोराईड, बेरियम हायड्रॉक्साइड, सल्फ्यूरिक acidसिड, तांबे (II) ऑक्साईड?
उत्तर. एचसीएल, एचएनओ 3, एच 2 एसओ 4.
2. लेबल नसलेल्या बाटल्यांमध्ये सोडा, खडू, जिप्सम आणि सोडियम सल्फेट असतात. पाणी आणि नायट्रिक acidसिडद्वारे या पदार्थांना कसे ओळखता येईल?
उत्तर.
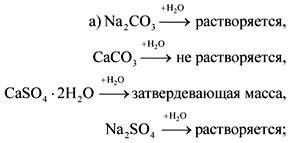
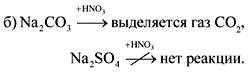
3. पदार्थ ए एक हलकी, जोरदार कठोर चांदी-पांढरा धातू आहे. ए बरोबर बी सारख्या वायू पदार्थांच्या संवादामध्ये कंपाऊंड सी तयार होतो जो पाण्यामध्ये विद्रव्य असतो आणि क्षारीय द्राव तयार करतो. सल्फ्यूरिक acidसिडद्वारे पदार्थावर प्रक्रिया करताना, मीठ तयार होते, त्यातील स्फटिकासारखे हायड्रेट फ्रॅक्चरसाठी फिक्सिव्ह ड्रेसिंगच्या वापरासाठी औषधात वापरले जाते. प्रतिक्रिया समीकरणे द्या.
उत्तर. ए सीए आहे; बी एच 2 आहे; सी सीएएच 2 आहे; क्रिस्टलीय हायड्रेट - सीएसओ 4 2 एच 2 ओ.
4. पदार्थ अ हा एक अल्कधर्मी द्राव तयार करण्यासाठी पाण्यात विरघळणारा ऑक्साईड आहे. या द्रावणामध्ये कंपाऊंड बी गंधरहित गॅस सी सह प्रतिक्रिया देते आणि पांढर्\u200dया अवस्थेत तयार होतो, जे हळूहळू विरघळते जेव्हा गॅस सी पुढे गेला तेव्हा प्रतिक्रिया समीकरण द्या आणि त्या पदार्थांची ओळख पटवा.
उत्तर. ए आहे काओ, बाओ; बी सीए (ओएच) 2, बा (ओएच) 2 आहे; सी सीओ 2 आहे.
5. पदार्थ अ, जो पृथ्वीच्या कवचातील सर्वात सामान्य खनिजांपैकी एक आहे, उच्च तापमानात दोन ऑक्साईड्समध्ये विघटित होतो, त्यापैकी एक जीवनाच्या प्रक्रियेत नेहमी तयार होतो. जेव्हा बी बी हा पदार्थ ग्रॅफाइटसह संवाद साधतो, गरम झाल्यावर, गॅस सी, जो उबदार-रक्ताळलेल्या प्राण्यांसाठी विषारी आहे, ज्वलनशील, रंगहीन आणि गंधहीन आहे. प्रतिक्रियेचे समीकरण द्या, पदार्थ ओळखा.
उत्तर. ए - सीएसीओ 3; बी सीओ 2 आहे; सी - सीओ.
पाण्याची कडकपणा आणि त्याचे निर्मूलन
रसायनशास्त्र सार
थीम:“पाण्याची कडकडीत”
कामाचा ठेकेदार:ग्रॅबिन पावेल.
योजना
परिचय 3
पाण्याची कडकपणा निश्चित करणे. 3
ताठर करण्याचे तंत्र 4
संदर्भ 6
परिचय
लेण्यांमध्ये, कॅव्हर्स सर्वात सुंदर चुनखडीच्या रचनेसह भेटतात - कमानी आणि स्टेलाग्मेट्सपासून वरच्या दिशेने लटकलेल्या स्टॅलेटाइट्स. रसायनशास्त्राच्या दृष्टिकोनातून, निसर्गाच्या या आश्चर्यकारक निर्मितींचा उदय हा भूगर्भातील कडकपणा आहे. आम्ही केवळ स्पेलोलॉजी आणि भूगर्भशास्त्रातच नाही तर सर्वसाधारणपणे, सर्वत्र - रसायनशास्त्र, तंत्रज्ञान आणि अगदी दैनंदिन जीवनात पाण्याची कठोरता ही संकल्पना पूर्ण करतो. आणि म्हणूनच, पाण्याची गुणवत्ता निश्चित करण्यासाठी ही संकल्पना खूप महत्वाची आहे.
पाण्याची कडकपणा निश्चित करणे
पाण्याची कडकपणा - कॅल्शियम आणि मॅग्नेशियम यौगिकांमध्ये विद्रव्य असलेल्या सामग्रीशी संबंधित पाण्याचे गुणधर्म (धुतले जाऊ नये, स्टीम बॉयलरमध्ये प्रमाणात प्रमाणात मोजण्यासाठी), हे पाण्यात कॅल्शियम आणि मॅग्नेशियम केटेशनची सामग्री दर्शविणारे एक पॅरामीटर आहे.
कडकपणा ही पाण्याचे विशेष गुणधर्म आहेत, जे मोठ्या प्रमाणात त्याचे ग्राहक गुण निर्धारित करतात आणि म्हणूनच त्यांचे महत्त्वपूर्ण आर्थिक मूल्य असते. कडक पाणी हीटिंग बॉयलर, बॅटरी इत्यादींच्या भिंतींवर प्रमाणात बनते, ज्यामुळे त्यांचे औष्णिक कार्यक्षमता लक्षणीय प्रमाणात कमी होते. हीटिंग पृष्ठभागावर अशी पातळ थर अजिबात निरुपद्रवी नसते, कारण कमी प्रमाणात थर्मल चालकता असलेल्या मैलच्या थरातून गरम होण्याचा कालावधी हळूहळू वाढत जातो, तळाशी वेगवान आणि वेगवान बाहेर जळत असते - प्रत्येक वेळी, धातू अधिक हळूहळू आणि हळूहळू प्रत्येक वेळी थंड होते, ते बर्\u200dयाच काळापर्यंत तापलेल्या स्थितीत राहते. सरतेशेवटी, असे होऊ शकते की जहाजातील तळाशी प्रतिकार होणार नाही आणि गळती होऊ देणार नाही. उद्योगात ही तथ्य अत्यंत धोकादायक आहे जिथे स्टीम बॉयलर अस्तित्वात आहेत.
कठोर पाणी धुण्यास योग्य नाही. वॉशिंग मशीनच्या हीटरवरील स्केल त्यांना व्यवस्थित ठेवते, साबणाने धुण्याचे गुणधर्म देखील खराब करते. सीए 2+ आणि एमजी 2+ कॅशन्स साबण फॅटी idsसिडस्सह प्रतिक्रिया देतात ज्यामुळे फिल्म आणि प्रिसिफिट तयार होणा sol्या थोड्या प्रमाणात विरघळणारे लवण तयार होतात, शेवटी वॉशिंगची गुणवत्ता कमी होते आणि डिटर्जंटचा वापर वाढतो, म्हणजे. कडक पाणी खराब होते
कठोरपणाचे दोन प्रकार आहेत: तात्पुरते आणि कायम. हा फरक कॅल्शियम आणि मॅग्नेशियमचे प्रतिरोध म्हणून समाधानात उपस्थित असलेल्या ionsनीऑनमुळे होतो.
तात्पुरते कडकपणा हायड्रोकार्बोनेट, किंवा बायकार्बोनेट ionsनाइन्स (एचसीओ 3 -) च्या सीए 2+, मिलीग्राम 2+ आणि फे 2+ सह पाण्यातील उपस्थितीशी संबंधित.
कायमस्वरुपी कडकपणा (किंवा नॉन-कार्बोनेट) द्रावणात सल्फेट, क्लोराईड, नायट्रेट आणि इतर ionsनिन उपस्थित असल्यास उद्भवू शकते, त्यातील कॅल्शियम आणि मॅग्नेशियम ग्लायकोकॉलेट चांगले विद्रव्य असतात आणि म्हणून ते सहजपणे काढले जाऊ शकत नाहीत. सोल्यूशनमधील सर्व कॅल्शियम आणि मॅग्नेशियम लवणांची एकूण सामग्री म्हणून एकूण कठोरता परिभाषित केली जाते.
पाण्यासाठी वेगवेगळ्या देशांचे त्यांचे कठोरपणाचे मानक आहेत. आपल्या देशात, पाण्याचे अशा प्रकारे कठोरतेने वर्गीकरण केले जाते:
कडकपणा सह मऊ पाणी m.० मे.क्यू / एल पेक्षा कमी,
मध्यम कडकपणा 3.0-6.0 एमईक्यू / एल
कठोर - 6.0 एमईक्यू / एमएल पेक्षा जास्त.
ताठरपणा दूर करण्याच्या पद्धती.
तात्पुरत्या कठोरतेपासून मुक्त होण्यासाठी आपल्याला फक्त पाणी उकळणे आवश्यक आहे. उकळत्या पाण्यात, बायकार्बोनेट आयन कॅशनवर प्रतिक्रिया देतात आणि त्यांच्याबरोबर अगदी खराब विरघळणारे कार्बोनेट ग्लायकोकॉलेट बनवतात, ज्यामुळे वर्षाव होतो.
सीए 2 + 2 एचसीओ 3 - \u003d सीसीओ 3 ↓ + एच 2 ओ + सीओ 2
लोह आयनसह, प्रतिक्रिया अधिक गुंतागुंतीची आहे कारण फॅको 3 पाण्यात अस्थिर पदार्थ आहे. ऑक्सिजनच्या उपस्थितीत, प्रतिक्रिया साखळीचे अंतिम उत्पादन फे (ओएच) 3 आहे, जे एक गडद लाल वर्षाव आहे. म्हणूनच, पाण्यात जास्त लोह असेल, स्केलवर रंग अधिक मजबूत होईल जो उकळत्या दरम्यान भिंती आणि पात्राच्या खाली ठेवला जातो.
सतत कठोरता लढणे कठीण आहे. एक पर्यायः हिमवर्षाव. आपल्याला हळूहळू पाणी गोठविणे आवश्यक आहे. जेव्हा सुरुवातीच्या प्रमाणात अंदाजे 10% द्रव शिल्लक असतो, तेव्हा गोठलेले पाणी काढून टाकावे आणि बर्फ परत पाण्यात बदलणे आवश्यक असते. कडकपणा तयार करणारे सर्व क्षार, गोठवलेल्या पाण्यातच राहतात.
अन्न हा एक मार्ग आहे - ऊर्धपातन, म्हणजेच त्यानंतरच्या संक्षेपणातून पाण्याचे बाष्पीभवन. ग्लायकोकॉलेट अस्थिर संयुगे असल्याने ते कायम राहतात आणि पाण्याचे बाष्पीभवन होते.
परंतु अतिशीत आणि ऊर्धपातन यासारख्या पद्धती केवळ थोड्या प्रमाणात पाणी मऊ करण्यासाठी योग्य आहेत. उद्योग टन सह व्यवहार करीत आहे. म्हणून, इतर पद्धती वापरल्या जातात. विशेष अभिकर्मकांच्या वापरावर आधारित सर्वात मोठ्या प्रमाणात वापरली जाणारी केशन एक्सचेंज पद्धत - केटेशन एक्सचेंजर्स, जे फिल्टरमध्ये लोड केले जातात आणि जेव्हा पाणी त्यांच्यामधून जाते तेव्हा कॅल्शियम आणि मॅग्नेशियम केटेशन्स सोडियम केशनसह बदला.
पाण्याच्या कठोरपणाच्या परिणामासह, रसायनशास्त्राच्या दृष्टिकोनातून, आपण अगदी सहजपणे लढा देऊ शकता. कमकुवत acidसिडच्या मीठावर मजबूत acidसिडचा प्रभाव असणे आवश्यक आहे. नंतरचे कोळशाचे स्थान घेते, जे अस्थिर होते, ते पाणी आणि कार्बन डाय ऑक्साईडमध्ये विघटित होते. स्केलच्या रचनामध्ये सिलिकेट्स, आणि सल्फेट्स आणि फॉस्फेट्स असू शकतात. परंतु आपण कार्बोनेट "कंकाल" नष्ट केल्यास, नंतर ही संयुगे पृष्ठभागावर राहणार नाहीत.
पाण्यात मिसळल्या जाणार्\u200dया अ\u200dॅडिपिक acidसिड आणि मॅरिकिक hyनहाइड्राइडचा वापर डेस्केलिंग एजंट म्हणूनही केला जातो. हे पदार्थ सल्फॅमिक acidसिडपेक्षा कमकुवत आहेत, म्हणूनच उकळणेदेखील डेसेकलिंगसाठी आवश्यक आहे.
संदर्भ:
श्पाउसस झेड. रसायनशास्त्र जगाकडे प्रवास - मॉस्को: शिक्षण, 1967. - 431 एस.
खरलंपोविच जी.डी. आणि इतर. अनेक बाजूंनी रसायनशास्त्र. - एम.: शिक्षण, 1992.-159 पी.
खोमचेन्को जी.पी. रसायनशास्त्र पाठ्यपुस्तक .:एम .: न्यू वेव्ह, 1996. - 304 पी.
तत्सम निबंध:
पॉलीएरिलेट्सच्या सौम्य सोल्यूशन्सच्या गुणधर्मांचा अभ्यास दोन घटक विचारात घेतल्यास: द्रावणामध्ये मॅक्रोमोलेक्यूलसची रूपांतर आणि सॉल्व्हेंट रेणूंचे विलीनीकरण करण्याच्या अभिमुख क्रम, ज्याचे समाधान थर्मोडायनामिक पॅरामीटर्स आणि सोल्यूशनच्या रचनेद्वारे केले गेले.
पहिल्या आणि दुसर्\u200dया टप्प्यातील मिश्रित क्रियेच्या समांतर-अचूक आयनाइट फिल्टरचा हेतू आणि रचना. काउंटरकंटंट आयनीकरण तंत्रज्ञानाचे वैशिष्ट्य. पाणी मऊ करण्याच्या सोडियम-कॅशनिक पद्धतीचे वर्णन. पाण्याचे पृथक्करण आणि पृथक्करण करण्याचे सिद्धांत.
केशन एक्सचेंजर्स आणि त्यांची मालमत्ता. सोडियम कॅटेशनेशनद्वारे पाणी मऊ करण्याची प्रक्रिया. हायड्रोजन-सोडियम-केशन एक्सचेंज वॉटर सॉफ्टनर. कॅल्क-कॅशनाइट आणि आंशिक कॅशनेशनच्या पद्धती. केशन एक्सचेंज इंस्टॉलेशन्सची केशन एक्सचेंज फिल्टर्स आणि सहायक डिव्हाइस.
फोम आणि सर्फेक्टंट्स म्हणजे काय. फेज इंटरफेसचे सर्वात महत्वाचे वैशिष्ट्य म्हणून पृष्ठभाग ताण. फोमिंगवर पाण्याच्या कडकपणाच्या प्रभावाच्या प्रायोगिक अभ्यासाच्या पद्धती आणि विविध प्रकारचे सर्फेक्टंटसाठी फोम स्थिरता.
पाण्याचे गुणधर्म आणि ते मऊ करण्याच्या पद्धती. उष्णता आणि उर्जा उद्योगात उपभोगलेल्या पाण्याच्या कठोरतेसाठी आवश्यकता. कॉम्प्लेक्सेट्रिक पद्धतीने पाण्याची कडकपणा निर्धारित करण्यासाठी सैद्धांतिक पाया आणि पद्धती. नमुना, अभिकर्मक, निर्धार.
लाकडाचे थर्मल विघटन करून कार्बनचे उत्पादन, कोळशाद्वारे वितळलेल्या पदार्थांचे आणि वायूंचे शोषण. अल्कलीबरोबर कार्बन डाय ऑक्साईडचा संवाद, कार्बन मोनोऑक्साइडचे उत्पादन आणि त्यातील गुणधर्मांचा अभ्यास. कार्बोनेट्स आणि बायकार्बोनेट्सच्या गुणधर्मांशी परिचित होणे.
पिण्याच्या पाण्याच्या गुणवत्तेचे सशर्त संकेतक. पाणी, तांबे आणि शिसे आयनमध्ये सेंद्रिय पदार्थांचे निर्धारण. पाण्याची कडकपणा दूर करण्याच्या पद्धती. पाणी स्वच्छ करण्याचे मार्ग. पोटॅशियम सल्फेटच्या कार्यरत सोल्यूशनची तयारी. आंशिक अतिशीत करून जल शुध्दीकरण.
कॅल्शियमचे रासायनिक गुणधर्म. ऑप्टिक्समध्ये शुद्ध कॅल्शियम कार्बोनेटचा वापर, धातुशास्त्रात चुनखडी - फ्लक्स म्हणून. कॅल्शियम सल्फेट क्रिस्टलीय हायड्रेट म्हणून जिप्सम. फॉस्फोरिक आणि atपेटाइट्सचे मुख्य घटक म्हणून फॉस्फरिक acidसिडचे कॅल्शियम मीठ.
कार्बन संयुगे विविधता, त्यांचे स्वरूप आणि अनुप्रयोग मध्ये वितरण. अलॉट्रॉपिक बदल भौतिक गुणधर्म आणि मुक्त कार्बन अणूची रचना. कार्बनचे रासायनिक गुणधर्म. कार्बोनेट्स आणि बायकार्बोनेट्स. डायमंड आणि ग्रेफाइटची रचना.
लिथोस्फीयरचे वैशिष्ट्य, पृथ्वीच्या क्रस्टमध्ये रासायनिक घटक आणि खनिजांची रचना. हायड्रोस्फीयरची रचना, रासायनिक रचना आणि कार्ये जीवशास्त्रामध्ये उद्भवणार्\u200dया सेंद्रिय पदार्थांच्या प्रकाशसंश्लेषणाची वैशिष्ट्ये. जैवरासायनिक प्रक्रियेचा अभ्यास.
गरम आणि घरगुती गरम पाण्याच्या यंत्रणेत उंच पाण्याची कडकपणा उष्णता हस्तांतरण प्रक्रियेवर नकारात्मक परिणाम करते, उर्जा वापर वाढवते. याव्यतिरिक्त, कठोर पिण्याचे पाणी मानवी आरोग्यास हानिकारक आहे. पाण्यासाठी विविध कारणांसाठी, मऊ करण्याच्या विविध पद्धती वापरल्या जातात.
वॉटर मऊनिंग ही पाण्यामधून कडकपणाचे क्षार काढून टाकण्याची प्रक्रिया आहे. पण पाण्याची कडकपणा म्हणजे काय आणि ते का दूर केले पाहिजे?
पाण्याची कडकपणा ही संकल्पना सहसा कॅल्शियम (सीए 2+) च्या कॅशनशी संबंधित असते आणि कमी प्रमाणात मॅग्नेशियम (एमजी 2+) असते. खरं तर, सर्व भावी कथांचा एक अंश किंवा दुसर्या कडकपणावर परिणाम होतो. ते ionsनऑनिसशी संवाद साधतात आणि कंपाऊंड बनवतात (कडकपणाचे क्षार) जे क्षीण होऊ शकतात.
लोह, मॅंगनीज आणि स्ट्रॉन्टीयमचे मीठदेखील येऊ शकते परंतु प्रत्यक्ष व्यवहारात या सर्व घटकांवर ताठरपणाचा इतका छोटासा प्रभाव पडतो की ते सहसा दुर्लक्ष करतात.
अ\u200dॅल्युमिनियम (अल 3+) आणि फेरिक आयर्न (फे 3+) देखील कडकपणावर परिणाम करतात, परंतु नैसर्गिक पाण्यात आढळणार्\u200dया पीएच पातळीवर, त्यांची विद्रव्यता आणि त्यानुसार, कठोरपणाचे "योगदान" नगण्य आहे. त्याचप्रमाणे बेरियमचा (बा 2+) क्षुल्लक प्रभाव विचारात घेतला जात नाही.
ताठरपणाचे प्रकार
पाण्याचे कडकपणाचे अनेक प्रकार आहेत. एकूण कठोरता कॅल्शियम आणि मॅग्नेशियम आयनच्या एकूण एकाग्रतेद्वारे निर्धारित केली जाते. हे कार्बोनेट (तात्पुरते) आणि नॉन-कार्बोनेट (कायम) कडकपणाचे योग आहे.
कार्बोनेट कडकपणा पाण्यामध्ये हायड्रोकार्बोनेट्स आणि कार्बोनेट्सच्या अस्तित्वामुळे आहे (पीएच\u003e 8.3 वर). तात्पुरती कडकपणा पाण्यात उपस्थिती आणि हायड्रोकार्बोनेटचे एमजी 2+ आणि फे 2+, किंवा बाइकार्बोनेट ionsनाइन्स (एचसीओ 3-) सह पाण्यातील उपस्थिती द्वारे दर्शविले जाते. उकळत्या पाण्यामुळे अशाप्रकारचे कठोरपणा जवळजवळ पूर्णपणे काढून टाकले जाते आणि म्हणूनच त्याला तात्पुरते कडकपणा म्हणतात. जेव्हा पाणी गरम होते, हायड्रोकार्बोनेट्स विघटन होते आणि कार्बनिक acidसिड तयार करतात आणि कॅल्शियम कार्बोनेट, मॅग्नेशियम हायड्रॉक्साईड आणि लोह घेतात.
नॉन-कार्बोनेट कठोरता कॅल्शियम आणि मॅग्नेशियम क्षारांच्या सशक्त idsसिडस् (सल्फ्यूरिक, नायट्रिक, हायड्रोक्लोरिक) च्या अस्तित्वामुळे आहे आणि उकळत्यामुळे काढून टाकली जात नाही, म्हणूनच त्याला सतत कठोरपणाचे नाव प्राप्त झाले आहे.
युनिट्स
जागतिक सराव मध्ये, कडकपणाची अनेक युनिट्स वापरली जातात, त्या सर्व विशिष्ट प्रकारे एकमेकांशी परस्परसंबंधित असतात.
कडकपणा एकक पाण्याचे कठोरता म्हणून घेतले जाते, 1 एल मध्ये सीए 2+ किंवा एमजी 2+ च्या 1 मिमीोल समतुल्य असते. कडकपणाचे एक युनिट (1 मिमीोल / एल) 20.04 मिलीग्राम / एल च्या समान कॅल्शियम आयन किंवा 12.15 मिलीग्राम / एल बरोबर मॅग्नेशियम आयनच्या सामग्रीशी संबंधित आहे. पाण्याची एकूण कठोरता (एच) सूत्राद्वारे मोजली जाऊ शकते:
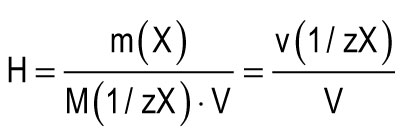
एम (एक्स) विरघळलेल्या पदार्थाचा द्रव्यमान, मिलीग्राम; एम (1 / झेडएक्स) हा पदार्थ, मिलीग्राम / एमएमओएल (जी / मोल) च्या समकक्ष भागांचा दाढीचा द्रव्यमान आहे; व्ही पाण्याचे खंड आहे, एल; एम (1 / झेडका 2+) \u003d 20.04 मिलीग्राम / मिमीोल; एम (1 / झेडएमजी 2+) \u003d 12.15 मिलीग्राम / मिमीोल.
याव्यतिरिक्त, जर्मन डिग्री (एडी, डीएच), फ्रेंच पदवी (एफएफ), अमेरिकन डिग्री, आणि पीपीएम सीएसीओ 3 यासारख्या ताठरपणाचे युनिट्स परदेशी देशांमध्ये मोठ्या प्रमाणात वापरले जातात.
या कठोरता युनिट्सचे गुणोत्तर टेबलमध्ये सादर केले आहे. 1
सारणी 1. ताठरपणाच्या वेगवेगळ्या युनिट्सचे प्रमाण
तर, एक जर्मन डिग्री पाण्यात 10 मिलीग्राम / डीएम 3 सीओ किंवा 17.86 मिलीग्राम / डीएम 3 सीसीओ 3 शी संबंधित आहे. एक फ्रेंच पदवी 10 मिलीग्राम / डीएम 3 सीसीओ 3 पाण्यात असते आणि अमेरिकन पदवी पाण्यात 1 मिलीग्राम / डीएम 3 सीसीओ 3 च्या समतुल्य असते.
पाण्याची कडकपणा मोठ्या प्रमाणात बदलते आणि तेथे बरेच प्रकारांचे वर्गीकरण आहेत. तर, जर्मनीमध्ये, जर्मन मानक संस्था (डीआयएन १ 19 364idity) च्या कठोरपणाचे मानके लागू केले जातात आणि यूएसएमध्ये - पर्यावरण संरक्षण एजन्सी (यूएसईपीए) ने 1986 मध्ये दत्तक वर्गीकरण (तक्ता 2).
सारणी 2. विविध प्रकारच्या कडकपणाचे वर्गीकरण
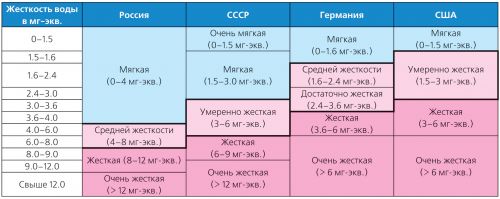
कोणते पाणी मऊ आहे
थोडक्यात, कमी खनिज पाण्यामध्ये, कॅल्शियम आयनमुळे कडकपणा दिसून येतो (जरी काही क्वचित प्रसंगी मॅग्नेशियम कडकपणा 50-60% पर्यंत पोहोचू शकतो). पाण्याच्या सामान्य खनिजतेच्या प्रमाणात वाढ झाल्यामुळे, कॅल्शियम आयन (सीए 2+) चे प्रमाण झपाट्याने कमी होते आणि क्वचितच 1 ग्रॅम / एलपेक्षा जास्त आहे. अत्यंत खनिजयुक्त पाण्यांमध्ये मॅग्नेशियम आयन (एमजी 2+) ची सामग्री अनेक ग्रॅम पर्यंत पोहोचू शकते, आणि मीठ तलावांमध्ये - दहा लिटर पाण्यात दहा ग्रॅम.
साधारणतया, भूजल कठोरपणापेक्षा पृष्ठभागावरील पाण्याची कडकपणा कमी असतो. पृष्ठभागाच्या पाण्याचा कडकपणा हा सहज लक्षात येणा season्या हंगामी चढउतारांच्या अधीन असतो, सामान्यत: हिवाळ्याच्या शेवटी आणि महापुराच्या दरम्यान सर्वात कमी किंमतीपर्यंत पोहोचतो जेव्हा मुबलक प्रमाणात पाऊस पडतो आणि पाण्याने वितळवले जाते. समुद्राच्या आणि समुद्राच्या पाण्यामध्ये खूपच कठोरता आहे (दहापट आणि शेकडो मेक / एल).
कडकपणाचे परिणाम
मॅग्नेशियम चवमुळे कठोर पिण्याचे पाणी कडू आहे आणि पाचन तंत्रावर नकारात्मक प्रभाव पडतो. जागतिक आरोग्य संघटनेच्या (डब्ल्यूएचओ) मानकांनुसार, पिण्याच्या पाण्याची इष्टतम कठोरता 1.0-2.0 एमईएक / एल आहे.
कडक पाण्यात खाद्य पदार्थ खराब पचतात कारण खाद्य प्रथिने असलेले कॅल्शियम केशन अघुलनशील संयुगे तयार करतात; त्यांचे पौष्टिक मूल्य कमी झाले आहे. कठोर पाण्याचा सतत वापर केल्यास मानवी शरीरात ग्लायकोकॉलेट (यूरोलिथियासिस) जमा होऊ शकते.
अशा पाण्यात चहा आणि कॉफी खराब प्रमाणात तयार केली जाते. घरगुती परिस्थितीत, कडकपणाच्या क्षारांपेक्षा जास्त प्रमाणात बॉयलर, टीपॉट्स, पाईप्समध्ये गरम होणारी पृष्ठभागांचे स्केलिंग होते, प्लंबिंग फिक्स्चरवर क्षारांचे साठा आणि त्यांचे अपयश, एखाद्या व्यक्तीच्या केस आणि त्वचेवर ठेव ठेवते ज्यामुळे त्यांच्या “कडकपणा” ची अप्रिय खळबळ निर्माण होते.
विविध उत्पादने तयार करण्यासाठी वापरल्या जाणार्\u200dया पाण्याचे कठोरपणाचे नियमन स्पष्टपणे केले जाते आणि ते ०.०-२.२ एमईक्यू / एल पातळीवर आहे.
कडक पाणी हीटिंग बॉयलर, बॅटरी इत्यादींच्या भिंतींवर मोजमाप करते, जे त्यांच्या औष्णिक कार्यक्षमतेस लक्षणीय करते, पाइपलाइनचे मुक्त विभाग कमी करते.
पाइपलाइन्स स्केल डिपॉझिटसह जास्त प्रमाणात वाढविले जातात जेणेकरून त्यांची उत्पादकता बर्\u200dयाच वेळा खाली येते. म्हणूनच, अशा प्रक्रियांमध्ये जिथे विशिष्ट मीठयुक्त पाण्याचा वापर करण्यास परवानगी आहे, त्याची कडकपणा अगदी अगदी कमी मूल्यांमध्ये मर्यादित आहे - 0.03-0.05 एमईक्यू / एल.
वॉशिंग मशीनच्या हीटरवरील स्केल त्यांना ऑर्डरच्या बाहेर ठेवते. धुताना, साबण किंवा लाँड्री डिटर्जंटच्या पृष्ठभागावर-सक्रिय पदार्थ (सर्फेक्टंट्स) शी संवाद साधताना, कडकपणाचे क्षार त्यांना बांधतात आणि जास्त खप घेण्याची आवश्यकता असते. काही तांत्रिक प्रक्रिया पार पाडताना कठोर पाण्याचा वापर केला जाऊ शकत नाही, उदाहरणार्थ, चित्रकला दरम्यान, इलेक्ट्रोकेमिस्ट्रीमध्ये आणि अशाच काही.
मीठ काढून टाकणे
वॉटर ट्रीटमेंटमधील पाण्यामधून सीए 2+ आणि एमजी 2+ साल्ट काढण्याच्या प्रक्रियेस वॉटर सॉफ्टनिंग असे म्हणतात.
पाण्यामधून कडकपणाचे क्षार दूरस्थपणे निवडण्याची पद्धत पद्धतींद्वारे केली जाऊ शकते:
- उष्णता उपचार;
- ऊर्धपातन;
- अभिकर्मक मऊ करणे;
- अतिशीत
- चुंबकीय प्रक्रिया;
- प्रचंड कंपनसंख्या असलेल्या (ध्वनिलहरी) प्रक्रिया;
- आयन एक्सचेंज
- उलट ऑस्मोसिस
जल उपचार पद्धती देखील ज्ञात आहेत (इलेक्ट्रोमॅग्नेटिक प्रभाव, पॉलीफॉस्फेट किंवा इतर "अँटी स्केल" ची जोड) काही काळ कडकपणाच्या क्षारांना "बांधून" ठेवण्यास परवानगी देतात, जे काही काळ स्केलच्या रूपात बाहेर पडण्यापासून प्रतिबंध करतात. तथापि, या पद्धती रासायनिकरित्या कडकपणाचे क्षार क्षीण करण्यास बेअसर करत नाहीत, त्या प्रत्यक्षात काढून टाकू नका आणि म्हणूनच औद्योगिक पाण्याच्या उपचारात मर्यादित वापर आढळला आहे.
औष्णिक नरम करणे
अशा प्रकारे, ते कॅल्शियम आणि मॅग्नेशियम बायकार्बोनेट्समुळे अस्थायी कडकपणापासून मुक्त होतात. उकळत्या पाण्यात, हायड्रोकार्बन विघटित होऊन मध्यम किंवा मूलभूत कार्बोनेटचा अवयव तयार करतात:
सीए (एचसीओ 3) 2 \u003d सीसीओ 3 ↓ + सीओ 2 + एच 2 ओ,
मिलीग्राम (एचसीओ 3) 2 \u003d एमजी 2 (ओएच) 2 सीओ 3 ↓ + 3 सीओ 2 + एच 2 ओ.
परिणामी, पाण्याची कडकपणा कमी झाली आहे. म्हणूनच बायकार्बोनेट कडकपणाला तात्पुरते असे म्हणतात.
लोह आयनसह, प्रतिक्रिया अधिक गुंतागुंतीची आहे कारण फॅको 3 पाण्यात अस्थिर पदार्थ आहे. ऑक्सिजनच्या उपस्थितीत, प्रतिक्रिया साखळीचे अंतिम उत्पादन फे (ओएच) 3 आहे, जे एक गडद लाल वर्षाव आहे. म्हणूनच, पाण्यात जास्त लोह असेल, स्केलवर रंग अधिक मजबूत होईल जो उकळत्या दरम्यान भिंती आणि पात्राच्या खाली ठेवला जातो.
अशा प्रकारे, दररोजच्या जीवनात पाणी उकळताना, त्याच्या अर्धवट नरम होण्याची प्रक्रिया एकाच वेळी उद्भवते.
आसवन
ऊर्धपातन एक पारंपारिक, प्रभावी आणि विश्वासार्ह पद्धत आहे जी उच्च खारटपणा आणि कडकपणासह उच्च खारट पाण्याचे शुद्धीकरण करण्याची उच्च पदवी प्रदान करते.
या पद्धतीने पाणी मिळविण्याचे सामान्य तत्व खालीलप्रमाणे आहेतः पूर्व-तयार पिण्याचे पाणी डिस्टिलरमध्ये प्रवेश करते, ज्यामध्ये तीन मुख्य घटक असतात: एक बाष्पीभवन, एक कंडेनसर आणि एक संग्रहकर्ता.
पाण्याने बाष्पीभवन उकळणे गरम केले जाते. पाण्याची वाफ कंडेन्सरमध्ये प्रवेश करते, जिथे ते द्रव असतात आणि डिस्टिलेटच्या रूपात कलेक्टरमध्ये प्रवेश करतात. स्त्रोत पाण्यात उपस्थित सर्व नॉन-अस्थिर अशुद्धी डिस्टिलरमध्येच राहिली आहेत.
शुद्ध पाणी मिळविण्यासाठी, डिस्टिलर्स वापरले जातात, जे हीटिंग, उत्पादकता आणि डिझाइन वैशिष्ट्यांच्या मार्गात एकमेकांपासून भिन्न असतात.
सिंगल डिस्टिलेशनची पद्धत एककमीय आहे, कारण जेव्हा याचा वापर केला जातो तेव्हा गरम आणि बाष्पीभवन (उष्मा प्रति 1 किलो सुमारे 3000 केजे), तसेच स्टीम कंडेन्सेशनसाठी (पाण्याचे 1 किलो स्टीम सुमारे 8 लीटर पाणी) जास्त ऊर्जा खर्च होते. म्हणून, कमी पाण्याच्या वापरासाठी एकाच आसवांचा वापर करण्यास सूचविले जाते - 10-20 एल / ता.
पारंपारिक आसवन पेक्षा अधिक कार्यक्षम आणि किफायतशीर उच्च-कार्यक्षमता मल्टि-कॉलम डिस्टिलर आहेत. परंतु ते अत्यंत महाग आहेत, त्याव्यतिरिक्त, त्यांच्यासाठी पाण्याचे पूर्व-उपचार खर्च जास्त आहे.
हे लक्षात घेण्यासारखे आहे की ऊर्धपातन करणारी पद्धत स्त्रोताच्या पाण्यातील सर्व विसर्जित लवण काढून टाकते.
अभिकर्मक अनुप्रयोग
पाणी मऊ करण्याची सोय-लिमिनिंग आणि सोडा-सोडियम पद्धतीद्वारे पाणी मऊ करते.
मर्यादित केल्यावर, हायड्रेटेड चुना सीए (ओएच) 2 सुमारे 10 च्या पीएचच्या द्रावणात जोडला जातो परिणामी, प्रतिक्रियांचे पुढे जाणे:
सीए (एचसीओ 3) 2 + सीए (ओएच) 2 \u003d 2 सीसीओ 3 + 2 एच 2 ओ,
मिलीग्राम (एचसीओ 3) 2 + 2 सीए (ओएच) 2 \u003d मिलीग्राम (ओएच) 2 + 2СaCO 3 + 2Н 2 ओ.
कडकपणा आणि क्षारीयतेमध्ये एकाच वेळी घट आवश्यक असताना, ही पद्धत उच्च कार्बोनेट आणि पाण्याच्या कमी कार्बनेट कडकपणासाठी वापरली जाते. अवशिष्ट कडकपणा नॉन-कार्बोनेट कडकपणापेक्षा 0.4-0.8 एमएक / एल जास्त आहे.
जेव्हा सोडा चुना जोडला जाईल तेव्हा स्लेक्ड लिंबू सीए (ओएच) 2 आणि सोडा ना 2 सीओ 3 सुमारे 10 पीएचमध्ये पाण्यात मिसळले जाते. परिणामी, खालील प्रतिक्रिया आढळतात:
सीए (एचसीओ 3) 2 + सीए (ओएच) 2 + ना 2 सीओ 3 \u003d 2 सीसीओ 3 + 2 नाओएच + एच 2 सीओ 3,
मिलीग्राम (एचसीओ 3) 2 + 2 एनओओएच \u003d एमजी (ओएच) 2 + 2 एनएएचसीओ 3.
प्रतिक्रियेच्या समीकरणांनुसार, पाण्यापासून गाळ तयार करणे आणि गाळ काढण्याच्या प्रक्रियेत, कडकपणाचे लवण काढले जातात. त्यांच्याबरोबर एकत्रित प्रदूषणासह कोलोइडल आणि निलंबित कण काढून टाकले जातात. सेंद्रिय गाळाचे तुकडे अंशतः गाळाच्या फ्लेक्सवर फोडल्या जातात.
सोडा लिमिनिंगसह, एचसीओ 3 आयनपेक्षा जास्त प्रमाणात, पाण्यातून कडकपणाचे क्षार काढून टाकण्याचे मोठे परिपूर्णता प्राप्त होते. तापमान 70-80 डिग्री सेल्सिअस पर्यंत वाढविणे आपल्याला उर्वरित कडकपणा 0.35-1.0 एमईक्यू / एल पर्यंत आणू देते. अभिकर्मकांच्या डोसमध्ये वाढ करून समान परिणाम प्राप्त केला जाऊ शकतो.
सोडा सोडा पद्धत
कार्बोनेटपेक्षा कार्बोनेट नसणे कठोर असल्यास सोडा जोडणे आवश्यक आहे. जर हे पॅरामीटर्स समान असतील तर सोडा घालणे अजिबात आवश्यक नाही.
अल्कलीच्या प्रतिक्रियेमध्ये कॅल्शियम आणि मॅग्नेशियमचे हायड्रोकार्बोनेट्स कॅल्शियम आणि मॅग्नेशियम, सोडा, पाणी आणि कार्बन डाय ऑक्साईडचे विद्रव्य विरघळणारे संयुगे तयार करतात:
सीए (एचसीओ 3) 2 + 2 एनओओएच \u003d सीसीओ 3 ↓ + ना 2 सीओ 3 + 2 एच 2 ओ,
मिलीग्राम (एचसीओ 3) 2 + 2 एनओओएच \u003d एमजी (ओएच) 2 ↓ + ना 2 सीओ 3 + एच 2 ओ + सीओ 2.
अल्कलीसह मॅग्नेशियम हायड्रोजन कार्बोनेटच्या प्रतिक्रियेच्या परिणामी तयार झालेले कार्बन डाय ऑक्साईड पुन्हा क्षारीबरोबर पुन्हा सोडा आणि पाणी तयार करण्यासाठी प्रतिक्रिया देते:
सीओ 2 + नाओएच \u003d ना 2 सीओ 3 + एच 2 ओ.
नॉन-कार्बोनेट कठोरता
सल्फेट आणि कॅल्शियम क्लोराईड कार्बनेट कडकपणा आणि अल्कलीच्या प्रतिक्रियेत तयार झालेल्या सोडावर प्रतिक्रिया देतात आणि सोडा जोडल्यामुळे कॅल्शियम कार्बोनेट तयार होते जे अल्कधर्मी परिस्थितीशी चिकटत नाही:
CaCl 2 + Na 2 CO 3 \u003d CaCO 3 2 + 2NaCl,
सीएसओ 4 + ना 2 सीओ 3 \u003d सीसीओ 3 ↓ + ना 2 एसओ 4.
मॅग्नेशियम सल्फेट आणि क्लोराईड अल्कलीवर प्रतिक्रिया देते आणि मॅग्नेशियम हायड्रॉक्साईड तयार होते:
MgSO 4 + 2NaOH \u003d Mg (OH) 2 ↓ + ना 2 एसओ 4,
MgCl 2 + 2NaOH \u003d Mg (OH) 2 ↓ + 2NaCl.
क्षार असलेल्या बायकार्बोनेटच्या प्रतिक्रियेत, सोडा तयार होतो, जो नंतर नॉन-कार्बोनेट कडकपणासह प्रतिक्रिया देतो, त्याची रक्कम कार्बोनेट (एलएफए) आणि नॉन-कार्बोनेट (एलएफए) कडकपणाच्या प्रमाणात सहसंबंधित असणे आवश्यक आहे:
- जर ते समान असतील तर सोडा वगळता येऊ शकतो;
- एलसी\u003e एलएनसी या अटीखाली सोडाचा एक जास्त भाग तयार होतो;
- एलसीडीच्या प्रमाणात< Жнк - недостаток соды и ее необходимо добавлять.
उपयोजन प्रक्रिया तलछटीच्या टाकी आणि स्प्लिफायर्समध्ये निलंबित गाळाच्या थरांसह केल्या जातात.
गाळाच्या टाक्या अकार्यक्षम असतात आणि त्यामध्ये मिळविलेल्या हायड्रॉक्साईड लगद्याची उच्च आर्द्रता 97-99% असते. म्हणून, ते सध्या व्यावहारिकरित्या वापरले जात नाहीत.
सराव मध्ये, निलंबित तलछट थर असलेल्या स्पष्टीकरणाच्या विविध आवृत्त्या वापरल्या जातात. त्यामध्ये, शुद्ध होण्याचे समाधान खाली वरून पुरवले जाते आणि गाळाच्या थरातून जाते. यामुळे जलशुद्धीकरणाचे गुणांक वाढते.
पिण्याचे पाणी तयार करताना रीएजेंट पद्धती वापरल्या जात नाहीत. त्यांच्या नंतर, पाण्याची तीव्र क्षारयुक्त प्रतिक्रिया आहे. म्हणून, अभिकर्मक यांत्रिक फिल्टरपासून शुध्दीकरणाच्या पहिल्या टप्प्यात ऊर्जा आणि उद्योगात मोठ्या प्रमाणात वापरले जातात. एकत्र काम करताना ते आपल्याला पाणी मऊ करण्याची परवानगी देतात, कोलोइड्ससह निलंबित घन काढून टाकतात आणि सेंद्रीय पदार्थांपासून अंशतः पाणी शुद्ध करतात.
अतिशीत
पाण्याच्या निरंतर कडकपणाचा सामना करण्यासाठी हिमवर्षाव यासारख्या पध्दतीचा वापर केला जातो. हे करण्यासाठी, आपल्याला हळूहळू पाणी गोठविणे आवश्यक आहे. जेव्हा अंदाजे 10% द्रव सुरुवातीच्या प्रमाणात राहतो, तेव्हा गोठलेले पाणी काढून टाकावे आणि बर्फ परत पाण्यात बदलणे आवश्यक आहे. कडकपणा तयार करणारे सर्व क्षार गोठलेल्या पाण्यात राहतात.
ऊर्धपातन सोबत, त्याच वेळी अत्यंत खारट पाण्याला पिण्यायोग्य गुणवत्तेसाठी खाली सोडण्याचा एक मार्ग आहे.
इतर पद्धती
इलेक्ट्रोडायलिसिस पद्धत थेट चालू नेटवर्कशी जोडलेल्या इलेक्ट्रोड्सकडे इलेक्ट्रोलाइट आयनच्या निर्देशित हालचालीच्या घटनेवर आधारित आहे. अशा प्रकारे, धातूचे आयन, जे पाण्याची कठोरता निर्धारित करतात, इलेक्ट्रोड्सवर अडकतात आणि पाण्याचे पृथक्करण करतात ज्यामुळे जल उपचार करण्याचे यंत्र सोडले जाते.
चुंबकीय आयनीकरण पद्धत आयनांच्या निर्देशित हालचालीची घटना देखील वापरते, परंतु आधीपासूनच चुंबकीय क्षेत्राच्या प्रभावाखाली असतात. पाण्यात आयनांची संख्या वाढविण्यासाठी, हे प्रामुख्याने आयनीकरण रेडिएशनसह विकिरण आहे.
पाण्याच्या चुंबकीय उपचारात विरोधी दिशानिर्देशांच्या चुंबकीय क्षेत्राच्या यंत्रणेद्वारे पाणी जात असते. याचा परिणाम म्हणून, विरघळलेल्या पदार्थाच्या हायड्रेशनची डिग्री कमी होते आणि त्यांचे मिश्रण मोठ्या कणांमध्ये घसरते ज्याचा वर्षाव होतो.
पाण्याचे प्रचंड कंपनसंख्या असलेल्या (ध्वनिलहरी) उपचारांमुळे गाळ तयार होण्याबरोबर विरघळलेल्या पदार्थाचे मोठे कण तयार होते.
आयन एक्सचेंज पद्धतीचा विचार करणे आणि लेखाच्या दुसर्\u200dया भागामध्ये उलट ऑस्मोसिस प्रक्रियेचा तपशीलवारपणे विचार करणे चांगले आहे, जे आपण पुढच्या अंकात आमच्या जर्नलमध्ये प्रकाशित करू.
