ភាពរឹងរបស់ទឹកនិងការលុបបំបាត់ចោល។ ភារកិច្ចនិងលំហាត់សម្រាប់លោហធាតុនៃក្រុមរងអាយ។ អេ
ទំព័រទី ១
ការលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នត្រូវបានអនុវត្តដោយទឹករំពុះ។ នៅពេលពុះកញ្ជ្រោលអ៊ីដ្រូកាបូនត្រូវបានបំផ្លាញហើយកាបូនដែលរលាយមិនល្អបង្កើតបានរបបទឹកភ្លៀង។ នៅពេលកាបូនសូដ្យូមកាបូអ៊ីដ្រាតកាល់ស្យូមត្រូវបានបញ្ចូលទៅក្នុងទឹកភាពរឹងសរុបរបស់ទឹកត្រូវបានយកចេញ។ ក្នុងករណីនេះភាពរឹងកាបូនត្រូវបានលុបចោលដោយកំបោរហើយភាពរឹងដែលមិនមែនជាកាបូនត្រូវបានលុបចោលដោយសូដា។
បន្ថែមពីលើការលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នកំបោរជួយបញ្ជូលសារធាតុម៉ាញ៉េស្យូមនិងដែកទាំងអស់ចេញពីទឹកនិងជំរុញឱ្យមានការប្រមូលផ្តុំជាតិកូឡាជែនសរីរាង្គនិងសរីរាង្គ។
បន្ទាប់ពីសម្អាតភាពមិនស្អាតលុបបំបាត់ភាពរឹងនិងការហៀរចេញជាបណ្តោះអាសន្នទឹកផាត់មុខត្រូវបានបញ្ចូលទៅក្នុងឧបករណ៍ផ្លាស់ប្តូរកំដៅ (២) កន្លែងដែលវាត្រូវបានកំដៅដល់ ៣៣៥ ឃេ។ បន្ទាប់ពីលាយទឹកបង្កើតនិងត្រឡប់ត្រូវបានបូមទៅតំបន់ទី ២ នៃឧបករណ៍ផ្លាស់ប្តូរកំដៅ (២) ដែលវាត្រូវបានកំដៅដល់ ៣៥៥ ខេហើយហូរចូល បណ្តាញកំដៅ។
ការបន្ទន់ត្រូវបានប្រើជាញឹកញាប់ដើម្បីលុបបំបាត់ភាពរឹងរបស់ទឹកជាបណ្តោះអាសន្នដែលត្រូវបានរចនាឡើងសម្រាប់ការខាតបង់ (បញ្ចូលឡើងវិញ) នៅក្នុងប្រព័ន្ធផ្គត់ផ្គង់ទឹកដែលកំពុងចរាចរនិងដើម្បីការពារការបំភាយរ៉ែនៃការផ្លាស់ប្តូរកំដៅនិងផ្ទៃត្រជាក់ដែលទាក់ទងនឹងទឹកដែលចរាចរ។ ក្នុងករណីជាច្រើនការបង្កើតទឹកគឺជាប្រភពសំខាន់នៃការប្រមូលផ្តុំអ៊ីយ៉ុងកាល់ស្យូមនិងជីវគីមីក្នុងទឹកដែលចរាចរដែលនៅក្នុងប្រព័ន្ធដែលមានមេគុណហួតខ្ពស់អាចរំខានដល់សមាសធាតុស្ថេរភាពនៃទឹកដែលកំពុងចរាចរ។
ការបន្ទន់ទឹកក្នុងគោលបំណងដើម្បីលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នត្រូវបានអនុវត្តដោយគីមីដោយណែនាំឱ្យប្រើឡើងវិញដែលត្រូវបានប្រើជាកំបោរស៊ុលហ្វារិចឬអាស៊ីតអ៊ីដ្រូក្លរីក។ វិធីសាស្ត្រគីមីសម្រេចបាននូវការបន្ទន់ទឹករាក់ ៗ ។ ចំពោះការបន្ទន់កំរិតខ្ពស់ជាងនេះវិធីសាស្រ្តនៃការផ្លាស់ប្តូរស៊ីអ៊ីតត្រូវបានប្រើដែលខ្លឹមសារគឺប្រើសមត្ថភាពនៃសារធាតុមួយចំនួនដើម្បីផ្លាស់ប្តូរសូចនាករនៃសូដ្យូមដែលមាននៅក្នុងពួកគេសំរាប់ដកស្រង់អំបិលរឹងនៅក្នុងទឹក។
សូដា Caustic ត្រូវបានប្រើនៅក្នុងរោងចក្រថាមពលកំដៅដើម្បីលុបបំបាត់ភាពរឹងនៃទឹកជាបណ្តោះអាសន្នសម្រាប់ការបង្កើតឡើងវិញនៃតម្រងអាណូទីសដែលត្រូវបានប្រើនៅក្នុងរុក្ខជាតិសម្រាប់ការបន្សុទ្ធជាតិគីមីនៃទឹក។
សូដា Caustic ត្រូវបានគេប្រើនៅក្នុងរោងចក្រថាមពលកំដៅដើម្បីលុបបំបាត់ភាពរឹងនៃទឹកបណ្តោះអាសន្ននិងបង្កើតឡើងវិញនូវតម្រង anionic ដែលត្រូវបានប្រើនៅក្នុងរុក្ខជាតិដែលមានជាតិគីមី។
ស្រដៀងគ្នានេះដែរបរិមាណ Ca (OH) 2 ដែលត្រូវការដើម្បីលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នក៏គួរតែត្រូវបានគេគណនាផងដែរ។
ហេតុអ្វីបានជាដើម្បីលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នដោយសារតែអំបិលម៉ាញ៉េស្យូមតម្រូវឱ្យមានកំបោរច្រើនជាងការលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នដោយសារអំបិលកាល់ស្យូម។
ដូច្ន្រះដើម្របីបញ្ចូលប្រពន្ធ័ផ្គត់ផ្គង់ទឹកសា្អ្រតដ្រលបិទជិត (ការបន្សុតដោយមិនគិតគូរ) ការធ្វើឱ្រយទឹកនិងការលុបបំបាត់ភាពរឹងបណ្តោះអាសន្នគួរត្រូវបានអនុវត្ត។
សេចក្តីផ្តើមនៃការប្រើសារធាតុអាល់កាឡាំងក្នុងបរិមាណតិចតួចបង្កើនប្រសិទ្ធភាពនៃការព្យាបាលម៉ាញ៉េទិចនៃទឹកទោះបីជាសេចក្តីណែនាំអំពីសារធាតុគីមីអាល់កាឡាំងជាឧទាហរណ៍កំបោរក្នុងបរិមាណមិនលើសពី ១០ - ២០ ភាគរយនៃសារធាតុចាំបាច់ដើម្បីលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្ននេះបើយោងតាមការសិក្សាដែលអនុវត្តនៅ KhIEI ក្នុងឆ្នាំ ១៩៥៩ កាត់បន្ថយការកកើតទ្រង់ទ្រាយ ៨ ទៅ ១០ ដង។
ក្នុងករណីនេះទឹកដែលមានឆ្អឹង ៦ ដែលបណ្តាលមកពីប៊ីកាបូណាតត្រូវបានលុបចោល។ ដូច្នេះភាពរឹងនេះត្រូវបានគេហៅថាបណ្តោះអាសន្នឬប៊ីការិបូណាត។ ដូច្នេះដើម្បីលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្នវាគ្រប់គ្រាន់ហើយក្នុងការដាំទឹក។
អំបិលរឹងរឹងឧទាហរណ៍ CaCl, CaSO4 ជាដើមមិនត្រូវបានយកចេញពីទឹកនៅពេលកម្តៅ។ ពួកវាត្រូវបានទឹកភ្លៀងក្នុងកំឡុងពេលហួតទឹកបង្កើតនៅលើជញ្ជាំងនៃបរិធានពិបាកដកចេញខ្នាតក្រាស់។ ទឹករឹងអាចត្រូវបានប្រើតែក្នុងករណីដែលលក្ខខណ្ឌនៃការប្រើប្រាស់របស់វាមិនបណ្តាលឱ្យមានការធ្លាក់ទឹកភ្លៀងរឹងឧទាហរណ៍នៅក្នុងទូទឹកកកដែលទឹកត្រជាក់មិនកម្តៅរហូតដល់សីតុណ្ហភាពដែលជួយលុបបំបាត់ភាពរឹងជាបណ្តោះអាសន្ន។ នៅក្នុងរុក្ខជាតិឡចំហាយដែលជាកន្លែងដែលទឹកមិនត្រឹមតែត្រូវបានកំដៅប៉ុណ្ណោះទេប៉ុន្តែវាក៏ហួតផងដែរមិនត្រឹមតែបណ្តោះអាសន្នប៉ុណ្ណោះទេប៉ុន្តែក៏រឹងរឹងដែលមិនអាចទទួលយកបាន។ ដូច្នេះទឹកសម្រាប់ពួកគេត្រូវបានបន្សុតជាមុនពីអំបិលកាល់ស្យូមនិងម៉ាញ៉េស្យូមដោយវិធីសាស្ត្រគីមីនៅក្នុងរុក្ខជាតិពិសេស។
ស្ថាប័នអប់រំក្រុង
“ អនុវិទ្យាល័យលេខ ១
ជាមួយនឹងការសិក្សាស៊ីជម្រៅលើមុខវិជ្ជានីមួយៗ
អាស័យដ្ឋាន៖ តំបន់ Belgorod,
ការធ្វើតេស្តភាពរឹងរបស់ទឹក
និងវិធីដើម្បីលុបបំបាត់វា
mOU ថ្នាក់ ១១ "A" មធ្យម
អនុវិទ្យាល័យលេខ ១
ជាមួយនឹងការសិក្សាស៊ីជម្រៅ
របស់របរនីមួយៗ
អាស័យដ្ឋាន៖ តំបន់ Belgorod,
អ្នកប្រឹក្សាវិទ្យាសាស្ត្រ៖
គ្រូគីមីវិទ្យា
អនុវិទ្យាល័យលេខ ១
ជាមួយនឹងការសិក្សាស៊ីជម្រៅ
របស់របរនីមួយៗ
novy Oskol, តំបន់ Belgorod
អាស័យដ្ឋាន៖ តំបន់ Belgorod,
novy Oskol,
novy Oskol
១. សេចក្តីផ្តើម……………………………………………………………… .៣
2. ភាពរឹងរបស់ទឹកនិងវិធីសាស្រ្តសំរាប់ការលុបបំបាត់របស់វា…………………………… .៤
·ហេតុអ្វីបានជាទឹកក្លាយជារឹង ..................................................................... ៤
value តម្លៃនៃភាពរឹងរបស់ទឹកនៅក្នុងជីវិតរបស់មនុស្ស ...................................... ៤
·វិធីបំបាត់ភាពរឹង………………………………………… ៥
៣. ការសិក្សាអំពីភាពរឹងរបស់ទឹកនិងវិធីសាស្រ្តក្នុងការលុបបំបាត់ចោល…………… ៨
4. សេចក្តីសន្និដ្ឋាននិងការសន្និដ្ឋាន
5. បញ្ជីឯកសារយោង
សេចក្តីផ្តើម
អ្នកដែលសិក្សាផ្នែកវិទ្យាសាស្ត្រតែមិនអនុវត្តទេ
ស្រដៀងនឹងអ្នកដែលភ្ជួររាស់តែមិនសាបព្រោះ។
សាឌី
នៅក្នុងទសវត្សទី ៨០ នៃសតវត្សរ៍ទី ២០ សៀវភៅរបស់លោក Paul Chappius Bragg បានលេចចេញពីការលើកកម្ពស់របៀបរស់នៅដែលមានសុខភាពល្អ។ ហើយទោះបីជាអ្នកសិក្សាជាច្រើនគិតថាគំនិតរបស់គាត់មានភាពចម្រូងចម្រាសក៏ដោយសៀវភៅរបស់ Paul Bragg សមនឹងទទួលបានការយកចិត្តទុកដាក់។ ផ្នែកមួយនៃសៀវភៅរបស់គាត់ (ការពិសោធន៍ដំបូងរបស់ខ្ញុំជាមួយនឹងភាពរឹង) គឺផ្តោតទៅលើបញ្ហានៃភាពរឹងរបស់ទឹកដែលអ្នកនិពន្ធនៅក្នុងសៀវភៅកត់ត្រារបស់គាត់ពិពណ៌នាអំពីជំងឺរបស់ជីតាគាត់ដែលបានស្លាប់ដោយសារការពិតដែលថាសរសៃឈាមរបស់គាត់បានក្លាយទៅជាស្អុយរលួយពីទឹករឹងហើយស្ត្រីដែលរស់នៅក្នុងផ្នែករបស់ពួកគេ ( ស្ត្រីអកុសលត្រូវបានគេហៅថាស្ត្រីដុំថ្មដោយសារតែរាងកាយរបស់នាងត្រូវបានចិញ្ចឹមដោយអំបិលយ៉ាងច្រើន) ។ ស្ត្រីនោះគឺជាម្នាក់ក្នុងចំនោមជនរងគ្រោះជាច្រើននៃទឹករឹង។ សរីរាង្គមិនល្អបានបរាជ័យក្នុងការដោះស្រាយជាមួយនឹងដំណើរការនៃសារធាតុអសរីរាង្គដ៏ច្រើនដែលមាននៅក្នុងទឹកបែបនេះហើយពួកគេបានចាប់ផ្តើមកកកុញយ៉ាងសកម្មនៅក្នុងខ្លួនរបស់នាង។
សមាសធាតុកាល់ស្យូម precipitate នៅក្នុងខ្លួនរបស់យើងនៅក្នុងសំណុំបែបបទនៃគ្រួសតំរងនោមនិងប្លោកនោម។
សព្វថ្ងៃនេះការព្យាបាលទឹកមិនមែនជាអ្វីដែលគួរអោយចង់ធ្វើនោះទេប៉ុន្តែវាជាតម្រូវការចាំបាច់មួយ។ ការពិតគឺថាបាតុភូតមិនល្អដូចជាស្នាមរលាកក្លិនភាគីទីបីក្លិនក៏ដូចជាវត្តមាននៃរបបទឹកភ្លៀងពពកមិនត្រឹមតែបង្កឱ្យមានការរអាក់រអួលប៉ុណ្ណោះទេប៉ុន្តែថែមទាំងបង្កឱ្យមានជំងឺជាច្រើនផងដែរ។ ទឹកដែលមានគុណភាពទាបជំរុញឱ្យមានការដាក់អំបិលបង្កើនល្បឿនដំណើរការចាស់នៃរាងកាយនិងក្លាយជាបុព្វហេតុនៃការផ្លាស់ប្តូរជំងឺជាច្រើនទៅដំណាក់កាលរ៉ាំរ៉ៃ។ លើសពីនេះទៀតក្លរីនមានផ្ទុកនូវសារធាតុមួយចំនួនដែលអាចបង្កឱ្យមានជំងឺមហារីក។ ប៉ុន្តែទឹកគឺជាមូលដ្ឋានគ្រឹះនៃជីវិតទាំងអស់ហើយមិនមែនសារពាង្គកាយមានជីវិតតែមួយទេដែលអាចធ្វើដោយគ្មានទឹក។ ឧទាហរណ៍មនុស្សម្នាក់មានទឹកនៅ 60-65% ។ ដូច្នេះទឹកស្អាតគឺចាំបាច់សម្រាប់មនុស្សគ្រប់គ្នា។ ជាអកុសលទឹកធម្មជាតិនៅសម័យរបស់យើងគឺមិនសមស្របសម្រាប់ការប្រើប្រាស់ដោយគ្មានការព្យាបាលបឋមដែលត្រូវបានបញ្ជាក់ដោយការវិភាគទឹកផ្សេងៗគ្នា។ អ្នករាល់គ្នាដឹងថាស្ថានីយ៍ចម្រោះទឹកដែលត្រូវបានគេអះអាងថាអនុវត្តការបន្សុតទឹកត្រូវបានគេជួសជុលជាយូរមកហើយហើយប្រព័ន្ធផ្គត់ផ្គង់ទឹកតាមរយៈការបញ្ជូនទឹកទៅផ្ទះរបស់យើងតម្រូវឱ្យមានការជំនួស។
គោលបំណងនៃការងាររបស់យើងគឺសិក្សាពីកម្រិតនៃភាពរឹងរបស់ទឹកនៅឯស្រុកកំណើតរបស់យើង។
ភាពរឹងនៃទឹកនិងវិធីសាស្រ្តសម្រាប់ការលុបបំបាត់របស់វា
ហេតុអ្វីបានជាទឹកពិបាក
កាល់ស្យូមនិងសមាសធាតុរបស់វាគឺចាំបាច់ណាស់សម្រាប់រាងកាយ៖ បន្ទាប់ពីបានទាំងអស់វាគឺមកពីកាល់ស្យូម orthophosphate Ca3 (P04) ២ ដែលឆ្អឹងនិងធ្មេញរបស់មនុស្សនិងសត្វត្រូវបានផ្សំឡើង។ ពួកវាត្រូវបានបង្កើតឡើងពីសមាសធាតុកាល់ស្យូមរលាយដែលផ្ទុកឈាមពាសពេញរាងកាយ។ សូមអរគុណដល់សារជាតិកាល់ស្យូម Ca2 + ដែលឈាមអាចកកអាចបង្កើតជាកំណកឈាមនិងស្ទះនិងបញ្ឈប់ការហូរឈាម។
សមាសធាតុកាល់ស្យូមមិនត្រឹមតែមានប្រយោជន៍ប៉ុណ្ណោះទេប៉ុន្តែវាក៏មានគ្រោះថ្នាក់ខ្លាំងផងដែរ - ឧទាហរណ៍នៅពេលពួកគេផ្តល់ភាពរឹងដល់ទឹកធម្មតា។ នៅក្នុងជីវិតប្រចាំថ្ងៃពាក្យ "រឹង" នៅ glance ដំបូងអាចត្រូវបានអនុវត្តតែចំពោះអ្នកដែលនៅសេសសល់: កៅអីឧទ្យានឬលាមកនៅក្នុងផ្ទះបាយអាចរឹងមាំ។ ទោះយ៉ាងណាទឹកក៏ពិបាកដែរ។
ប្រភពសំខាន់នៃអំបិលម៉ាញ៉េស្យូមនិងកាល់ស្យូមដែលចូលក្នុងទឹកគឺជាប្រាក់បញ្ញើនៃថ្មកំបោរហ្គីបស៊ូមនិងដូម៉ូម៉ីតដែលត្រូវបានបំផ្លាញដោយទឹកធម្មជាតិ។
នៅក្នុងទឹកមានជាតិប្រៃទាបភាគច្រើននៃអ៊ីយ៉ុងកាល់ស្យូម។ ជាមួយនឹងការកើនឡើងនូវកំរិតរ៉ែរ៉ែមាតិកាអ៊ីយ៉ុងកាល់ស្យូមមានការថយចុះយ៉ាងឆាប់រហ័សនិងកម្រលើសពី 1 ក្រាម / លីត្រ។ ខ្លឹមសារនៃអ៊ីយ៉ុងម៉ាញ៉េស្យូមនៅក្នុងទឹករ៉ែរ៉ែអាចឡើងដល់ច្រើនក្រាមហើយក្នុងទឹកអំបិលជាច្រើនរាប់សិបក្រាម។
ភាពរឹងរបស់ទឹក - ការរួមបញ្ចូលគ្នានៃលក្ខណៈគីមីនិងរូបធាតុរបស់ទឹកទាក់ទងនឹងខ្លឹមសារនៃអំបិលរលាយនៃលោហធាតុអាល់កាឡាំងដែលមាននៅក្នុងវាភាគច្រើនគឺកាល់ស្យូមនិងម៉ាញ៉េស្យូម។ ទឹកដែលមានមាតិកាខ្ពស់នៃអំបិលបែបនេះត្រូវបានគេហៅថាទឹករឹងដែលមានមាតិកាទាប - ទន់។ មានភាពរឹងជាបណ្តោះអាសន្ន (កាបោន) ដែលបង្កើតឡើងដោយអ៊ីដ្រូកាបូននិងរឹងជាអចិន្ត្រៃយ៍ (មិនមែនកាបូន) ដែលបណ្តាលមកពីវត្តមាននៃអំបិលផ្សេងៗ ភាពរឹងជាបណ្តោះអាសន្នគឺដោយសារតែវត្តមាននៃកាល់ស្យូមនិងម៉ាញ៉េស្យូមប៊ីកាកាបូណាត (Ca (HCO3) 2; Mg (HCO3) 2) នៅក្នុងទឹក។ ភាពរឹងនៃទឹកថេរគឺដោយសារតែវត្តមាននៅក្នុងទឹកស៊ុលហ្វាតស៊ីលនិងអេលក្លរ (CaSO4, CaCl2, MgSO4, MgCl2) ។
តម្លៃនៃភាពរឹងរបស់ទឹកនៅក្នុងជីវិតមនុស្ស
ភាពរឹងរបស់ទឹកគឺជាផលបូកនៃអ៊ីយ៉ុងកាល់ស្យូម Ca2 + និងម៉ាញ៉េស្យូម Mg2 + រលាយក្នុងទឹក។
អ៊ីយ៉ុងកាល់ស្យូមនិងម៉ាញ៉េស្យូមមិនបង្កគ្រោះថ្នាក់ច្រើនដល់សារពាង្គកាយមានជីវិតទេប៉ុន្តែវត្តមានរបស់វានៅក្នុងទឹកក្នុងបរិមាណដ៏ច្រើនគឺមិនចង់បានទេព្រោះទឹកបែបនេះមិនសមស្របសម្រាប់តម្រូវការគ្រួសារ។
នៅក្នុងទឹករឹងការប្រើប្រាស់សាប៊ូនិងម្សៅកើនឡើងនៅពេលលាងសម្លៀកបំពាក់សាច់និងបន្លែត្រូវបានរំលាយយឺត ៗ ហើយចលនារបស់ក្រពះត្រូវបានកាត់បន្ថយ។ ទឹករឹងមិនសមស្របសម្រាប់ប្រព័ន្ធផ្គត់ផ្គង់ទឹកនិងឧបករណ៍កំដៅទឹក។
ភាពរឹងត្រូវបានវាស់គិតជាមីលីក្រាមស្មើនឹងមួយលីត្រ (ម។ ល។ / លី) ។ ស្តង់ដារឧស្សាហកម្មសម្រាប់តម្លៃរឹងដែលអាចអនុញ្ញាតបានអាស្រ័យលើប្រភេទឧបករណ៍ដែលបានប្រើ។ ជាធម្មតាទឹករឹងដែលមានកំរាស់ ១ \u200b\u200bម៉ែត / អិលឬច្រើនជាងនេះត្រូវបានគិត។
ភាពរឹងគឺជាបញ្ហាគុណភាពទឹកទូទៅបំផុត។ ដើមឡើយពាក្យថាទឹករឹងត្រូវបានអនុវត្តទៅលើទឹកដែលពិបាកលាងសំអាត។
ទឹករឹងនៅពេលលាងសម្អាតស្ងួតស្បែកពពុះត្រូវបានបង្កើតឡើងមិនសូវល្អនៅក្នុងវានៅពេលប្រើសាប៊ូ។ ការប្រើប្រាស់ទឹករឹងបណ្តាលឱ្យដីល្បាប់ (ជញ្ជីង) លេចឡើងនៅលើជញ្ជាំងឡចំហាយក្នុងបំពង់ជាដើមក្នុងពេលដំណាលគ្នាការប្រើប្រាស់ទឹកទន់ពេកអាចបណ្តាលឱ្យច្រេះបំពង់ពីព្រោះក្នុងករណីនេះមិនមានទ្រនាប់អាស៊ីត - មូលដ្ឋានដែលផ្តល់ដោយអ៊ីដ្រូកាបូន។ (បណ្តោះអាសន្ន) ភាពរឹង។ ការប្រើប្រាស់ទឹករឹងឬទន់ជាធម្មតាមិនបង្កគ្រោះថ្នាក់ដល់សុខភាពនោះទេទោះបីជាមានភស្តុតាងបង្ហាញថាភាពរឹងខ្ពស់រួមចំណែកដល់ការបង្កើតគ្រួសក្នុងទឹកនោមនិងទាបក៏ដោយ - តិចតួចបង្កើនហានិភ័យនៃជំងឺបេះដូងនិងសរសៃឈាម។
ភាពរឹងនៃទឹកធម្មជាតិអាចមានលក្ខណៈខុសគ្នាច្រើនហើយមិនមានស្ថេរភាពពេញមួយឆ្នាំ។ ភាពរឹងកើនឡើងដោយសារតែការហួតទឹកមានការថយចុះនៅរដូវវស្សាក៏ដូចជាកំឡុងពេលរលាយនៃព្រិលនិងទឹកកក។
វិធីដើម្បីលុបបំបាត់ភាពរឹង
សម្គាល់ ជារួម ភាពរឹងដែលត្រូវបានផ្សំឡើងដោយ បណ្តោះអាសន្ន និង ថេរ.
រំពុះ។
បណ្តោះអាសន្ន ភាពរឹង (ការចោលឬកាបូន) គឺដោយសារតែវត្តមានរបស់ Ca (HCO3) 2 និង Mg (HCO3) 2 ក្នុង bicarbonates នៅក្នុងទឹក។ កាបូនរឹងងាយដកចេញ ទឹកក្តៅក្នុងនោះ Ca2 + និង Mg2 + ត្រូវបានយកចេញដើម្បីបង្កើតជារបបទឹកភ្លៀងដែលមិនអាចរលាយបាន៖
Ca (HCO3) 2 CaCO3 ↓ + CO2 + H2O
អ៊ីជីអ៊ីយ៉ុង precipitate នៅក្នុងសំណុំបែបបទនៃកាបូនមូលដ្ឋានឬនៅក្នុងសំណុំបែបបទនៃម៉ាញេស្យូមអ៊ីដ្រូសែន (នៅ pH\u003e 10.3) ។
2Mg2 + + OH) 2CO3 ↓ + CO2 + H2O
(អូអ៊ី - អ៊ីយ៉ុងត្រូវបានបង្កើតឡើងដោយសារតែអន្តរកម្មនៃអ៊ីយ៉ុងជាមួយទឹក: និងលំនឹងវិលទៅខាងស្តាំនៅពេលកម្តៅ) ។
ដើម្បីកាត់បន្ថយភាពរឹងកាបូន វិធីសាស្ត្រកំណត់ នៅក្នុងនោះទឹកដែលត្រូវបានព្យាបាលត្រូវបានណែនាំ កំបោរCa (OH) ២ ។ ប្រតិកម្មដែលកើតឡើងជាមួយនឹងការណែនាំកំបោរអាចត្រូវបានសរសេរជាទម្រង់ម៉ូលេគុល៖
Ca (HCO3) 2 + Ca (OH) 2 → 2CaCO3 ↓ + H2O
Mg (НСО3) 2 + Са (ОН) 2 → Mg (ОН) 2 ↓ + 2СаСО3 + Н2О
ភាពរឹងថេរ (មិនអាចរក្សាទុកបានឬមិនមានជាតិកាបូន) ត្រូវបានថែរក្សានៅពេលដែលទឹកពុះព្រោះភាពរឹងថេរគឺដោយសារវត្តមាននៅក្នុងទឹកស៊ុលហ្វាតក្លរីតនិងអំបិលផ្សេងទៀតនៃ Ca និង Mg ។ បរិមាណវាស្មើនឹងការផ្តោតអារម្មណ៍របស់ Ca2 + និង Mg2 + ions ដកពេលវេលារឹង។ ជាធម្មតាត្រូវបានប្រើដើម្បីកាត់បន្ថយភាពរឹងកាបូន។ calcined សូដា (Na2CO3)៖
MgSO4 + Na2CO3 → MgCO3 ↓ + Na2SO4
ខណៈពេលបន្ថែម កំបោរ និង សូដា អ្នកអាចកម្ចាត់ភាពរឹងកាបូននិងមិនមែនកាបូណាត។ វិធីសាស្រ្តកំបោរ - សូដា).
ភាពរឹងទាំងអស់ត្រូវបានលុបចោលសូម្បីតែជាមួយ ការណែនាំ ផូស្វ័រសូដ្យូម, tetraborate សូដ្យូម ដោយហេតុថាអ័រភូថូស្យូសមិនរលាយតិចជាងកាបូនការប្រើប្រាស់របស់ពួកគេក្នុងការបន្ទន់ទឹកកាន់តែងាយស្រួល:
3CaSO4 + 2Na3PO4 → Ca3 (PO4) 2 ↓ + 3Na2SO4
វិធីទំនើបនៃការបន្ទន់ទឹកគឺផ្អែកលើ ដោយប្រើ ជ័រផ្លាស់ប្តូរអ៊ីយ៉ុង - ឧបករណ៍ផ្លាស់ប្តូរអ៊ីយ៉ុង (ការផ្លាស់ប្តូរស៊ីអរនិងការផ្លាស់ប្តូរអ៊ីយូន) ។ ឧបករណ៍ផ្លាស់ប្តូរស៊ីម៉ងត៍គឺជាជ័រផ្លាស់ប្តូរអ៊ីយ៉ុងសំយោគ - aluminosilicates ឧទាហរណ៍៖
សមាសភាពរបស់ពួកគេអាចត្រូវបានបង្ហាញដោយលក្ខខណ្ឌដោយរូបមន្តទូទៅ Na2R ដែល Na + គឺជាអាណាឡូកចល័តខ្ពស់និង R - គឺជាភាគល្អិតនៃការផ្លាស់ប្តូរស៊ីអេសដែលផ្ទុកបន្ទុកអវិជ្ជមាន។
នៅពេលដែលទឹករឹងហូរឆ្លងកាត់ស្រទាប់នៃជ័រផ្លាស់ប្តូរស៊ីដ្យូមត្រូវបានផ្លាស់ប្តូរយោងទៅតាមប្រតិកម្ម
Ca2 + + Na2R → 2Na + + CaR
Mg2 + + + Na2R → 2Na + + MgR
ដូច្នេះ Ca2 + និង Mg2 + ions ឆ្លងកាត់ពីដំណោះស្រាយទៅជ័រប្តូរស៊ីម៉ងត៍។ ដើម្បីស្តារជ័រប្តូរស៊ីម៉ងត៍វាត្រូវបានទឹកនាំទៅជាមួយដំណោះស្រាយប្រមូលផ្តុំរបស់ណុក។
CaR + 2NaCl → CaCl2 + Na2R
បន្ទាប់ពីលាងសម្អាតជ័រប្តូរស៊ីម៉ងត៍អាចត្រូវបានប្រើម្តងទៀតដើម្បីយកភាពរឹងចេញពីទឹក។
បញ្ច្រាស osmosis។ វិធីសាស្រ្តគឺផ្អែកលើការឆ្លងកាត់ទឹកតាមរយៈភ្នាស semipermeable (ជាធម្មតាប៉ូលីម៉ីត) ។ រួមគ្នាជាមួយអំបិលរឹងអំបិលផ្សេងទៀតភាគច្រើនក៏ត្រូវបានយកចេញដែរ។ ប្រសិទ្ធភាពនៃការសម្អាតអាចឈានដល់ ៩៩,៩% ។ វិធីសាស្រ្តនេះបានរកឃើញការប្រើប្រាស់ដ៏អស្ចារ្យបំផុតនៅក្នុងប្រព័ន្ធប្រព្រឹត្តិកម្មទឹកស្អាតក្នុងស្រុក។ ក្នុងនាមជាគុណវិបត្តិនៃវិធីសាស្រ្តនេះតម្រូវការសម្រាប់ការរៀបចំបឋមនៃទឹកដែលផ្គត់ផ្គង់ដល់ភ្នាសបញ្ច្រាសគួរត្រូវបានកត់សម្គាល់។
អេឡិចត្រូលីត វាត្រូវបានផ្អែកលើការយកអំបិលចេញពីទឹកដោយសកម្មភាពនៃវាលអគ្គីសនី។ ការយកចេញនូវអ៊ីយ៉ុងនៃសារធាតុរំលាយកើតឡើងដោយសារតែភ្នាសពិសេស។ ដូចគ្នានឹងបច្ចេកវិទ្យាបូសបញ្ច្រាសអំបិលផ្សេងទៀតត្រូវបានយកចេញបន្ថែមលើអ៊ីយ៉ុងរឹង។
វិធីសាស្ត្រកំដៅ។ ដោយផ្អែកលើកំដៅទឹកលុបបំបាត់តែភាពរឹង (កាបូន) បណ្តោះអាសន្នប៉ុណ្ណោះ។ ស្វែងរកកម្មវិធីនៅក្នុងជីវិតប្រចាំថ្ងៃ។ នៅក្នុងឧស្សាហកម្មវាត្រូវបានប្រើឧទាហរណ៍នៅរោងចក្រថាមពលកំដៅ។
ការបន្ទន់ខ្លួនឡើងវិញ។ វិធីសាស្រ្តគឺផ្អែកលើការបន្ថែមសូដាឬកំបោររំអិលទៅក្នុងទឹក។ ក្នុងករណីនេះអំបិលកាល់ស្យូមនិងម៉ាញេស្យូមឆ្លងកាត់សមាសធាតុរលាយហើយជាលទ្ធផលទឹកភ្លៀង។ វិធីសាស្រ្តនេះត្រូវបានគេរាប់បញ្ចូលក្នុងការប្រើប្រាស់ទឹកខ្ពស់ពីព្រោះវាត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងដំណោះស្រាយនៃបញ្ហាជាក់លាក់មួយចំនួនដូចជាការច្រោះយកកាកសំណល់បរិមាណដូសត្រឹមត្រូវនៃការរំreក។
ការដកស្រង់ចេញ។ វិធីសាស្រ្តគឺផ្អែកលើការប្រើប្រាស់នៃការផ្ទុកក្រឡាចត្រង្គអ៊ីយ៉ុងផ្លាស់ប្តូរ (ភាគច្រើនជាជ័រផ្លាស់ប្តូរអ៊ីយ៉ុង) ។ ទំនក់ទំនងបែបនេះនៅពេលមានទំនាក់ទំនងជាមួយទឹកស្រូបយកអំបិលដករឹង (កាល់ស្យូមនិងម៉ាញ៉េស្យូម) ។ នៅក្នុងការផ្លាស់ប្តូរអាស្រ័យលើទម្រង់អ៊ីយ៉ុងផ្តល់ឱ្យនូវសូដ្យូមអ៊ីដ្រូសែនឬអ៊ីដ្រូសែនអ៊ីដ្រូសែន។ វិធីសាស្រ្តទាំងនេះត្រូវបានគេហៅថារៀង Na-cation និង H-cation ។ តាមក្បួនមួយភាពរឹងនៃទឹកមានការថយចុះជាមួយនឹងការដាក់ស៊ីដ្យូមតែមួយដំណាក់កាលដល់ ០.០៥-០,១ ម៉ែល / អ៊ីដោយមានពីរដំណាក់កាល - ដល់ ០,០១ ម៉ែល / អិល។
ល្អបំផុត ដើម្បីលុបបំបាត់ភាពរឹងទូទៅនៃទឹកសូដ្យូម otophosphate គឺ Na3PO4: 3Ca (HCO3) 2 + 2Na3PO4 → Ca3 (PO4) 2 ↓ + 6NaHCO3 3MgSO4 + 2Na3PO4 → Mg3 (PO4) 2 ↓ + 3Na2SO4 មានជាតិកាល់ស្យូមនិងរលាយច្រើន។ ការបន្ទន់ទឹកល្អប្រសើរ។ នៅក្នុងឧស្សាហកម្មការប្រើប្រាស់តម្រងផ្លាស់ប្តូរអ៊ីយ៉ុងកាល់ស្យូមនិងអ៊ីយ៉ុងម៉ាញ៉េស្យូមត្រូវបានជំនួសដោយអ៊ីយ៉ុងសូដ្យូមនិងប៉ូតាស្យូមដើម្បីផលិតទឹកទន់។ ការបន្ទន់ទឹកជាក់លាក់មួយកើតឡើងនៅក្នុងតម្រងគ្រួសារសម្រាប់ទឹកផឹក។ ទឹកត្រងផ្តល់នូវទំហំតិច។ ទឹកអាចត្រូវបានបន្សុតទាំងស្រុងដោយការច្របាច់បញ្ចូលគ្នា។
សព្វថ្ងៃនេះល្អណាស់ ចម្រោះទឹក ដែលត្រូវបានតំឡើងនៅក្នុងអាផាតមិនដោយគ្មានបញ្ហាហើយដើរតួជាឧបករណ៍ដ៏ល្អសម្រាប់ការព្យាបាលទឹកដែលមានគុណភាពខ្ពស់។ ប្រហែលជាសព្វថ្ងៃនេះមនុស្សជាច្រើនចូលចិត្តទិញទឹកបរិសុទ្ធដបនៅក្នុងផ្សារទំនើប។ ជម្រើសទឹកបែបនេះពិតជាធំធេងណាស់ប៉ុន្តែតើអាចធានាបាននូវគុណភាពរបស់វា ១០០ ភាគរយដែរឬទេ? ប្រហែលជាមិនមែនទេ! នោះហើយជាមូលហេតុដែលការបន្សុតទឹកដោយមានជំនួយពីតម្រងដែលបានរចនាឡើងពិសេសសម្រាប់ការបន្សុតគឺជាដំណោះស្រាយដ៏ប្រសើរបំផុតសម្រាប់មនុស្សសម័យទំនើបដែលយកចិត្តទុកដាក់លើសុខភាពនិងសុខភាពរបស់សាច់ញាតិរបស់គាត់។ ប្រព័ន្ធបន្សុតទឹកមានភាពចម្រុះណាស់។ តាមក្បួនមួយពួកគេខុសគ្នា: ការសម្តែងប៉ារ៉ាម៉ែត្រមួយចំនួនកំរិតនៃការបន្សុតទឹកក៏ដូចជាការរចនា។ ត្រងទឹកស្អាតឥតខ្ចោះនិងធ្វើឱ្យវាសមស្របសម្រាប់ផឹកកាត់បន្ថយមាតិកាអាលុយមីញ៉ូមដែកម៉ង់ហ្គាណែសក្លរីននីត្រាតគ្រប់ប្រភេទនៅក្នុងវា។ លើសពីនេះទៀតតម្រងសម្រាប់ការបន្សុតទឹកជួយលុបបំបាត់ក្លិនមិនល្អរសជាតិក៏ដូចជាកម្ចាត់មេរោគនិងបាក់តេរីដែលមាននៅក្នុងទឹក។ ទឹកដែលត្រូវបានបន្សុតតាមរយៈប្រព័ន្ធបែបនេះប្រែជាមិនសូវរឹងមាំទោះយ៉ាងណាវាមិនបាត់បង់សារធាតុដែលមានប្រយោជន៍សម្រាប់រាងកាយមនុស្សទេ។ ឧបករណ៍ចម្រោះទឹកគឺជាឱកាសដ៏ប្រសើរបំផុតក្នុងការទទួលបានទឹកបរិសុទ្ធក្នុងបរិមាណគ្មានកំណត់ដោយមិនចាំបាច់ចាកចេញពីផ្ទះរបស់អ្នក។ ចម្រោះដែលបានជ្រើសរើសត្រឹមត្រូវនឹងជាដំណោះស្រាយដ៏ប្រសើរមួយចំពោះបញ្ហាទឹកស្អាតធ្វើអោយប្រសើរឡើងនូវសុខភាពនិងពន្យារអាយុយឺនយូរ។
ការសិក្សាអំពីភាពរឹងរបស់ទឹកនិងវិធីសាស្រ្តក្នុងការលុបបំបាត់
ភាពរឹងរបស់ទឹកគឺដោយសារតែវត្តមានរបស់ Ca2 + និង Mg2 + ions ។ មាតិការបស់ពួកវាខ្ពស់ជាងនៅក្នុងទឹកធម្មជាតិ (ទឹកឆ្លងកាត់ថ្មនិងដី) ។
បរិមាណភាពរឹងនៃទឹកត្រូវបានបង្ហាញជាផលបូកនៃមីលីខននៃ Ca2 + និង Mg2 + ions ដែលមាននៅក្នុងទឹកមួយលីត្រ (meq / l) ។ ភាពរឹងមួយមីលីក្រាមទាក់ទងនឹងខ្លឹមសារ ២០.០៤ មីលីក្រាម / អិលនៃ Ca2 + ions ឬ ១២,១៦ មីលីក្រាម / អិលនៃ Mg2 + ions ។
ដូច្នេះនៅពេលដោះស្រាយបញ្ហាអ្នកអាចប្រើរូបមន្ត៖
(mmol - equiv / l),
កន្លែងណា m ម៉ាស់សារធាតុដែលធ្វើឱ្យទឹករឹងឬប្រើដើម្បីលុបបំបាត់ភាពរឹងរបស់ទឹក, មីលីក្រាម;
ម៉ា- ម៉ាស់សមមូលនៃសារធាតុនេះ, ក្រាម / ម៉ូល;
វី- បរិមាណទឹកលីត្រ
ដោយភាពរឹងទឹកធម្មជាតិទាំងអស់ត្រូវបានបែងចែក ទន់(រឹងរឹងតិចជាង ២ ម។ ល / លី) និង ស្វិតស្វាញជាមួយនឹងកំរិតមធ្យមនៃភាពរឹង (២-១០ ម។ ល។ ម / លី) និងកំរិតខ្ពស់នៃភាពរឹង (ច្រើនជាង ១០ ម។ ម។ ល / លី) ។
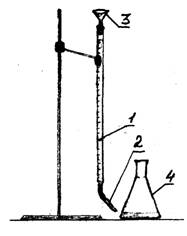
1 - burette
២ - ដំណក់ទឹក
៣ - ចីវលោ
រូបភាពទី 1 - ការរៀបចំពិសោធន៍
បទពិសោធន៍ការសម្តែង
នៅក្នុងឡចំហាយចំនួនបីវាស់ជាមួយស៊ីឡាំងដែលបានបញ្ចប់ការសិក្សាធំមួយទឹក ១០០ មីលីលីត្រ។ បន្ថែមសឺរាុំងពណ៌ទឹកក្រូចមេតាន ២-៣ ដំណក់ចូលក្នុងខ្ទះនីមួយៗជាមួយទឹក។ ការផ្តល់តម្លៃត្រូវបានអនុវត្ត 0,1 អិន។ ដំណោះស្រាយអាស៊ីតអ៊ីដ្រូក្លរីកដោយប្រើប៊ីតថេត។ កំណត់កំរិតអាសុីតនៅក្នុងប៊ែរតេសទៅសូន្យចែក។ ចាក់ទឹកអាស៊ីត hydrochloric តាមទ្រនិចនាឡិការហូតដល់ពណ៌នៃដំណោះស្រាយផ្លាស់ប្តូរពីពណ៌លឿងទៅពណ៌ទឹកក្រូច - ផ្កាឈូក។ កត់ត្រាបរិមាណអាសុីតដែលបានចូលជាធរណី។ ធ្វើម្តងទៀតនូវការផ្តល់ប្រាក់កម្ចីម្តងទៀតពីរដង។ បញ្ចូលទិន្នន័យក្នុងតារាង។
ការគណនាត្រូវបានអនុវត្តតាមរូបមន្ត:
![]() (mmol - equiv / l),
(mmol - equiv / l),
ដែលជាកន្លែងដែលកំហាប់ធម្មតានៃទឹកអាស៊ីត hydrochloric;
Vcp ( ហ។ ស) - បរិមាណមធ្យម អេសអិល បានទៅសម្រាប់ការរាប់ជា;
ទឹកហូរ - បរិមាណទឹកដែលយកសម្រាប់ភាគលាភ។
ទិន្នន័យដែលទទួលបានយើងបានរចនាជាទម្រង់តារាង។
គំរូទឹក
ប្រើសម្រាប់ការធ្វើកម្មនីតិសម្បទា
ត្រូវបានប្រើសម្រាប់ការរាប់ជាទឹកនៃចម្រោះ
ទឹកម៉ាស៊ីន - គណៈរដ្ឋមន្ត្រីគីមី
ទឹកពីម៉ាស៊ីន - ស្ត។ អាកាសចរណ៍
ទឹកពីម៉ាស៊ីន - ស្ត។ តុលា
ទឹកពីជួរឈរ - ទំ។ ឆ្នេរសមុទ្រ
ទឹកពីម៉ាស៊ីន - ស្ត។ Pokrovsky
ទឹកពីអណ្តូង - ស្ត។ Pokrovsky
ទឹកពីម៉ាស៊ីន - ស្ត។ Belgorod
ទឹកពីម៉ាស៊ីន - ស្ត។ ទាហាន
ទឹកសូដា "ស្រស់ស្អាត"
នៅក្នុងល័ក្ខខ័ណ្ឌនៃមន្ទីរពិសោធន៍សាលាយើងបានធ្វើការសិក្សាអំពីទឹកដែលបានមកពីប្រភពផ្សេងៗគ្នាសម្រាប់ភាពរឹង។ ដើម្បីកំណត់ភាពរឹងការរាប់មួយភាគនៃទឹកធម្មជាតិជាមួយទឹកអាស៊ីដ hydrochloric នៅក្នុងវត្តមាននៃសូចនាករនៃពណ៌ទឹកក្រូចមេតានត្រូវបានគេប្រើ។ ភាពរឹងនៃកាបោននៃគំរូទឹកត្រូវបានកំណត់មុននិងក្រោយពេលឆ្លងកាត់វាតាមតម្រងគ្រួសារ (អាកហ្វ័រត្រូវបានប្រើ) ។
ជាលទ្ធផលនៃការងារការសន្និដ្ឋានដូចខាងក្រោមត្រូវបានធ្វើឡើង:
១) ទឹកនៅទីក្រុង Novy Oskol គឺរឹង (W \u003d 7-10.5) ។ មនុស្សជាច្រើនរស់នៅក្នុងវិស័យឯកជនហើយប្រើប្រាស់ទឹកពីអណ្តូងហើយទឹកនេះពិបាកណាស់។
2) ទឹកដែលចូលក្នុងការផ្គត់ផ្គង់ទឹកត្រូវបានទទួលរងនូវការបន្សុតនិងការបន្ទន់ (L \u003d 6-7) ដូច្នេះវាអាចត្រូវបានគេចាត់ទុកថារឹងមធ្យម (យោងទៅតាម GOST ភាពរឹងនៃទឹកផឹកមិនគួរលើសពី 7 មីល្លីល / លីត្រទេ) ។
៣) មធ្យោបាយធ្វើនៅផ្ទះងាយបំផុតក្នុងការបន្ទន់ទឹកគឺមានលក្ខណៈពុះ។
៤) ការពិសោធន៍បានបង្ហាញថាចម្រោះទឹកក្នុងគ្រួសារក៏ធ្វើឱ្យទឹកទន់ឥតខ្ចោះដែរ។ ដូច្នេះទឹកយកសម្រាប់ស្រាវជ្រាវពីអណ្តូងនៅលើដំបៅ។ Pokrovsky (រឹង 10,5 mmol / L) បន្ទាប់ពីការច្រោះមានភាពរឹងត្រឹមតែ 2 មិល្លីលីត្រ / អិលដែលវាទាបជាងបទដ្ឋានសរីរវិទ្យា (3,5 មីល្លីលីត្រ / អិល) ។ ដូច្នេះចម្រោះទឹកគឺជាឱកាសដ៏ល្អបំផុតដើម្បីទទួលបានទឹកបរិសុទ្ធក្នុងបរិមាណមិនកំណត់ដោយមិនចាំបាច់ចាកចេញពីផ្ទះរបស់អ្នក។
បញ្ជីឯកសារយោង
១, ។ ការណែនាំអំពីលំហាត់អនាម័យជាក់ស្តែងជាមួយបច្ចេកទេសស្រាវជ្រាវអនាម័យ។ - អិមៈ“ វេជ្ជសាស្ត្រ” អាយុ ១៩ ឆ្នាំ។
2. និង។ មូលដ្ឋានគ្រឹះនៃការវិភាគគីមី។ សៀវភៅណែនាំការសិក្សាសម្រាប់និស្សិត។ - អិមៈ "ការត្រាស់ដឹង" ឆ្នាំ ១៩៧១ - ១៩២ ទំ។
៣ .. គីមីវិទ្យាសរីរាង្គ៖ សៀវភៅសិក្សា។ សម្រាប់អ្នកបច្ចេកទេស ពិសេស សាកលវិទ្យាល័យ។ - អិមៈខ្ពស់ជាង។ សាលាឆ្នាំ ១៩៨៩ ។— ៤៣២ ទំ។
៤, ។ យើងតាមដានបរិដ្ឋាននៃទីក្រុងរបស់យើង៖ ថ្នាក់ទី ៩-១១ ៈសិក្ខាសាលាសាលា។ - អិមៈមនុស្សជាតិ។ ed ។ មជ្ឈមណ្ឌល VLADOS, ឆ្នាំ ២០០១។ - ១១២ ទំ។
គីមីវិទ្យា៖ យោង។ ed./V ។ Schroeter, K.-H. Lautenschleger, H. Bibrak et al: ក្នុងមួយ។ ជាមួយវា។ - អិមៈគីមីវិទ្យាឆ្នាំ ១៩៨៩ ។ ed: GDR, 1986.- 648 ទំ។
ខ្សែសង្វាក់ផ្លាស់ប្តូរ
1. កាល់ស្យូមកាបូនកាល់ស្យូមអុកស៊ីដកាល់ស្យូមកាល់ស្យូមអ៊ីដ្រូសែនកាល់ស្យូមនីត្រាតកាល់ស្យូមនីត្រាត។
2. ម៉ាញ៉េស្យូមស៊ុលហ្វាតម៉ាញ៉េស្យូមនីត្រាតម៉ាញ៉េស្យូមអុកស៊ីតម៉ាញ៉េស្យូមអុកស៊ីដ។
3. កាល់ស្យូមក្លរីតកាល់ស្យូមស៊ុលហ្វាតកាល់ស្យូមស៊ុលហ្វីតកាល់ស្យូមស៊ុលហ្វីតកាល់ស្យូមអ៊ីដ្រូសែនកាល់ស្យូមអ៊ីដ្រូសែនកាល់ស្យូម។
4. ម៉ាញ៉េស្យូមម៉ាញ៉េស្យូមអុកស៊ីដម៉ាញ៉េស្យូមអ៊ីដ្រូស៊ីតម៉ាញ៉េស្យូមក្លរីតម៉ាញ៉េស្យូមអ៊ីដ្រូហ្សូកាបូនម៉ាញ៉េស្យូមស៊ុលហ្វាតម៉ាញ៉េស្យូមអ៊ីដ្រូសែន។
5. ម៉ាញ៉េស្យូមស៊ុលហ្វីតម៉ាញ៉េស្យូមអុកស៊ីដ ... ម៉ាញ៉េស្យូមអ៊ីដ្រូស៊ីត ... នីត្រាតម៉ាញ៉េស្យូម។
6. កាល់ស្យូមកាល់ស្យូមកាល់ស្យូមអ៊ីដ្រូសែនកាល់ស្យូមកាបូនកាល់ស្យូមអុកស៊ីដកាល់ស្យូមកាបូនកាល់ស្យូមកាបូណាតអ៊ីដ្រូកាបូនកាល់ស្យូមអ៊ីដ្រូកាបូន។
កិច្ចការដោះស្រាយ
កំរិត A
1. អន្តរកម្មនៃដែក ១៣,៧ ក្រាមជាមួយនឹងការបញ្ចេញទឹក ២,២៤ លីត្រ (ឧ។ ) ។ សម្គាល់លោហៈ។ តើអ្វីទៅជារបបទឹកភ្លៀងនិងបរិមាណអ្វីដែលត្រូវបានបង្កើតឡើងប្រសិនបើការបន្ថែមសូដ្យូមស៊ុលហ្វាតត្រូវបានបន្ថែមទៅក្នុងដំណោះស្រាយលទ្ធផល?
ដំណោះស្រាយ
ហ្គាស (H 2) ត្រូវបានបញ្ចេញក្នុងកំឡុងពេលអន្តរកម្មនៃក្រុមរង M Ia និង IIa ជាមួយទឹក។
យោងតាមច្បាប់សមមូល៖
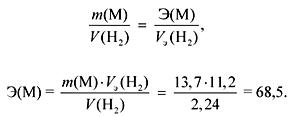
ប្រសិនបើក្រុមរងអេអាយអាយ, បន្ទាប់មក
ក r (M) \u003d ភាពជឿជាក់អ៊ី \u003d ៦៨.៥ (មិនមានលោហៈធាតុបែបនេះ) ។
ប្រសិនបើក្រុមរង M IIa, បន្ទាប់មក
ក r (M) \u003d ភាពជឿជាក់អ៊ី \u003d ១៣៧ (បា) ។
បា + ២ ហ ២ ឱ \u003d បា (អូ) ២ + ហ ២,
បា (អូអេ) ២ + ណា ២ សូ ៤ \u003d បាអេអូ ៤ + ២ អិន។ អូ,
(BaSO ៤) \u003d (បា (អូ) ២) \u003d (បា) \u003d\u003d ០១ ម។
m(BaSO ៤) \u003d ម\u003d 0.1 ២៣៣ \u003d ២៣.៣ ក្រាម។
ចម្លើយ។ ដែក - បា; m(BaSO ៤) \u003d ២៣.៣ ក្រាម។
2. តើសូលុយស្យុងអ៊ីដ្រូសែនកាល់ស្យូម 0,5 មីលីម៉ែត្រគួរតែត្រូវបានបន្ថែមទៅ 81 ក្រាមនៃដំណោះស្រាយ 10% (ដង់ស៊ីតេ 1 ក្រាម / សង់ទីម៉ែត្រ 3) នៃកាបូអ៊ីដ្រាតកាល់ស្យូមដើម្បីបញ្ចប់ការបង្កើតដីល្បាប់ដែរឬទេ? កំណត់ម៉ាស់ដីល្បាប់។
ចម្លើយ។ ១០០ មីលីលីត្រនៃ Ca (OH) ២, ១០ ក្រាមនៃ CaCO ៣ ។
3. ដំណោះស្រាយដែលមានផ្ទុក ២៣.៣ ក្រាមនៃល្បាយនៃប៉ូតាស្យូមស៊ុលហ្វាតនិងក្រូមីតត្រូវបានប៉ះពាល់ដោយការលើសនៃក្លរីតក្លរីត។ របបទឹកភ្លៀងត្រូវបានច្រោះចេញលាងហើយបន្ទាប់មកទឹកអាស៊ីត hydrochloric លើសត្រូវបានបន្ថែមទៅវា។ ផ្នែកមួយនៃរបបទឹកភ្លៀងត្រូវបានរំលាយផ្នែកដែលនៅសល់ត្រូវបានត្រងលាងនិងស្ងួត។ ម៉ាស់ទឹកភ្លៀងបន្ទាប់ពីស្ងួតគឺ ២៣.៣ ក្រាមកំណត់សមាសភាពនៃល្បាយដំបូង។
ចម្លើយ។ ១៧.៤ ក្រាមនៃ K ២ SO ៤ និង ៥.៩ ក្រាមនៃ K 2 CrO ៤ ។
4. មានល្បាយនៃកាល់ស្យូមអុកស៊ីតនិងកាល់ស្យូមកាបូអ៊ីដ្រាតដែលមានសមាមាត្រម៉ូលេគុលនៃសមាសធាតុនៃ 1: 3: 4 (តាមលំដាប់លំដោយ) ។ តើបរិមាណទឹកអ្វីខ្លះដែលអាចចូលទៅក្នុងអន្តរកម្មគីមីជាមួយនឹងល្បាយ 35 ក្រាម?
ចម្លើយ។ ១៧.៥៦៨ ម។ ល។
5. ភាពរលាយនៃអ៊ីដ្រូសែនអ៊ីដ្រូស៊ីដនៅក្នុងទឹកនៅសីតុណ្ហភាព ១០០ អង្សាសេគឺ ២៨ ក្រាមហើយនៅសីតុណ្ហភាព ២៥ អង្សាសេ - ១ ក្រាមក្នុងទឹក ១០០ ក្រាម។ 200 ក្រាមនៃសូលុយស្យុង strontium hydroxide ឆ្អែតនៅសីតុណ្ហភាព 100 អង្សាសេត្រូវបានត្រជាក់ដល់ 25 អង្សាសេ។ រកម៉ាសម៉ាសស្តុតអ៊ីដ្រូសែនអ៊ីដ្រូហ្សែតនៅពេលដែលដំណោះស្រាយត្រជាក់។
ចម្លើយ។ ៩៣.០៨ ក្រាមអេសអេស (អូ។ ) ២ ៨ ហ ២ អ។
កំរិតខ
1. ម៉ាស់កាបូនម៉ាញ៉េស្យូមគ្រីស្តាល់ជាក់លាក់ត្រូវបានគេរំលាយរហូតដល់ការវិវត្តនៃឧស្ម័នបានចប់។ ក្រោយមកទៀតត្រូវបានឆ្លងកាត់ដបទឹកហូរដោយទឹកអាស៊ីដស៊ុលហ្វួរីសនិងទឹកកំបោរ។ ម៉ាស់ហ្វ្លុកទីមួយកើនឡើង ១,៨ ក្រាមហើយក្នុងរបបទឹកភ្លៀង ២ ក្រាមធ្លាក់ចុះ។ កំណត់សមាសភាពនៃអ៊ីដ្រូសែនគ្រីស្តាល់ដែលចាប់ផ្តើមនិងម៉ាស់របស់វា។
ចម្លើយ។ MgCO 3 5H 2 O pentahydrate; ៣.៤៨ ក្រាម
2. សមាមាត្រម៉ូលេគុលនៃកាបូណាតប៊ីកាបូណាតនិងកាល់ស្យូមនីត្រាតក្នុងល្បាយមានទំងន់ ១០០ ក្រាមគឺ ១: ២: ៣ (តាមលំដាប់ចុះបញ្ជី) ។ តើបរិមាណអ្វីដែលមានសីតុណ្ហភាព ១២០០ អង្សាសេនិងសម្ពាធធម្មតានឹងធ្វើឱ្យផលិតផលខូចគុណភាពនៃល្បាយនេះទទួលយកបានដែរឬទេ?
ដំណោះស្រាយ
សមីការនៃប្រតិកម្មបំបែកធាតុផ្សំនៃល្បាយ។
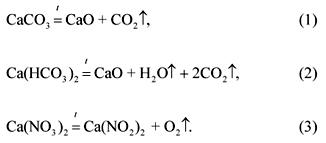
ដោយលក្ខខណ្ឌនៃបញ្ហា៖
(CaCO ៣)៖ (Ca (HCO ៣) ២): (Ca (ទេ ៣) ២) \u003d ១: ២: ៣ ។
សូមឱ្យ (CaCO 3) \u003d x mole បាន។
បន្ទាប់មក (Ca (HCO 3) 2) \u003d ២ x;
(កា (ទេ ៣) ២) \u003d ៣ x;
100x + 162 2x +164 3x \u003d100,
x 0,109 ម។
នៅ ទំ \u003d ១០១.៣ kPa និង t \u003d ១២០០ អង្សាសេនៅក្នុងស្ថានភាពខ្ជិលវាត្រូវបានបញ្ចេញ៖
CO 2 យោងតាមសមីការ (១)៖
1 (CO 2) \u003d (CaCO 3) \u003d x \u003d ០,១០៩ ម៉;
H 2 O, CO 2 យោងទៅតាមសមីការ (២)៖
២ (ហ ២ អូ) \u003d (Ca (HCO ៣) ២) \u003d ២ x \u003d ០.២១៨ ម៉,
២ (CO ២) \u003d ២ (Ca (HCO ៣) ២) \u003d ៤ x \u003d ០.៤៣៦ ម;
អូ ២ យោងតាមសមីការ (៣)៖
៣ (អូ ២) \u003d (Ca (ទេ ៣) ២) \u003d ៣ x \u003d ០៣២៧ ម។
ចំនួនសរុបនៃ moles នៃផលិតផលខូចរលួយ:
០.១០៩ + ០.២១៨ + ០,៤៣៦ + ០៣២៧ \u003d ១,០៩ មម (ន។ ) ។
ពីសមីការនៃរដ្ឋឧស្ម័ន្ធល្អយើងរកឃើញបរិមាណ៖
pV = ត្រ។ អរ,
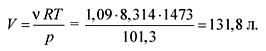
ចម្លើយ. វី \u003d ១៣១.៨ លីត្រ
3. ល្បាយនៃបរិមាណអ៊ីដ្រូសែនអ៊ីដ្រូកាបូននិងកាបូនឌីអុកស៊ីតមានបរិមាណស្មើគ្នា។ ម៉ាសនៃសំណល់រឹងបានប្រែជា ១,៧៧៥ ដងតិចជាងម៉ាសនៃល្បាយដំបូង។ ចំពោះសំណល់នេះត្រូវបានបន្ថែមចំនួន ១០ ដងនៃបរិមាណដ៏ច្រើននៃដំណោះស្រាយអាស៊ីតស៊ុលហ្វួរីស ៥% ។ គណនាប្រភាគដ៏ធំនៃសារធាតុនៅក្នុងដំណោះស្រាយលទ្ធផល។
ចម្លើយ។ ៦% មីហ្គេស ៤ ។
4. នៅពេលដែលទឹកត្រូវបានព្យាបាលដោយល្បាយអ៊ីដ្រូសែននិងនីត្រាតនៃលោហៈធាតុដែលមានបរិមាណប្រភាគស្មើគ្នានោះល្បាយឧស្ម័នត្រូវបានបង្កើតឡើងដោយដង់ស៊ីតេអ៊ីដ្រូសែន ២,៦៥៨ ។ កំណត់លោហៈដែលមាននៅក្នុងសមាសធាតុ (កុំប្រមូលលេខនៅពេលគណនា!) ។
ចម្លើយ។ កាល់ស្យូម
5. ចានម៉ាញ៉េស្យូម ១៦ ក្រាមត្រូវបានទម្លាក់ចូលទៅក្នុងសូលុយស្យុងស្ពាន់ (II) ១៦% មានទំងន់ ៣៥០ ក្រាមនៅពេលដែលចានត្រូវបានដកចេញបំណែកប្រភាគនៃអំបិលដែលមាននៅក្នុងសូលុយស្យុងប្រែជាដូចគ្នា។ តើម៉ាសចានបានប៉ុន្មានដង?
ចម្លើយ។ ៤.៥ ដង។
ភារកិច្ចគុណភាព
1. តើសារធាតុមួយណាដែលនឹងមានអន្តរកម្មជាមួយអ៊ីដ្រូសែនម៉ាញ៉េស្យូមៈអាស៊ីតអ៊ីដ្រូក្លរីកអាស៊ីតនីទ្រីកកាបូនឌីអុកស៊ីតសូដ្យូមក្លរួសូដ្យូមអ៊ីដ្រូសែនស៊ុលហ្វីលីកទង់ដែង (II) កត់សុី?
ចម្លើយ។ HCl, HNO 3, H 2 SO 4 ។
2. នៅក្នុងដបដែលគ្មានស្លាកគឺសូដាដីសហ្គីបស៊ូមនិងសូដ្យូមស៊ុលហ្វាត។ តើសារធាតុទាំងនេះអាចត្រូវបានទទួលស្គាល់ដោយទឹកនិងអាស៊ីតនីទ្រីកយ៉ាងដូចម្តេច?
ចម្លើយ.
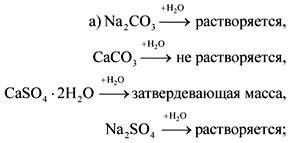
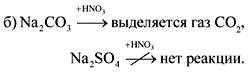
3. សារធាតុ A គឺជាលោហៈធាតុមានពណ៌សស្រាលនិងស។ នៅក្នុងអន្តរកម្មនៃសារធាតុ A ជាមួយខដែលជាសារធាតុហ្គាសដ៏សាមញ្ញសមាសធាតុ C ត្រូវបានបង្កើតឡើងដែលរលាយក្នុងទឹកដើម្បីបង្កើតជាដំណោះស្រាយអាល់កាឡាំង។ នៅពេលកែច្នៃសារធាតុជាមួយអាស៊ីតស៊ុលហ្វួរីអំបិលត្រូវបានបង្កើតឡើងជាតិទឹកគ្រីស្តាល់ដែលត្រូវបានប្រើក្នុងវេជ្ជសាស្ត្រសម្រាប់ការអនុវត្តការស្លៀកពាក់រ៉ាំរ៉ៃសម្រាប់ការបាក់ឆ្អឹង។ ផ្តល់សមីការប្រតិកម្ម។
ចម្លើយ។ កគឺកា; ខគឺក្រុមហ៊ុន H 2; C គឺ CaH 2; hydrate គ្រីស្តាល់ - CaSO 4 2H 2 O ។
4. សារធាតុ A គឺជាអុកស៊ីដរលាយក្នុងទឹកដើម្បីបង្កើតជាដំណោះស្រាយអាល់កាឡាំង។ សមាសធាតុខក្នុងសូលុយស្យុងនេះមានប្រតិកម្មជាមួយឧស្ម័នគ្មានក្លិន C ដើម្បីបង្កើតរបបទឹកភ្លៀងពណ៌សដែលរលាយបន្តិចម្តង ៗ នៅពេលដែលឧស្ម័ន C ឆ្លងកាត់បន្ថែមទៀតឱ្យសមីការប្រតិកម្មនិងកំណត់អត្តសញ្ញាណសារធាតុទាំងនោះ។
ចម្លើយ។ មួយគឺ CaO, BaO; ខគឺ Ca (OH) ២, Ba (OH) ២; C គឺជា CO 2 ។
5. សារធាតុ A ដែលជាផ្នែកមួយនៃសារធាតុរ៉ែទូទៅបំផុតមួយនៅលើសំបកផែនដីរលួយនៅសីតុណ្ហភាពខ្ពស់ទៅជាអុកស៊ីដពីរដែលមួយក្នុងនោះ B ត្រូវបានបង្កើតឡើងជានិច្ចក្នុងដំណើរជីវិត។ នៅពេលដែលសារធាតុ B មានអន្តរកម្មជាមួយក្រាហ្វិចនៅពេលដែលកម្តៅឧស្ម័ន C ដែលមានជាតិពុលដល់សត្វដែលមានឈាមក្តៅគឺងាយឆេះគ្មានពណ៌និងមានក្លិន។ ផ្តល់សមីការនៃប្រតិកម្ម, កំណត់អត្តសញ្ញាណសារធាតុ។
ចម្លើយ។ ក - CaCO 3; ខគឺ CO 2; ស៊ី - ស៊ី។
ភាពរឹងរបស់ទឹកនិងការលុបបំបាត់ចោល
គីមីវិទ្យាអរូបី
ប្រធានបទ៖“ ភាពរឹងរបស់ទឹក”
អ្នកម៉ៅការនៃការងារ៖Grabin Pavel.
ផែនការ
សេចក្តីផ្តើម ៣
ការកំណត់ភាពរឹងរបស់ទឹក។ ៣
បច្ចេកទេសរឹង ៤
ឯកសារយោង ៦
សេចក្តីផ្តើម
នៅក្នុងរូងភ្នំរូងភ្នំជួបជាមួយទម្រង់ថ្មកំបោរដ៏ស្រស់ស្អាតបំផុត - ស្តុបស្តូតដែលព្យួរពីធ្នូនិង stalagmites រីកលូតលាស់ឡើង។ តាមទស្សនៈគីមីវិទ្យាការកើតឡើងនៃការបង្កើតធម្មជាតិដ៏អស្ចារ្យទាំងនេះគឺភាពរឹងនៃទឹកក្រោមដី។ យើងជួបប្រទះនឹងគំនិតនៃភាពរឹងរបស់ទឹកមិនត្រឹមតែក្នុងវិស័យវិទ្យាសាស្ត្រនិងភូគព្ភសាស្ត្រប៉ុណ្ណោះទេប៉ុន្តែជាទូទៅនៅគ្រប់ទីកន្លែង - ទាំងគីមីវិទ្យាបច្ចេកវិទ្យានិងសូម្បីតែនៅក្នុងជីវិតប្រចាំថ្ងៃ។ ហេតុដូច្នេះហើយគំនិតនេះមានសារៈសំខាន់ណាស់សម្រាប់ការកំណត់គុណភាពទឹក។
ការកំណត់ភាពរឹងរបស់ទឹក
ភាពរឹងរបស់ទឹក - ទ្រព្យសម្បត្តិទឹក (មិនត្រូវលាងសម្អាតដើម្បីផ្តល់ជញ្ជីងក្នុងឡចំហាយចំហាយ) ដែលជាប់ទាក់ទងនឹងខ្លឹមសារនៃសមាសធាតុកាល់ស្យូមនិងម៉ាញ៉េស្យូមរលាយនៅក្នុងវានេះគឺជាប៉ារ៉ាម៉ែត្របង្ហាញពីខ្លឹមសារនៃការដកកាល់ស្យូមនិងម៉ាញ៉េស្យូមនៅក្នុងទឹក។
ភាពរឹងគឺជាលក្ខណៈពិសេសនៃទឹកដែលកំណត់គុណសម្បត្ដិរបស់អតិថិជនភាគច្រើនហើយដូច្នេះវាមានតម្លៃសេដ្ឋកិច្ចសំខាន់។ ទម្រង់ទឹករឹងធ្វើមាត្រដ្ឋាននៅលើជញ្ជាំងនៃឡចំហាយកំដៅអាគុយជាដើមដែលបំផ្លាញមុខងារកម្ដៅរបស់វាយ៉ាងខ្លាំង។ ស្រទាប់ស្តើងបែបនេះនៅលើផ្ទៃកំដៅគឺមិនមានគ្រោះថ្នាក់អ្វីទាំងអស់ចាប់តាំងពីរយៈពេលនៃការឡើងកំដៅតាមរយៈស្រទាប់ស្នាមដែលមានចរន្តកំដៅទាបកើនឡើងបន្តិចម្តង ៗ បាតរលាកចេញលឿននិងលឿនជាងមុន - បន្ទាប់ពីលោហៈធាតុត្រជាក់កាន់តែយឺតនិងយឺត ៗ រាល់ពេលវានៅតែស្ថិតក្នុងស្ថានភាពក្តៅខ្លាំងក្នុងរយៈពេលយូរ។ នៅទីបញ្ចប់វាអាចកើតឡើងដែលថាបាតនៃនាវានឹងមិនទប់ទល់និងអនុញ្ញាតឱ្យលេចធ្លាយ។ ការពិតនេះមានគ្រោះថ្នាក់ខ្លាំងណាស់នៅក្នុងឧស្សាហកម្មដែលមានឡចំហាយចំហាយ។
ទឹករឹងមិនសមស្របសម្រាប់ការលាងទេ។ ធ្វើមាត្រដ្ឋានលើឧបករណ៍កំដៅរបស់ម៉ាស៊ីនបោកគក់ធ្វើឱ្យពួកគេមិនមានសណ្តាប់ធ្នាប់វាក៏កាន់តែអាក្រក់ដល់លក្ខណៈលាងរបស់សាប៊ូផងដែរ។ ការដកស្រង់ Ca 2+ និង Mg 2+ មានប្រតិកម្មជាមួយអាស៊ីតខ្លាញ់សាប៊ូដើម្បីបង្កើតជាអំបិលរលាយមិនល្អដែលបង្កើតជាខ្សែភាពយន្តនិងទឹកភ្លៀងនៅទីបំផុតកាត់បន្ថយគុណភាពនៃការបោកគក់និងបង្កើនការប្រើប្រាស់សាប៊ូបោកខោអាវ។ គំរបទឹករឹង
ភាពរឹងមានពីរប្រភេទគឺបណ្តោះអាសន្ននិងអចិន្រ្តៃយ៍។ ភាពខុសគ្នានេះគឺដោយសារតែប្រភេទនៃថ្នាំដែលមានវត្តមាននៅក្នុងដំណោះស្រាយជាការប្រឆាំងនឹងកាល់ស្យូមនិងម៉ាញ៉េស្យូម។
ភាពរឹងជាបណ្តោះអាសន្ន បានផ្សារភ្ជាប់ជាមួយនឹងវត្តមាននៅក្នុងទឹករួមជាមួយការដកស្រង់ Ca 2+, Mg 2+ និង Fe 2+ នៃអ៊ីដ្រូកាបូនឬ anions bicarbonate (HCO 3 -) ។
ភាពរឹងអចិន្រ្តៃយ៍ (ឬមិនមែនកាបូន) កើតឡើងប្រសិនបើស៊ុលស៊ុលក្លរីតនីត្រាតនិងអាស៊ីតដទៃទៀតមាននៅក្នុងដំណោះស្រាយនោះអំបិលកាល់ស្យូមនិងម៉ាញ៉េស្យូមដែលរលាយល្អហើយដូច្នេះមិនអាចយកចេញបានទេ។ ភាពរឹងសរុបត្រូវបានកំណត់ជាមាតិកាសរុបនៃអំបិលកាល់ស្យូមនិងម៉ាញ៉េស្យូមទាំងអស់នៅក្នុងដំណោះស្រាយ។
ប្រទេសផ្សេងៗគ្នាមានស្តង់ដាររឹងសម្រាប់ទឹក។ នៅក្នុងប្រទេសរបស់យើងទឹកត្រូវបានចាត់ថ្នាក់ដោយភាពរឹងតាមរបៀបនេះ:
ទឹកទន់ដែលមានកំរាស់តិចជាង ៣.០ ម៉ែល / លីត្រ
ភាពរឹងមធ្យម ៣.០-៦.០ mEq / អិល
រឹង - ច្រើនជាង 6.0 mEq / ml ។
វិធីសាស្រ្តក្នុងការលុបបំបាត់ភាពរឹង។
ដើម្បីកម្ចាត់ភាពរឹងជាបណ្តោះអាសន្នអ្នកគ្រាន់តែត្រូវការដាំទឹកឱ្យពុះ។ នៅពេលដែលទឹកក្តៅអាន់ទិកប៊ីកាបូណាតមានប្រតិកម្មជាមួយនឹងការដកស្រង់ហើយបង្កើតបានជាអំបិលកាបូនដែលរលាយមិនសូវល្អជាមួយពួកវាដែលមានទឹកភ្លៀង។
Ca 2 + 2HCO 3 - \u003d CaCO 3 ↓ + H 2 O + CO 2
ជាមួយនឹងអ៊ីយ៉ុងដែកប្រតិកម្មកាន់តែស្មុគស្មាញដោយសារតែការពិតដែលថា FeCO 3 គឺជាសារធាតុមិនស្ថិតស្ថេរនៅក្នុងទឹក។ នៅក្នុងវត្តមាននៃអុកស៊ីសែនផលិតផលចុងក្រោយនៃខ្សែសង្វាក់ប្រតិកម្មគឺហ្វី (អូអេដ) ៣ ដែលជារបបទឹកភ្លៀងពណ៌ក្រហមងងឹត។ ដូច្នេះជាតិដែកនៅក្នុងទឹកកាន់តែច្រើនពណ៌កាន់តែខ្លាំងនៅជញ្ជីងដែលត្រូវបានដាក់នៅលើជញ្ជាំងនិងបាតនៃនាវាក្នុងពេលពុះ។
ភាពរឹងថេរគឺពិបាកក្នុងការប្រយុទ្ធ។ ជម្រើសមួយ: ទឹកកកត្រជាក់។ អ្នកគ្រាន់តែត្រូវការបង្កកទឹកបន្តិចម្តង ៗ ។ នៅពេលមានអង្គធាតុរាវប្រមាណ ១០% ពីបរិមាណនៅសល់វាចាំបាច់ត្រូវបង្ហូរទឹកដែលមិនកកហើយបង្វែរទឹកកកទៅជាទឹកវិញ។ អំបិលទាំងអស់ដែលបង្កើតបានជារឹងនៅតែរក្សាក្នុងទឹកមិនកក។
ចំណីអាហារគឺជាវិធីមួយ - ការធ្វើឱ្យមានភាពច្របូកច្របល់ពោលគឺការហួតទឹកជាមួយនឹងការ condensation ជាបន្តបន្ទាប់របស់វា។ ដោយសារអំបិលគឺជាសមាសធាតុមិនងាយនឹងបង្កជាហេតុវានៅតែមានហើយទឹកហួត។
ប៉ុន្តែវិធីសាស្រ្តដូចជាការត្រជាក់និងការច្របាច់ទឹកគឺសមស្របសម្រាប់តែបន្ទន់បរិមាណទឹកតិចតួចប៉ុណ្ណោះ។ ឧស្សាហកម្មកំពុងដោះស្រាយជាមួយតោន។ ដូច្នេះវិធីសាស្រ្តផ្សេងទៀតត្រូវបានប្រើ។ វិធីសាស្រ្តផ្លាស់ប្តូរស៊ីម៉ងត៍ដែលត្រូវបានគេប្រើជាទូទៅបំផុតដោយផ្អែកលើការប្រើប្រាស់នៃការជំនួសពិសេស - ការផ្លាស់ប្តូរស៊ីម៉ងត៍ដែលត្រូវបានផ្ទុកទៅក្នុងតម្រងហើយនៅពេលដែលទឹកត្រូវបានឆ្លងកាត់ពួកវាជំនួសស៊ីលីននិងម៉ាញ៉េស្យូមជាមួយស៊ីដ្យូម។
ជាមួយនឹងផលវិបាកនៃភាពរឹងនៃទឹក - មាត្រដ្ឋានពីចំណុចនៃគីមីសាស្ត្រអ្នកអាចប្រយុទ្ធបានយ៉ាងងាយស្រួល។ វាចាំបាច់ក្នុងការជះឥទ្ធិពលលើអំបិលនៃអាស៊ីតខ្សោយជាមួយអាស៊ីតខ្លាំង។ ក្រោយមកទៀតជំនួសកន្លែងធ្យូងថ្មដែលមិនស្ថិតស្ថេរបំផ្លាញដល់ទឹកនិងកាបូនឌីអុកស៊ីត។ សមាសភាពនៃជញ្ជីងអាចរួមបញ្ចូលស៊ីលីតនិងស៊ុលហ្វាតនិងផូស្វាត។ ប៉ុន្តែប្រសិនបើអ្នកបំផ្លាញ "គ្រោងឆ្អឹងកាបូន" បន្ទាប់មកសមាសធាតុទាំងនេះនឹងមិនស្ថិតនៅលើផ្ទៃទេ។
ទឹកអាស៊ីត Adipic និង anhydride របស់បុរសដែលត្រូវបានបន្ថែមទៅក្នុងទឹកក៏ត្រូវបានគេប្រើជាភ្នាក់ងារកម្ចាត់ចោលដែរ។ សារធាតុទាំងនេះខ្សោយជាងអាស៊ីតស្ពាន់ធ័រដូច្នេះការពុះក៏ចាំបាច់សម្រាប់ការដកខ្លួនចេញដែរ។
ឯកសារយោង៖
Shpausus Z. ធ្វើដំណើរទៅពិភពគីមីវិទ្យា - ម៉ូស្គូ: ការអប់រំឆ្នាំ ១៩៦៧ - ៤៣១ ។
ខាឡាំពៅវិចជី។ គីមីវិទ្យាមានច្រើនផ្នែក។ - អិមៈការអប់រំឆ្នាំ ១៩៩២ -១៥៩ ទំ។
Khomchenko G.P. សៀវភៅគីមីវិទ្យា –M .: រលកថ្មីឆ្នាំ ១៩៩៦ - ៣០៤ ភី។
អត្ថបទស្រដៀងគ្នា៖
ការសិក្សាអំពីលក្ខណៈសម្បត្តិនៃដំណោះស្រាយរាវនៃសារធាតុប៉ូលីយូធ្យូតដោយពិចារណាលើកត្តាពីរគឺការអនុលោមនៃម៉្រូតូកូលក្នុងដំណោះស្រាយនិងលំដាប់តំរង់ទិសនៃម៉ូលេគុលសូលុយស្យុងរលាយដែលត្រូវបានវិនិច្ឆ័យដោយប៉ារ៉ាម៉ែត្រទែម៉ូម៉ែត្រនិងរចនាសម្ព័ន្ធនៃដំណោះស្រាយ។
គោលបំណងនិងរចនាសម្ព័ននៃតម្រងអ៊ីយ៉ុងស្របគ្នានៃដំណាក់កាលទីមួយនិងទីពីរសកម្មភាពចម្រុះ។ លក្ខណៈនៃបច្ចេកវិទ្យាអ៊ីយ៉ូដអ៊ីដ្រូសែនចរន្ត។ ការពិពណ៌នាអំពីវិធីសាស្រ្តសូដ្យូមស៊ីអ៊ីតនៃការបន្ទន់ទឹក។ គោលការណ៍នៃការអស់សង្ឃឹមនិងការចង់បានទឹក។
អ្នកផ្លាស់ប្តូរស៊ីម៉ងត៍និងទ្រព្យសម្បត្តិរបស់ពួកគេ។ ដំណើរការនៃការបន្ទន់ទឹកដោយសូដ្យូមសូដ្យូម។ ម៉ាស៊ីនផ្លាស់ប្តូរទឹកអ៊ីដ្រូសែន - សូដ្យូម - ស៊ីអ៊ីត។ វិធីសាស្រ្តនៃការ calc-cationite និងការដកស្រង់ដោយផ្នែក។ តម្រងផ្លាស់ប្តូរស៊ីស៊ីនិងឧបករណ៍ជំនួយការតំឡើងប្តូរស៊ីម៉ងត៍។
តើស្នោនិង surfactants គឺជាអ្វី។ ភាពតានតឹងលើផ្ទៃគឺជាលក្ខណៈសំខាន់បំផុតនៃចំណុចប្រទាក់ដំណាក់កាល។ វិធីសាស្រ្តនៃការសិក្សាពិសោធន៍នៃឥទ្ធិពលនៃភាពរឹងរបស់ទឹកទៅលើស្នោនិងស្ថេរភាពស្នោសម្រាប់ប្រភេទផ្សេងៗនៃ surfactants ។
លក្ខណៈសម្បត្តិនៃទឹកនិងវិធីសាស្រ្តធ្វើឱ្យវាទន់។ តម្រូវការសម្រាប់ភាពរឹងនៃទឹកដែលប្រើប្រាស់នៅក្នុងឧស្សាហកម្មកំដៅនិងថាមពល។ មូលដ្ឋានគ្រឹះទ្រឹស្តីនិងវិធីសាស្រ្តក្នុងការកំណត់ភាពរឹងរបស់ទឹកដោយប្រើវិធីសាស្រ្តស្មុគស្មាញ។ គំរូ, ការនិយាយឡើងវិញ, ការប្តេជ្ញាចិត្ត។
ការផលិតកាបូនដោយការបំផ្លាញកម្ដៅឈើការស្រូបយកសារធាតុរំលាយនិងឧស្ម័នដោយធ្យូងថ្ម។ អន្តរកម្មនៃកាបូនឌីអុកស៊ីតជាមួយអាល់កាឡាំងការផលិតកាបូនម៉ូណូអុកស៊ីតនិងការសិក្សាអំពីលក្ខណៈសម្បត្តិរបស់វា។ ភាពស៊ាំជាមួយលក្ខណៈសម្បត្តិនៃកាបូននិងកាបូណាត។
សូចនាករលក្ខខណ្ឌនៃគុណភាពទឹកផឹក។ ការកំណត់សារធាតុសរីរាង្គក្នុងទឹកទង់ដែងនិងអ៊ីយ៉ុងសំណ។ វិធីសាស្រ្តដើម្បីលុបបំបាត់ភាពរឹងរបស់ទឹក។ វិធីសម្អាតទឹក។ ការរៀបចំដំណោះស្រាយដែលមានប្រសិទ្ធភាពនៃស៊ុលហ្វាតប៉ូតាស្យូម។ ការបន្សុតទឹកដោយការត្រជាក់ដោយផ្នែក។
លក្ខណៈគីមីរបស់កាល់ស្យូម។ ការប្រើប្រាស់កាបូនកាល់ស្យូមសុទ្ធនៅក្នុងអុបទិច, ថ្មកំបោរនៅក្នុងលោហធាតុ - ដូចជាលំហូរ។ ហ្គីបសីមជាអ៊ីដ្រូលីកស៊ុលហ្វីលីក។ អំបិលកាល់ស្យូមនៃអាស៊ីតផូស្វ័រដែលជាធាតុផ្សំសំខាន់នៃផូស្វ័រនិងអេតាទីត។
ភាពខុសគ្នានៃសមាសធាតុកាបូនការចែកចាយរបស់ពួកគេនៅក្នុងធម្មជាតិនិងការអនុវត្ត។ ការផ្លាស់ប្តូរអ៊ីប៉ូតាទិក។ លក្ខណៈសម្បត្តិរូបវន្តនិងរចនាសម្ព័ន្ធនៃអាតូមកាបូនសេរី។ លក្ខណៈគីមីនៃកាបូន។ កាបូននិងកាបូណាត។ រចនាសម្ព័នពេជ្រនិងក្រាហ្វិច។
ចរិតលក្ខណៈលីចូស្យូសសមាសធាតុនៃធាតុគីមីនិងសារធាតុរ៉ែនៅក្នុងសំបកផែនដី។ រចនាសម្ព័ន្ធសមាសធាតុគីមីនិងមុខងារនៃវារីអគ្គិសនីបរិយាកាស។ លក្ខណៈពិសេសនៃរស្មីសំយោគនៃសារធាតុសរីរាង្គដែលកើតឡើងនៅក្នុងជីវឧស្ម័ន។ ការសិក្សាអំពីដំណើរការជីវឧស្ម័ន។
ភាពរឹងរបស់ទឹកខ្ពស់នៅក្នុងប្រព័ន្ធកំដៅនិងប្រព័ន្ធទឹកក្តៅក្នុងស្រុកជះឥទ្ធិពលអវិជ្ជមានដល់ដំណើរការផ្ទេរកំដៅបង្កើនការប្រើប្រាស់ថាមពល។ លើសពីនេះទៀតទឹកផឹករឹងអាចបង្កគ្រោះថ្នាក់ដល់សុខភាពមនុស្ស។ សម្រាប់ទឹកសម្រាប់គោលបំណងផ្សេងៗវិធីសាស្រ្តបន្ទន់ផ្សេងៗត្រូវបានប្រើ។
ការបន្ទន់ទឹកគឺជាដំណើរការនៃការយកអំបិលរឹងចេញពីទឹក។ ប៉ុន្តែតើអ្វីទៅជាភាពរឹងរបស់ទឹកហើយហេតុអ្វីវាគួរតែត្រូវបានយកចេញ?
គំនិតនៃភាពរឹងរបស់ទឹកជាធម្មតាត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងការដកស្រង់កាល់ស្យូម (Ca 2+) និងក្នុងកម្រិតតិចជាងនេះគឺម៉ាញ៉េស្យូម (មី ២+) ។ ជាការពិតរាល់ការដកស្រង់សញ្ញាសំគាល់ពីមួយដឺក្រេឬមួយផ្សេងទៀតប៉ះពាល់ដល់ភាពរឹង។ ពួកវាធ្វើអន្តរកម្មជាមួយតណ្ហាបង្កើតជាសមាសធាតុ (អំបិលរឹង) ដែលអាចធ្វើអោយទឹកភ្លៀង។
អំបិលដែកម៉ង់ហ្គាណែសនិងស្តូត្យូមក៏អាចមានទឹកភ្លៀងដែរប៉ុន្តែនៅក្នុងការអនុវត្តធាតុទាំងអស់នេះមានឥទ្ធិពលតិចតួចទៅលើភាពរឹងដែលជាធម្មតាពួកគេត្រូវបានគេមិនយកចិត្តទុកដាក់។
អាលុយមីញ៉ូម (អាល់ ៣+) និងដែក ferric (Fe 3+) ក៏ជះឥទ្ធិពលដល់ភាពរឹងដែរប៉ុន្តែនៅកំរិត pH ដែលត្រូវបានរកឃើញនៅក្នុងទឹកធម្មជាតិភាពរលាយរបស់ពួកគេហើយដូច្នេះ“ ការចូលរួមចំណែក” ចំពោះភាពរឹងគឺមិនអាចធ្វេសប្រហែសបានទេ។ ស្រដៀងគ្នានេះដែរឥទ្ធិពលមិនសំខាន់នៃបារីយ៉ូម (បា ២+) មិនត្រូវបានគេគិតទេ។
ប្រភេទនៃភាពរឹង
មានភាពរឹងនៃទឹកច្រើនប្រភេទ។ ភាពរឹងសរុបត្រូវបានកំណត់ដោយកំហាប់សរុបនៃអ៊ីយ៉ុងកាល់ស្យូមនិងម៉ាញ៉េស្យូម។ វាគឺជាផលបូកនៃកាបូន (បណ្តោះអាសន្ន) និងរឹងដែលមិនមែនជាកាបូន (អចិន្រ្តៃយ៍) ។
ភាពរឹងនៃកាបូនគឺដោយសារតែវត្តមានអ៊ីដ្រូកាបូននិងកាបូននៅក្នុងទឹក (នៅ pH\u003e 8.3) ។ ភាពរឹងជាបណ្តោះអាសន្នត្រូវបានកំណត់ដោយវត្តមាននៅក្នុងទឹករួមជាមួយ Ca 2+, Mg 2+ និង Fe 2+ ដកស្រង់អ៊ីដ្រូសែនកាបូណាតឬ anions ប៊ីការ៉ាបូត (HCO 3-) ។ ប្រភេទរឹងនេះស្ទើរតែត្រូវបានលុបចោលទាំងស្រុងដោយទឹកពុះហើយនោះជាមូលហេតុដែលវាត្រូវបានគេហៅថារឹងរឹងបណ្តោះអាសន្ន។ នៅពេលដែលទឹកត្រូវបានកំដៅអ៊ីដ្រូកាបូនបណ្តាលឱ្យរលាយបង្កើតជាអាស៊ីតកាបូនិកនិង precipitate កាបូនកាល់ស្យូមម៉ាញ៉េស្យូមអ៊ីដ្រូអ៊ីដនិងជាតិដែក។
ភាពរឹងដែលមិនមែនជាកាបូនគឺដោយសារតែវត្តមាននៃអំបិលកាល់ស្យូមនិងម៉ាញ៉េស្យូមនៃអាស៊ីដខ្លាំង (ស្ពាន់ធ័រនីត្រាតអ៊ីដ្រូក្លរីក) ហើយមិនត្រូវបានលុបចោលដោយការពុះទេដូច្នេះវាត្រូវបានគេហៅថារឹងថេរ។
ឯកតា
នៅក្នុងការអនុវត្តពិភពលោកផ្នែកជាច្រើននៃភាពរឹងត្រូវបានប្រើពួកគេទាំងអស់ត្រូវបានទាក់ទងគ្នាតាមរបៀបជាក់លាក់ជាមួយគ្នា។
ឯកតាភាពរឹងត្រូវបានយកជាភាពរឹងនៃទឹកក្នុង ១ លីត្រមានផ្ទុក ១ មីល្លីលស្មើនឹង Ca 2+ ឬ Mg 2+ ។ មួយឯកតារឹង (១ មិល្លីលីត្រ / អិល) ត្រូវនឹងខ្លឹមសារនៃអ៊ីយ៉ុងកាល់ស្យូមស្មើនឹង ២០,០៤ មីលីក្រាម / លីត្រឬអ៊ីយ៉ុងម៉ាញ៉េស្យូមស្មើនឹង ១២,១៥ មីលីក្រាម / អិល។ ភាពរឹងនៃទឹកសរុបអាចត្រូវបានគណនាដោយរូបមន្ត៖
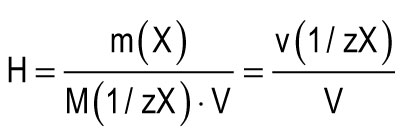
m (X) គឺជាម៉ាស់នៃសារធាតុរំលាយ, មីលីក្រាម; M (1 / zX) គឺជាម៉ាស់ម៉ាស់នៃសមមូលនៃសារធាតុ, មីលីក្រាម / មីល្លីម (ក្រាម / ម៉ុល); V គឺជាបរិមាណទឹក, លីត្រ; ម (1 / zCa 2+) \u003d 20.04 មីលីក្រាម / មិល្លីល; ម (1 / zMg 2+) \u003d 12,15 មីលីក្រាម / មិល្លីល។
លើសពីនេះទៀតអង្គភាពរឹងដូចជាដឺក្រេអាឡឺម៉ង់ (,d, dH), សញ្ញាប័ត្របារាំង ()f), សញ្ញាប័ត្រអាមេរិច, ppm CaCO 3 ត្រូវបានគេប្រើយ៉ាងទូលំទូលាយនៅក្នុងប្រទេសក្រៅ។
សមាមាត្រនៃគ្រឿងរឹងទាំងនេះត្រូវបានបង្ហាញនៅក្នុងតារាង។ ១ ។
តារាង ១. សមាមាត្រនៃឯកតាផ្សេងៗគ្នានៃភាពរឹង
ដូច្នេះសញ្ញាប័ត្រអាឡឺម៉ង់មួយត្រូវនឹង ១០ មីលីក្រាមក្នុងមួយម៉ែត ៣ ស៊ីអូឬ ១៧,៨៦ មីលីក្រាម / ម។ ម។ ឃ។ ៣ ក្នុងទឹក។ សញ្ញាប័ត្របារាំងមួយគឺ ១០ មីលីក្រាម / ម។ ម ៣ CaCO ៣ ក្នុងទឹកហើយសញ្ញាប័ត្រអាមេរិកស្មើនឹង ១ មីលីក្រាម / ដុម ៣ CaCO ៣ ក្នុងទឹក។
ភាពរឹងរបស់ទឹកខុសគ្នាយ៉ាងខ្លាំងហើយមានចំណាត់ថ្នាក់ជាច្រើនប្រភេទ។ ដូច្នេះនៅប្រទេសអាឡឺម៉ង់បទដ្ឋានតឹងរឹងនៃវិទ្យាស្ថានស្តង់ដារភាវូបនីយកម្ម (DIN ឆ្នាំ ១៩៦៤៣) ត្រូវបានអនុវត្តហើយនៅសហរដ្ឋអាមេរិក - ការចាត់ថ្នាក់ដែលត្រូវបានអនុម័តដោយទីភ្នាក់ងារការពារបរិស្ថាន (USEPA) ក្នុងឆ្នាំ ១៩៨៦ (តារាងទី ២) ។
តារាងទី ២ ចំណាត់ថ្នាក់នៃប្រភេទផ្សេងៗគ្នានៃភាពរឹង
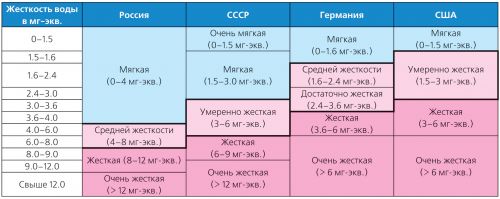
តើទឹកណាដែលទន់ជាង
ជាធម្មតានៅក្នុងទឹកដែលមានជាតិខនិជទាបភាពរឹងលើសលុបដោយសារអ៊ីយ៉ុងកាល់ស្យូម (ទោះបីជាក្នុងករណីខ្លះភាពរឹងម៉ាញ៉េស្យូមអាចឡើងដល់ ៥០-៦០%) ។ ជាមួយនឹងការកើនឡើងនៃកម្រិតនៃការធ្វើឱ្យមានជាតិរ៉ែទូទៅមាតិកានៃអ៊ីយ៉ុងកាល់ស្យូម (Ca 2+) មានការថយចុះយ៉ាងឆាប់រហ័សហើយកម្រលើសពី 1 ក្រាម / លីត្រ។ ខ្លឹមសារនៃអ៊ីយ៉ុងម៉ាញ៉េស្យូម (មី ២+) នៅក្នុងទឹកដែលមានជាតិរ៉ែខ្ពស់អាចឈានដល់ក្រាមជាច្រើនហើយនៅក្នុងបឹងអំបិល - រាប់សិបក្រាមក្នុងមួយលីត្រទឹក។
ជាទូទៅភាពរឹងរបស់ទឹកលើផ្ទៃទឹកជាទូទៅតិចជាងភាពរឹងរបស់ទឹកក្រោមដី។ ភាពរឹងនៃទឹកលើផ្ទៃគឺត្រូវមានការប្រែប្រួលតាមរដូវដែលគួរឱ្យកត់សម្គាល់ជាធម្មតាឈានដល់តម្លៃខ្ពស់បំផុតនៅចុងបញ្ចប់នៃរដូវរងារនិងទាបបំផុតក្នុងអំឡុងពេលទឹកជំនន់នៅពេលដែលវាត្រូវបានពនលាយជាមួយទឹកភ្លៀងទន់និងទឹករលាយ។ ទឹកសមុទ្រនិងមហាសមុទ្រមានភាពរឹងខ្ពស់ណាស់ (រាប់សិបរយ meq / l) ។
ផលវិបាកនៃភាពរឹង
ទឹកផឹករឹងគឺជូរចត់ដោយសារតែរសជាតិម៉ាញ៉េស្យូមនិងមានឥទ្ធិពលអវិជ្ជមានទៅលើប្រព័ន្ធរំលាយអាហារ។ យោងទៅតាមស្តង់ដាររបស់អង្គការសុខភាពពិភពលោក (WHO) ភាពរឹងល្អបំផុតនៃទឹកផឹកគឺ 1,0-2.0 mEq / l ។
ផលិតផលអាហារត្រូវបានរំលាយយ៉ាងលំបាកនៅក្នុងទឹករឹង, ចាប់តាំងពីការដកកាល់ស្យូមជាមួយប្រូតេអ៊ីនអាហារបង្កើតបានជាសមាសធាតុរលាយ។ តម្លៃអាហារូបត្ថម្ភរបស់ពួកគេត្រូវបានកាត់បន្ថយ។ ការប្រើប្រាស់ទឹករឹងថេរអាចបណ្តាលឱ្យមានការធ្លាក់ចុះនៃអំបិល (urolithiasis) នៅក្នុងខ្លួនមនុស្ស។
តែនិងកាហ្វេត្រូវបានបង្កាត់យ៉ាងលំបាកនៅក្នុងទឹកបែបនេះ។ នៅក្នុងលក្ខខណ្ឌក្នុងស្រុកការលើសនៃអំបិលរឹងនាំឱ្យមានការធ្វើមាត្រដ្ឋាននៃកំដៅនៅក្នុងឡចំហាយទឹកតែបំពង់បំពង់ប្រាក់បញ្ញើអំបិលនៅលើបំពង់បង្ហូរទឹកនិងការបរាជ័យរបស់ពួកគេទុកប្រាក់បញ្ញើនៅលើសក់និងស្បែករបស់មនុស្សបង្កើតអារម្មណ៍មិនរីករាយនៃ "រឹង" របស់ពួកគេ។
ភាពរឹងនៃទឹកដែលត្រូវបានប្រើដើម្បីរៀបចំផលិតផលផ្សេងៗត្រូវបានកំណត់យ៉ាងច្បាស់ហើយមានកម្រិត 0,1-0,2 mEq / l ។
ទម្រង់ទឹករឹងធ្វើមាត្រដ្ឋាននៅលើជញ្ជាំងនៃឡចំហាយកំដៅអាគុយជាដើមដែលធ្វើឱ្យថយចុះយ៉ាងខ្លាំងនូវដំណើរការកម្ដៅរបស់វាកាត់បន្ថយផ្នែកបំពង់បង្ហូរដោយឥតគិតថ្លៃ។
បំពង់បង្ហូរទឹកត្រូវបានពាសពេញដោយមានប្រាក់បញ្ញើខ្នាតយ៉ាងច្រើនដែលផលិតភាពរបស់វាធ្លាក់ចុះច្រើនដង។ ដូច្នេះនៅក្នុងដំណើរការទាំងនោះដែលការប្រើប្រាស់ទឹកជាមួយនឹងបរិមាណអំបិលជាក់លាក់គឺអាចអនុញ្ញាតិបាន, ភាពរឹងរបស់វាត្រូវបានកំណត់ចំពោះតម្លៃទាបសូម្បីតែ - ០.០៣-០.០៥ ម៉ែល / លីត្រ។
ធ្វើមាត្រដ្ឋានលើឧបករណ៍កម្តៅរបស់ម៉ាស៊ីនបោកគក់ធ្វើឱ្យពួកគេមិនមានសណ្តាប់ធ្នាប់។ នៅពេលលាងសម្អាតធ្វើអន្តរកម្មជាមួយសារធាតុសកម្មលើផ្ទៃមុខ (សារធាតុធ្វើឱ្យស្ទះ) នៃសាប៊ូឬសាប៊ូបោកខោអាវអំបិលរឹងរឹងចងវាហើយត្រូវការការប្រើប្រាស់ច្រើន។ ទឹករឹងមិនអាចត្រូវបានប្រើនៅពេលអនុវត្តដំណើរការបច្ចេកវិជ្ជាជាក់លាក់ទេឧទាហរណ៍ក្នុងកំឡុងពេលគូរគំនូរអេឡិចត្រូនិចជាដើម។
ការដកអំបិលចេញ
ដំណើរការនៃការទាញយកអំបិល Ca 2+ និង Mg 2+ ពីទឹកក្នុងការព្យាបាលទឹកត្រូវបានគេហៅថាធ្វើឱ្យទឹកទន់។
ការដកយកចេញនូវជម្រើសនៃអំបិលរឹងពីទឹកអាចត្រូវបានអនុវត្តដោយវិធីសាស្រ្ត៖
- ការព្យាបាលកំដៅ;
- distillation;
- ការបន្ទន់ខ្លួន reagent;
- ត្រជាក់;
- ដំណើរការម៉ាញេទិក;
- ដំណើរការ ultrasonic;
- ការផ្លាស់ប្តូរអ៊ីយ៉ុង;
- osmosis បញ្ច្រាស។
វិធីសាស្ត្រព្យាបាលទឹកក៏ត្រូវបានគេស្គាល់ផងដែរ (ផលប៉ះពាល់អេឡិចត្រូម៉ាញ៉េទិចការបន្ថែមប៉ូប៉ូថេតឬ“ ប្រឆាំងមាត្រដ្ឋាន” ផ្សេងទៀត) ដែលអនុញ្ញាតឱ្យ“ ចង” អំបិលរឹងមួយរយៈដែលរារាំងពួកគេមិនឱ្យធ្លាក់ក្នុងទម្រង់មួយរយៈ។ ទោះជាយ៉ាងណាក៏ដោយវិធីសាស្រ្តទាំងនេះមិនមានជាតិគីមីបន្សាបជាតិអំបិលរឹងទេកុំយកវាចេញហើយដូច្នេះបានរកឃើញថាការប្រើប្រាស់មានកំណត់ក្នុងការព្យាបាលទឹកឧស្សាហកម្ម។
ការបន្ទន់កម្តៅ
តាមរបៀបនេះពួកគេកម្ចាត់ភាពរឹងបណ្តោះអាសន្នដែលបណ្តាលមកពីកាល់ស្យូមនិងម៉ាញ៉េស្យូមប៊ីកកាបូណាត។ នៅពេលដែលទឹកពុះ, អ៊ីដ្រូកាបូនរលាយដើម្បីបង្កើតជារបបទឹកភ្លៀងនៃកាបូនកាបូនមធ្យមឬមូលដ្ឋាន៖
Ca (HCO 3) 2 \u003d CaCO 3 ↓ + CO 2 + H 2 O,
Mg (HCO 3) 2 \u003d Mg 2 (OH) 2 CO 3 ↓ + 3CO 2 + H 2 O ។
ជាលទ្ធផលភាពរឹងរបស់ទឹកត្រូវបានកាត់បន្ថយ។ នោះហើយជាមូលហេតុដែលភាពរឹងរបស់ប៊ីកកាបូណាតត្រូវបានគេហៅថាបណ្តោះអាសន្ន។
ជាមួយនឹងអ៊ីយ៉ុងដែកប្រតិកម្មកាន់តែស្មុគស្មាញដោយសារតែការពិតដែលថា FeCO 3 គឺជាសារធាតុមិនស្ថិតស្ថេរនៅក្នុងទឹក។ នៅក្នុងវត្តមាននៃអុកស៊ីសែនផលិតផលចុងក្រោយនៃខ្សែសង្វាក់ប្រតិកម្មគឺហ្វី (អូអេដ) ៣ ដែលជារបបទឹកភ្លៀងពណ៌ក្រហមងងឹត។ ដូច្នេះជាតិដែកនៅក្នុងទឹកកាន់តែច្រើនពណ៌កាន់តែខ្លាំងនៅជញ្ជីងដែលត្រូវបានដាក់នៅលើជញ្ជាំងនិងបាតនៃនាវាក្នុងពេលពុះ។
ដូច្នេះនៅពេលដែលទឹកក្តៅក្នុងជីវិតប្រចាំថ្ងៃដំណើរការនៃការបន្ទន់ផ្នែករបស់វាក្នុងពេលដំណាលគ្នាកើតឡើង។
Distillation
Distillation គឺជាវិធីសាស្រ្តបែបប្រពៃណីប្រសិទ្ធភាពនិងអាចជឿទុកចិត្តបានដែលផ្តល់នូវកំរិតនៃការបន្សុតទឹកអំបិលដែលមានជាតិប្រៃខ្ពស់និងរឹង។
គោលការណ៍ទូទៅនៃការទទួលបានទឹកដោយវិធីនេះមានដូចខាងក្រោមៈទឹកផឹកដែលបានរៀបចំទុកជាមុនបានចូលទៅក្នុងម៉ាស៊ីនខ្ចប់ដែលមានធាតុផ្សំសំខាន់ៗបីគឺៈហួតធុងទឹកនិងអ្នកប្រមូល។
ហួតជាមួយទឹកត្រូវបានកំដៅឱ្យឆ្អិន។ ចំហាយទឹកចូលក្នុងកុងដង់ដែលជាកន្លែងដែលវាត្រូវបានគេច្របាច់បញ្ចូលគ្នាហើយក្នុងទម្រង់នៃការធ្វើឱ្យមានភាពច្របូកច្របល់ចូលក្នុងអ្នកប្រមូល។ រាល់ភាពមិនបរិសុទ្ធដែលមិនងាយនឹងបង្កជាហេតុនៅក្នុងទឹកប្រភពនៅតែមាននៅក្នុងម៉ាស៊ីនចែកចាយ។
ដើម្បីទទួលបានទឹកបរិសុទ្ធម៉ាស៊ីនបូមទឹកត្រូវបានប្រើដែលខុសគ្នាពីគ្នាទៅវិញទៅមកតាមរបៀបកំដៅផលិតភាពនិងលក្ខណៈរចនា។
វិធីសាស្រ្តនៃការចំលងតែមួយគឺមិនមានលក្ខណៈសន្សំសំចៃទេព្រោះនៅពេលដែលវាត្រូវបានគេប្រើថាមពលខ្ពស់សម្រាប់កំដៅនិងហួត (ប្រហែល ៣០០០ គីជេក្នុង ១ គីឡូក្រាម) ក៏ដូចជាការប្រើប្រាស់ទឹកសម្រាប់ចំហាយទឹក (ប្រហែល ៨ លីត្រទឹក ១ គីឡូក្រាមនៃចំហាយទឹក) ។ ដូច្ន្រះការប្រើឡចំហាយតែមួយគឺគួរឱ្រយប្រើប្រស់ទឹកទាប - 10-20 លី / ម៉។
មានប្រសិទ្ធិភាពនិងសន្សំសំចៃជាងការបំប្លែងធម្មតាគឺម៉ាស៊ីនចំរុះចំរុះដែលមានសមត្ថភាពខ្ពស់។ ប៉ុន្តែវាមានតម្លៃថ្លៃណាស់លើសពីនេះទៀតថ្លៃដើមនៃការព្យាបាលមុនទឹកសម្រាប់ពួកគេគឺខ្ពស់។
គួរកត់សំគាល់ថាវិធីសាស្រ្តបំប្លែងយកអំបិលដែលរលាយទាំងអស់ចេញពីក្នុងប្រភពទឹក។
ពាក្យស្នើសុំឡើងវិញ
មានការបន្ទន់ទឹកដោយការច្របាច់សូដានិងការដាក់សូដា - សូដ្យូមនៃការបន្ទន់ទឹក។
នៅពេលដែលកំណត់ការខាប់ជាតិកំបោរ Ca (OH) ២ ត្រូវបានបន្ថែមទៅក្នុងដំណោះស្រាយទៅនឹងកំរិត pH ប្រហែល ១០ ។
Ca (HCO 3) 2 + Ca (OH) 2 \u003d 2 CaCO 3 + 2H 2 O,
Mg (HCO 3) 2 + 2Ca (OH) 2 \u003d Mg (OH) 2 + 2СaCO 3 + 2Н 2 O ។
វិធីសាស្រ្តនេះត្រូវបានប្រើសម្រាប់ទឹករឹងនិងកាបូនដែលមិនមានជាតិកាបូនទាបនៅពេលមានការថយចុះដំណាលគ្នានៃភាពរឹងនិងអាល់កាឡាំង។ ភាពរឹងដែលនៅសល់គឺ 0,4-0,8 mEq / L ខ្ពស់ជាងភាពរឹងដែលមិនមែនជាកាបូន។
នៅពេលដែលកំបោរសូដាត្រូវបានបន្ថែមកំបោរ Ca (OH) 2 និងសូដា Na 2 CO 3 ត្រូវបានបន្ថែមទៅក្នុងទឹកក្នុងកំរិតប្រមាណ ១០។ ជាលទ្ធផលប្រតិកម្មដូចខាងក្រោមកើតឡើង៖
Ca (HCO 3) 2 + Ca (OH) 2 + Na 2 CO 3 \u003d 2 CaCO 3 + 2NaOH + H 2 CO 3,
Mg (HCO 3) 2 + 2NaOH \u003d Mg (OH) 2 + 2NaHCO ៣ ។
ដូចខាងក្រោមពីសមីការប្រតិកម្មនៅក្នុងដំណើរការនៃការបង្កើតនិងការជ្រាបនៃដីល្បាប់ពីទឹកអំបិលរឹងត្រូវបានស្រង់ចេញ។ រួមគ្នាជាមួយពួកគេភាគល្អិតចម្រុះពណ៌និងផ្អាកជាមួយនឹងការបំពុលដែលជាប់ទាក់ទងត្រូវបានដកចេញ។ ដីល្បាប់សរីរាង្គត្រូវបានរំខានដោយផ្នែកនៃដីល្បាប់។
ជាមួយនឹងការកំនត់សូដាដោយសារតែការហួសកំរិតនៃ HCO 3 អ៊ីញភាពពេញលេញកាន់តែច្រើននៃការដកអំបិលរឹងចេញពីទឹកត្រូវបានសម្រេច។ ការបង្កើនសីតុណ្ហភាពដល់ 70-80 អង្សាសេអនុញ្ញាតឱ្យអ្នកនាំយកភាពរឹងដែលនៅសល់ដល់ 0.35-1.0 mEq / L ។ លទ្ធផលដូចគ្នាអាចសម្រេចបានដោយការបង្កើនកម្រិតថ្នាំ។
វិធីសាស្ត្រសូដាសូដា
ការបន្ថែមសូដាគឺចាំបាច់ប្រសិនបើភាពរឹងដែលមិនមែនជាកាបូនគឺធំជាងកាបូន។ ប្រសិនបើប៉ារ៉ាម៉ែត្រទាំងនេះស្មើគ្នានោះការបន្ថែមសូដាប្រហែលជាមិនចាំបាច់ទាល់តែសោះ។
អ៊ីដ្រូកាបូននៃកាល់ស្យូមនិងម៉ាញ៉េស្យូមក្នុងប្រតិកម្មជាមួយអាល់កាលីបង្កើតជាសមាសធាតុរលាយមិនល្អនៃកាល់ស្យូមនិងម៉ាញ៉េស្យូមសូដាទឹកនិងកាបូនឌីអុកស៊ីត៖
Ca (HCO 3) 2 + 2NaOH \u003d CaCO 3 ↓ + Na 2 CO 3 + 2H 2 O,
Mg (HCO 3) 2 + 2NaOH \u003d Mg (OH) 2 ↓ + Na 2 CO 3 + H 2 O + CO 2 ។
កាបូនឌីអុកស៊ីតបង្កើតឡើងជាលទ្ធផលនៃប្រតិកម្មនៃកាបូនអ៊ីដ្រូសែនម៉ាញ៉េស្យូមជាមួយអាល់កាឡាំងប្រតិកម្មម្តងទៀតជាមួយអាល់កាលីបង្កើតសូដានិងទឹក៖
CO 2 + NaOH \u003d Na 2 CO 3 + H 2 O ។
ភាពរឹងដែលមិនមែនជាកាបូន
ស៊ុលហ្វាតនិងកាល់ស្យូមក្លរួមានប្រតិកម្មជាមួយសូដាដែលបានបង្កើតឡើងនៅក្នុងប្រតិកម្មនៃភាពរឹងកាបូននិងអាល់កាឡាំងនិងបន្ថែមសូដាដើម្បីបង្កើតជាកាបូនកាល់ស្យូមដែលមិនជាប់នឹងលក្ខខណ្ឌអាល់កាឡាំង។
CaCl 2 + Na 2 CO 3 \u003d CaCO 3 ↓ + 2NaCl,
CaSO 4 + Na 2 CO 3 \u003d CaCO 3 ↓ + Na 2 SO 4 ។
ម៉ាញ៉េស្យូមស៊ុលហ្វាតនិងក្លរីតមានប្រតិកម្មជាមួយអាល់កាឡាំងដើម្បីបង្កើតម៉ាញ៉េស្យូមអ៊ីដ្រូសែនអ៊ីដ្រូអ៊ីដ។
MgSO 4 + 2NaOH \u003d Mg (OH) 2 ↓ + Na 2 SO 4,
MgCl 2 + 2NaOH \u003d Mg (OH) 2 ↓ + 2NaCl ។
ដោយសារតែការពិតដែលថានៅក្នុងប្រតិកម្មនៃកាលីកាបូណាតជាមួយអាល់កាលីសសូដាត្រូវបានបង្កើតឡើងដែលមានប្រតិកម្មជាបន្តបន្ទាប់ជាមួយនឹងភាពរឹងដែលមិនមានជាតិកាបូនបរិមាណរបស់វាត្រូវតែទាក់ទងគ្នារវាងសមាមាត្រនៃកាបូណាត (LFA) និងភាពរឹងដែលមិនមែនជាកាបូន (LFA)៖
- ប្រសិនបើពួកគេស្មើគ្នាសូដាអាចត្រូវបានលុបចោល។
- នៅក្រោមលក្ខខណ្ឌ Lc\u003e Lnc ការលើសនៃសូដាត្រូវបានបង្កើតឡើង។
- ជាមួយសមាមាត្រនៃ LCD< Жнк - недостаток соды и ее необходимо добавлять.
ដំណើរការនៃការដាក់ប្រាក់ត្រូវបានអនុវត្តនៅក្នុងធុង sedimentation និងការបំភ្លឺជាមួយស្រទាប់ sediment ដែលបានផ្អាក។
ធុង sedimentation មិនមានប្រសិទ្ធភាពហើយ pulp hydroxide ដែលទទួលបាននៅក្នុងនោះមានសំណើមខ្ពស់ ៩៧-៩៩% ។ ដូច្នេះបច្ចុប្បន្ននេះពួកគេមិនត្រូវបានប្រើទេ។
នៅក្នុងការអនុវត្តជាក់ស្តែងការបកស្រាយខុសៗគ្នាជាមួយនឹងស្រទាប់ដីល្បាប់ដែលត្រូវបានផ្អាកត្រូវបានប្រើ។ នៅក្នុងពួកគេដំណោះស្រាយដែលត្រូវបានបន្សុតត្រូវបានផ្គត់ផ្គង់ពីខាងក្រោមហើយឆ្លងកាត់ស្រទាប់ដីល្បាប់។ នេះបង្កើនមេគុណនៃការបន្សុតទឹក។
វិធីសាស្រ្ត Reagent មិនត្រូវបានប្រើក្នុងការរៀបចំទឹកផឹកទេ។ បន្ទាប់ពីពួកគេទឹកមានប្រតិកម្មអាល់កាឡាំងយ៉ាងខ្លាំង។ ហេតុដូច្នេះសារធាតុរំងាស់ត្រូវបានគេប្រើយ៉ាងទូលំទូលាយនៅក្នុងថាមពលនិងឧស្សាហកម្មដែលជាដំណាក់កាលដំបូងនៃការបន្សុតទៅតម្រងមេកានិច។ នៅពេលធ្វើការជាមួយគ្នាពួកគេអនុញ្ញាតឱ្យអ្នកធ្វើឱ្យទឹកទន់យកសារធាតុរាវដែលផ្អាករួមទាំងកូឡាជែននិងបន្សុទ្ធទឹកខ្លះពីសារធាតុសរីរាង្គ។
ត្រជាក់
ដើម្បីទប់ទល់នឹងភាពរឹងនៃទឹកថេរវិធីសាស្ត្រដូចជាទឹកកកត្រជាក់ត្រូវបានប្រើ។ ដើម្បីធ្វើដូចនេះអ្នកគ្រាន់តែត្រូវការបង្កកទឹកបន្តិចម្តង ៗ ។ នៅពេលប្រមាណ ១០% នៃអង្គធាតុរាវនៅសល់ពីបរិមាណដំបូងវាចាំបាច់ត្រូវបង្ហូរទឹកដែលមិនកកហើយបង្វែរទឹកកកទៅជាទឹកវិញ។ អំបិលទាំងអស់ដែលបង្កើតបានជារឹងនៅតែស្ថិតក្នុងទឹកមិនកក។
ទន្ទឹមនឹងការច្របាច់បញ្ចូលគ្នាក្នុងពេលតែមួយវិធីមួយក្នុងការធ្វើឱ្យទឹកប្រៃឡើងខ្ពស់ដល់គុណភាពដែលអាចធ្វើទៅបាន។
វិធីសាស្រ្តផ្សេងទៀត
វិធីសាស្រ្តអេឡិចត្រូតគឺផ្អែកលើបាតុភូតនៃចលនាដឹកនាំអ៊ីយ៉ុងអេឡិចត្រូលីតទៅនឹងអេឡិចត្រូតដែលភ្ជាប់ទៅបណ្តាញចរន្តផ្ទាល់។ ដូច្នេះអ៊ីយ៉ុងដែកដែលកំណត់ពីភាពរឹងនៃទឹកត្រូវបានជាប់នៅអេឡិចត្រូតហើយត្រូវបានបំបែកចេញពីទឹកបន្សល់ទុកនូវបរិក្ខាព្យាបាលទឹក។
វិធីសាស្រ្តអ៊ីយ៉ូដម៉ាញេទិកក៏ប្រើបាតុភូតនៃចលនាអ៊ីយ៉ុងដែលបានដឹកនាំប៉ុន្តែស្ថិតនៅក្រោមឥទ្ធិពលនៃដែនម៉ាញេទិក។ ដើម្បីបង្កើនចំនួនអ៊ីយ៉ុងនៅក្នុងទឹកវាត្រូវបានធ្វើឱ្យមានការរំខានជាមុនជាមួយវិទ្យុសកម្មអ៊ីយ៉ូដ។
ការព្យាបាលម៉ាញេទិកនៃទឹកមាននៅក្នុងការឆ្លងកាត់ទឹកតាមរយៈប្រព័ន្ធនៃដែនម៉ាញេទិកនៃទិសដៅផ្ទុយ។ ជាលទ្ធផលនៃការនេះមានការថយចុះនៃកំរិតជាតិទឹកនៃសារធាតុដែលបានរំលាយនិងការរួមផ្សំរបស់វាទៅជាភាគធំ ៗ ដែលមានទឹកភ្លៀង។
ការព្យាបាលទឹក Ultrasonic ក៏នាំទៅរកការបង្កើតភាគល្អិតធំ ៗ នៃសារធាតុរំលាយជាមួយនឹងការបង្កើតដីល្បាប់។
គួរពិចារណាវិធីសាស្រ្តនៃការផ្លាស់ប្តូរអ៊ីយ៉ុងនិងដំណើរការបញ្ច្រាស់អេកូស្យូមឱ្យបានលំអិតនៅក្នុងផ្នែកទី ២ នៃអត្ថបទដែលយើងនឹងចុះផ្សាយនៅក្នុងទិនានុប្បវត្តិរបស់យើងនៅអត្ថបទបន្ទាប់។
