Condizioni di occorrenza, metodi di rilevazione e metodi per prevenire la tendenza alla corrosione intergranulare dei giunti saldati di acciai ad alta lega
Pagina 1
Corrosione intergranulare acciai inossidabili il più delle volte si manifesta in ambienti con proprietà ossidanti.
La corrosione intergranulare degli acciai inossidabili può anche essere rilevata elettrochimicamente - mediante attacco anodico per 5 minuti a una densità di corrente di 0 65 a / cm2 e 20 10 C in una soluzione al 60% di acido solforico con urotropina allo 0 5% o altro inibitore di corrosione. Il metodo di attacco anodico, che consiste nella polarizzazione anodica della sezione studiata della superficie dell'acciaio, ha il vantaggio di consentire di determinare rapidamente (1 5 - 5 min) la tendenza dell'acciaio alla corrosione intergranulare direttamente sui prodotti semifiniti e saldati finiti. L'applicazione di questo metodo consente di eseguire un test interoperatorio della tendenza del metallo alla corrosione intergranulare e di eliminare questa tendenza mediante un adeguato trattamento termico.
Molto spesso, la corrosione intergranulare degli acciai inossidabili è associata alla precipitazione dei carburi di cromo a temperature di rinvenimento lungo i confini del grano, a seguito della quale la concentrazione di cromo in una soluzione solida vicino ai carburi diminuisce drasticamente.
Molto spesso, la corrosione intergranulare degli acciai inossidabili è associata alla precipitazione dei carburi di cromo durante la tempra ai bordi del grano, a seguito della quale la concentrazione di cromo in una soluzione solida vicino ai carburi diminuisce drasticamente.
La causa della corrosione intergranulare degli acciai inossidabili è la precipitazione dei carburi di cromo Cr23C6 o (Cr, Fe) 2cC al limite del grano quando riscaldati nell'intervallo di temperatura 450 - 850 C. Poiché a queste temperature il tasso di diffusione del carbonio è superiore a quello del cromo, nella formazione di carburi lungo il confine del grano che richiede è coinvolta tutta la lega di carbonio, mentre il cromo si trova solo al limite del grano. Ciò porta ad un esaurimento del confine del grano con cromo e una diminuzione della capacità di passare in uno stato passivo. Pertanto, in un ambiente corrosivo, il confine del grano si dissolve.
La natura della corrosione intergranulare degli acciai inossidabili è attualmente insufficientemente studiata e le teorie esistenti non spiegano sempre la loro suscettibilità alla corrosione intergranulare.
Per eliminare la corrosione intergranulare degli acciai inossidabili, è necessario prevenire la precipitazione dei carburi di cromo lungo il confine del grano. Ciò si ottiene riducendo il contenuto di carbonio nell'acciaio; acciai legati con elementi che formano carburo (titanio, tantalio, niobio), formando carburi più insolubili dei carburi di cromo; condurre trattamenti termici in condizioni che impediscono la formazione di carburi di cromo.
| L'effetto della concentrazione di vanadato sul tasso di corrosione dell'acciaio 1X18H9T nelle soluzioni HN03 a 100 C. | L'effetto della temperatura sul tasso di corrosione dell'acciaio 1X18H9T nelle soluzioni HN03 contenenti 1% VOj. |
La corrosione intergranulare (MCC) è considerata una delle opzioni più pericolose per la distruzione del metallo a causa del fatto che nella maggior parte dei casi non può essere determinato visivamente.
1
Per tipo di corrosione descritto si intende la distruzione dei metalli osservata, di regola, lungo i confini dei cristalli (altrimenti sono chiamati grani). Ciò porta al fatto che il materiale perde capacità di resistenza e duttilità. IWC è una forma di corrosione locale. Di solito influisce negativamente su leghe e metalli che sono soggetti a passività. Questi includono acciai inossidabili (cromo e cromo-nichel), composizioni a base di nichel, alluminio.
La corrosione intergranulare è dovuta alla delaminazione della soluzione solida, che porta alla comparsa di fasi speciali lungo i confini del grano in cui vi è una quantità eccessiva di uno o un altro elemento della lega metallica. Inoltre, nelle aree adiacenti ai confini dei cristalli, il volume di tale elemento è minimo. Sotto l'influenza di un certo mezzo con caratteristiche aggressive, si osserva la dissoluzione di aree esaurite o arricchite sugli anodi.
Corrosione intergranulare
In effetti, l'MCC, come si può vedere dalla descrizione del suo meccanismo, è una reazione elettrochimica che porta alla rapida distruzione di strutture e prodotti metallici. Molto spesso, questo si osserva in leghe con un alto contenuto di cromo. In ambienti con un alto indice di ossidazione, la corrosione da noi descritta è causata dal fatto che le fasi sature si dissolvono secondo il principio selettivo. Nelle situazioni in cui vi sono additivi leganti nelle fasi (rame, vanadio, molibdeno, manganese, tungsteno), il processo di dissoluzione è accelerato.
I principali fattori dell'IWC sono i seguenti:
- alta temperatura del mezzo e periodo di trattenimento del metallo al suo interno;
- la presenza di additivi leganti nella lega, che sono soggetti a passivazione;
- aggressività dell'ambiente operativo.
La frattura intergranulare può avere una velocità diversa. Dipende dal potenziale specifico del metallo. Tipicamente, l'accelerazione del decorso del MCC è fissata ai seguenti valori: 0,35 V (potenziale del cosiddetto movimento attivo-passivo); Da 1,15 a 1,25 V (zona passiva).
2
I MCC sono altamente sensibili alle leghe di duralluminio. Il meccanismo della loro distruzione è il seguente. Ai confini dei cristalli, CuAl2, un composto intermetallico, precipita. Viene distrutto, mentre si osserva l'evoluzione dell'idrogeno. Non vi è alcun film protettivo su questo composto intermetallico (a causa dell'assenza di una sostanza ossidante nella soluzione), quindi si dissolve abbastanza rapidamente.
Nella maggior parte dei casi, si osserva corrosione intergranulare dei prodotti in duralluminio nelle aree in cui sono presenti pori microscopici e piccole crepe. Meno comunemente, la distruzione inizia ai box. Si formano tra i confini dei cristalli. In questo caso, lo sviluppo della corrosione è facilitato dal fatto che si nota una certa acidificazione dell'elettrolita all'interno della vaiolatura. Per questi motivi, i prodotti in duralluminio (come molte altre leghe a base di alluminio), è auspicabile proteggere dalla distruzione compattandone la struttura.

Prodotto durale MK
Un tipo comune di MCC è la corrosione del coltello. Si nota su giunti saldati. La distruzione del coltello è considerata locale, si verifica tra la cucitura e il metallo di base. Nella maggior parte dei casi, i giunti saldati sono soggetti a tale distruzione: leghe con un alto contenuto di molibdeno; composizioni metalliche a cui è stato aggiunto il titanio; acciai ad alto tenore di carbonio-nichel.
Durante la saldatura di tali leghe, si verifica l'interazione del metallo freddo e riscaldato a 1300 °. In questo caso, i carburi di titanio o di cromo si dissolvono nel fuso. Quando quest'ultimo si raffredda, non si formano nuovi carburi, il carbonio rimane nella fase solida e si osserva la precipitazione dei carburi di cromo (in quantità molto grandi). Se l'atmosfera in cui si verificano tali processi è aggressiva, si osserva la dissoluzione (graduale) degli elementi che entrano nella lega su una sezione stretta del giunto saldato a livello intergranulare.
Il danneggiamento del coltello può essere prevenuto con i seguenti metodi:
- evitare calore eccessivo nella sezione vicino alla saldatura durante la saldatura;
- utilizzare solo composizioni a basso contenuto di carbonio di cromo-nichel;
- applicare una ricottura speciale (si chiama stabilizzazione), in cui i carburi di cromo passano nella soluzione solida.
3
Resistenza al MCC austenitico-ferritico, austenitico, austenitico-martensitico, ferritico e altri acciai resistenti alla corrosione, nonché a metallo depositato e giunti saldati Le leghe specificate sono determinate in conformità con GOST 6032. Dal 2005 opera nei paesi della CSI.
I seguenti metodi di prova per la corrosione intergranulare esistono in conformità con questo standard:
- AMU. Le analisi vengono eseguite in presenza di rame (metallico) in una soluzione di solfato di rame e acido solforico.
- AMUF. La tecnica è simile alla prima, ma prevede la presenza non solo di rame (metallo), ma anche di fluoruro di potassio o sodio.
- VU. Prove su acido solforico in presenza di ossido di ferro solfato.
- Controllo. I campioni vengono analizzati per la resistenza alla corrosione in acido nitrico (65%).

Analisi del campione per resistenza alla corrosione in acido nitrico
Inoltre, in alcuni casi, i test vengono eseguiti in una composizione costituita da polvere di zinco e acido solforico. Inoltre viene utilizzata la tecnica di attacco di metalli (anodici) in acido solforico inibito. Inoltre considereremo tutte queste tecniche in modo più dettagliato. Ma prima, parliamo di come preparare i campioni per i test di resistenza all'IWC. Gli spazi vuoti per loro sono tagliati da:
- regione assiale di prodotti lunghi;
- sezioni di superficie in lamiera d'acciaio;
- regione assiale di billette a tubo e;
- corpo o pezzi dimenticati;
- zona assiale del metallo saldato;
- superfici di metallo saldato.
Gli spazi vuoti devono avere tali parametri geometrici che consentano di preparare il numero di campioni richiesti dalle condizioni di prova. Quest'ultimo può essere piatto, anulare, segmentato, sotto forma di tubi, cilindrico. I campioni secondo GOST sono realizzati da uno strato di rivestimento, ma solo dopo che gli strati di transizione e principali sono stati completamente rimossi dal prodotto.
Le leghe non stabilizzate in cui vi è un massimo dello 0,03% di carbonio, le composizioni con niobio e titanio come additivi e anche gli acciai stabilizzati dovrebbero essere testate su preforme che hanno subito una procedura di preriscaldamento (i professionisti lo chiamano provocatorio). La procedura di prova specifica è selezionata per diversi indicatori. Di solito, vengono presi in considerazione lo scopo operativo della lega e la sua composizione chimica.
4
La corrosione intergranulare colpisce più spesso tali leghe: 03X17H14M3, 03X18H12, 08X21H6M2T, 08X17T, 06X18H11, 01X25TBYU-VI, 08X18H10, 09X16H15M3B, 15X25T, 12X18H18H12, 18X18H18H12, 18X18H18H18, 18X18 .
I prodotti e i disegni da essi analizzati sono analizzati per la resistenza alla frattura intergranulare secondo i metodi AMU e AMUF. Queste tecniche sono essenzialmente le stesse. La seconda è una versione accelerata dei test AMU. L'analisi dei campioni utilizzando tali tecnologie consiste nell'immergere le preforme in soluzioni preparate (ne abbiamo indicato la composizione sopra) e conservarle per un certo tempo.

Immersione di un metallo in una soluzione acida
Successivamente, i campioni vengono prelevati e piegati a 85–95 ° nella forma della lettera Z. Quindi la presenza di corrosione viene determinata usando una lente d'ingrandimento o utilizzando una speciale tecnologia metallografica. Se, quando si esaminano i campioni sotto una lente d'ingrandimento (aumento di 7-12 volte), sui pezzi non sono visibili crepe, ciò significa che i prodotti hanno la resistenza necessaria alla frattura intercristallina. Nota: è consentita la presenza di microcricche sui bordi dei pezzi.
La tecnica metallografica viene utilizzata in situazioni in cui i campioni non possono piegarsi all'angolo richiesto a causa dei loro piccoli parametri geometrici. Con questo controllo, dal pezzo viene tagliata una sezione sottile di circa 2 cm. Presta attenzione! In questo caso, il piano di taglio rispetto alla superficie del pezzo deve essere perpendicolare. La sezione sottile viene quindi incisa e analizzata con ingrandimento di 200 × (usando un microscopio).
Se il campione durante tale controllo indica la distruzione dei confini dei cristalli metallici con una profondità non superiore a 30 micron, il pezzo viene considerato resistente alla corrosione. Altrimenti (la profondità della distruzione è maggiore), si parla della tendenza della lega a MKC.
5
Per verificare la resistenza al MKC degli acciai 02X25H22AM2, 03X17H14M3, 03X18H1102X18H11, 03X24H6AM3 e 03X18H12, viene utilizzato il metodo DU. L'analisi viene eseguita come segue:
- sgrassare i campioni (si utilizza solvente organico), immergerli in acqua distillata, asciugare, pesare;
- posizionare i pezzi grezzi lavorati in un pallone di vetro con un condensatore a riflusso (le barche di porcellana o le perle di vetro sono pre-posizionate sul fondo del contenitore);
- versare i campioni con acido nitrico (65%), che dovrebbe coprire il prodotto di 1,5 cm;
- portare a ebollizione la soluzione.
La durata totale di tale controllo è di 5 cicli di 48 ore ciascuno. Per tutto questo tempo, i pezzi sono in acido, che bolle uniformemente (senza evoluzione di ossidi ed evaporazione). Quindi i campioni vengono rimossi e valutati per la suscettibilità alla corrosione secondo il metodo metallografico precedentemente descritto.
Vuoto in metallo acido
La tecnologia VU viene utilizzata per analizzare i prodotti delle leghe KhN30MDB, 06KhN28MDT, 03Kh21N21M4GB e 03KhN28MDT. Con questo test, i campioni vengono fatti bollire per 48 ore in acido solforico, quindi i risultati vengono valutati con il metodo AMU. I test che utilizzano polvere di zinco e acido solforico (metodo B) sono considerati un analogo meno affidabile della tecnologia VU. I campioni in questa analisi vengono conservati in soluzione bollente per 144 ore.
Spesso, metallo che sono testati per la resistenza a MCC tecnologia AMU e AMUF precedentemente analizzati mediante il metodo B. È comunemente usato per l'analisi di parti reso flessibile, caldo stampaggio o saldatura di leghe 12H18N12T, 03H18N11, 08H18N10, 12X18H9T, 08H18N12T, 12H18N9, 06H18N11 , 12X18H10T e 04X18H10.
Il test secondo il metodo B viene eseguito su un'installazione speciale costituita da un catodo (un recipiente di piombo svolge la sua funzione), una sorgente di corrente (costante), un reostato e un amperometro. Aggiungiamo che tale analisi non viene eseguita per il metallo saldato.
L'importanza degli studi sulla resistenza ai MCC non sta solo nello stabilire la durata del funzionamento di prodotti di un particolare grado di acciaio, ma anche nel determinare con precisione il meccanismo di frattura intergranulare. Pertanto, tali test ricevono sempre maggiore attenzione. Dopotutto, ti permettono di sviluppare nuovi metodi.
Il processo di corrosione intergranulare di metalli solidi in un mezzo di metallo liquido non è stato studiato in modo specifico. Di seguito sono riportati alcuni dei probabili meccanismi di questo processo, la cui esistenza è confermata da osservazioni sperimentali indirette.
1. Uno dei motivi della corrosione intergranulare è un livello di energia potenziale più elevato di atomi situati in zone intergranulari, rispetto agli atomi all'interno dei cristalliti. Di conseguenza, l'energia di attivazione della dissoluzione per questi atomi è inferiore rispetto al resto. Di conseguenza, la probabilità del loro rilascio nella soluzione aumenta. In precedenza era stato dimostrato che la costante della velocità di dissoluzione per il processo controllato dal primo stadio è α \u003d ωtρ "/ n∞. Pertanto, un aumento della probabilità di rilascio nella soluzione di metallo liquido per gli atomi delle zone intergranulari significa che la velocità di dissoluzione di queste sezioni della struttura metallica è superiore alla velocità Di conseguenza, il fronte di corrosione nelle condizioni di dissoluzione isotermica e non isotermica si approfondirà lungo i bordi del grano del metallo, cioè si verificherà una corrosione intergranulare. . Dissoluzione di bordo di grano è così grande che la matrice è separato da cereali integrali esempio pesante frattura intergranulare è il nichel corrosione in litio liquido a 1000 ° C, la microstruttura del metallo è caratteristico per questo caso è illustrato nella Figura 42 ..
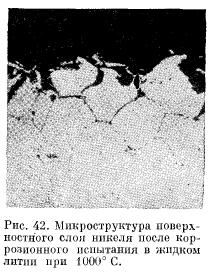
Stimiamo la profondità della corrosione intergranulare di un metallo causata dalla differenza nei tassi di dissoluzione degli atomi dal corpo del grano e dalle zone intergranulari. Per la dissoluzione isotermica, in questo caso, il numero di atomi che passano nella soluzione di metallo liquido per unità di tempo è determinato da una dipendenza simile all'equazione (1):
dove l'indice "z" indica che la caratteristica corrispondente si riferisce alla dissoluzione dalla superficie del grano e l'indice "g" si riferisce alla dissoluzione dalla zona intergranulare. Considerando, come prima, che N-nVж, otteniamo l'equazione differenziale
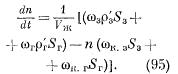
Risolvendo l'equazione (95) e usando la condizione iniziale: t \u003d 0, n \u003d 0 e il rapporto di saturazione dn / dt \u003d 0, troviamo l'equazione cinetica per la dissoluzione isotermica tenendo conto dell'influenza delle zone intergranulari nella seguente forma:
Per determinare la profondità della corrosione generale (lz) e intergranulare (lg), scriviamo l'equazione differenziale
dove ρз e ρг sono rispettivamente la densità apparente dei cristalliti e delle zone intergranulari. Otteniamo una soluzione a questa equazione usando l'uguaglianza (96) e la condizione iniziale t \u003d 0, lz \u003d 0, lg \u003d 0:
Al fine di ottenere il rapporto tra la profondità della corrosione intergranulare e quella generale, scriviamo la seguente espressione approssimativa per quest'ultima:
dove il simbolo a indica, come prima, la costante del tasso di dissoluzione pari a ωt * ρ "/ n∞, e nг∞ è quella parte della concentrazione della soluzione che si ottiene dissolvendo il metallo delle zone intergranulari. Sottraendo (99) da (98), troviamo :
Dividiamo l'equazione (100) per (99), trascurando il secondo termine sul lato destro dell'equazione (99), che è ovviamente molto più piccolo del primo. Quindi otteniamo il rapporto desiderato nel modulo
Dall'equazione (101) segue che la corrosione intergranulare aumenta con il tempo.
Di grande interesse è il valore massimo del rapporto lg / lz, che si ottiene entro la fine del processo di dissoluzione. Da (101) troviamo che quando la soluzione è satura, cioè come t → ∞, questo rapporto è
Il valore (lg / lz) max può essere stimato come segue. In una prima approssimazione, possiamo supporre che nг∞ / n∞≈αgSg / αзSз; inoltre, tenendo conto che α \u003d ω * ρ "/ n∞ e ρ" \u003d α * ρ, dove α è la distanza interatomica, otteniamo (lg / lz) max≈ωg / ωz. La probabilità della transizione di una soluzione di atomi dalla superficie del grano è espressa dalla dipendenza ωz \u003d v exp (-Qp / RT). A causa del fatto che l'energia di attivazione della dissoluzione dalle zone intergranulari è inferiore a quella del corpo dei cristalliti per la quantità della loro energia in eccesso ΔQg, la probabilità di transizione degli atomi da questi siti alla soluzione sarà ωg \u003d v * exp [- (Qр-ΔQg) / RT] Usando queste espressioni, otteniamo (lg / lz) max ≈ exp (ΔQg / RT).
Stimeremo numericamente il rapporto tra la profondità della corrosione intergranulare e il totale del ferro γ. Il valore medio dell'energia libera dei confini del grano in lui, secondo il lavoro, è 8040 cal / g * atomo. Detto questo, scopriamo che a una temperatura di 800 ° C il rapporto (lg / lz) massimo è di circa 40. Pertanto, la profondità della corrosione intergranulare nel ferro può essere quasi 40 volte la profondità della corrosione generale. Va notato, tuttavia, che con un significativo approfondimento del fronte di corrosione lungo i confini del grano, il processo di dissoluzione sarà ostacolato dalla diffusione degli atomi disciolti attraverso il metallo liquido nel canale stretto e lungo formato, che può essere considerato un aumento dello spessore del film perimetrale in questa regione. Un tale processo, ovviamente, limiterà la profondità della corrosione intergranulare.
Il rapporto tra la profondità della corrosione intergranulare e la profondità della corrosione generale durante il trasferimento di massa termica può essere ottenuto usando l'equazione del trasferimento di massa nella forma
dove Δt è il tempo di transito della zona calda per il flusso di metallo liquido. Poiché il peso del metallo trasferito nella zona fredda nel tempo t è ΔP \u003d S * Rpm * t, dove S è la superficie da cui si verifica la dissoluzione nella zona calda, quindi sulla base dell'uguaglianza (103) si ottiene
Passiamo ora alla Fig. 43, che mostra la cinetica della dissoluzione del metallo dei cristalliti e delle zone intergranulari. Si può vedere dagli schemi che le concentrazioni iniziali (ϗ * nн∞ + nк) e finali (nв) della soluzione nella zona calda sono le stesse per i cristalliti e le zone intercristalline, ma il valore Δt è diverso per loro, che è associato a un diverso valore di αg e αz . Tenendo presente che anche l'area di queste sezioni strutturali differisce, che ΔP \u003d ρSl, e usando il rapporto di beca del metallo disciolto dalle zone intercristallite e dai cristalliti, troviamo
Poiché ρз≥ρg e Δtз≥Δtg, lg / lз≥1, cioè la corrosione intergranulare si verifica anche in condizioni di trasferimento di massa termica. Se nv è significativamente inferiore a nv∞, allora possiamo usare l'uguaglianza approssimativa Δtg / Δtz \u003d αz / αg (vedi Fig. 43). Sulla base dell'ultima relazione, l'equazione (105) assume la forma lg / lz≈ρz / ρg * αg / αz. Pertanto, l'intensità della corrosione intergranulare in questo caso è determinata dal rapporto tra le costanti della velocità di dissoluzione del metallo delle zone intergranulari e i cristalliti. È interessante notare che la velocità di distruzione del metallo lungo i confini dei cristalliti durante il trasferimento di massa termica è pari al valore massimo del rapporto lg / lz durante la dissoluzione isotermica. Pertanto, è possibile utilizzare la valutazione precedentemente effettuata di questo rapporto, da cui consegue che la profondità della corrosione intergranulare, ad esempio il ferro a 800 ° C, può essere circa 40 volte la profondità della corrosione generale. Allo stesso tempo, va sottolineato che se l'intensità (lg / lz) della corrosione intergranulare cambia poco nel tempo, allora la differenza tra la profondità della corrosione intergranulare e generale aumenta continuamente. Quindi, la profondità della corrosione generale in condizioni di trasferimento di massa è determinata dall'equazione
e la profondità di corrosione intergranulare per il caso sopra considerato è uguale a
da cui segue
Pertanto, in questo caso, la differenza tra la profondità della corrosione intergranulare e generale aumenta con il tempo secondo una legge lineare. Tuttavia, tale sviluppo della corrosione intergranulare non può essere illimitato. Come già indicato, la massima profondità di corrosione intergranulare è determinata dal momento della transizione al controllo del processo di dissoluzione nei canali formati da cristalliti vicini da un meccanismo di diffusione.
La distruzione dei confini del grano dovuta all'aumentata energia degli atomi situati qui può verificarsi durante la dissoluzione, nonché in condizioni isotermiche quando la soluzione raggiunge la saturazione. In quest'ultimo caso, la corrosione sarà effettuata mediante trasferimento di energia della massa. Questo a volte spiega l'effetto dei metalli liquidi sui metalli solidi durante i test isotermici di lunga durata, sebbene la soluzione abbia da tempo raggiunto la concentrazione di equilibrio.
Va notato che il trasferimento di energia della massa è di natura locale e copre solo piccole aree della superficie. Questa caratteristica è spiegata dal fatto che la forza motrice del trasferimento è il gradiente di energia dU / dx, dove x è la distanza lungo la superficie. metallo. Il processo di trasferimento di energia della massa è un insieme di processi di dissoluzione, diffusione nel film superficiale di metallo liquido e cristallizzazione. La velocità di diffusione in questo caso è determinata da un'equazione simile a (78):
dove D è il coefficiente di diffusione nel metallo liquido; S è l'area superficiale attraverso la quale si verifica la diffusione; f è il coefficiente di proporzionalità. Ovviamente, con una distanza sufficientemente ampia tra regioni con diverse energie atomiche, il gradiente di energia sarà piccolo e la velocità di diffusione sarà trascurabile. Di conseguenza, il processo di trasferimento tra queste sezioni non si verificherà praticamente.
2. La corrosione intergranulare delle leghe può essere associata a corrosione selettiva. Questo effetto dovrebbe essere osservato in due casi. Se l'elemento prontamente solubile è orofilo, quindi, naturalmente, la sua dissoluzione preferenziale causerà più probabilmente la distruzione delle zone intergranulari rispetto ai cristalliti stessi, dove la concentrazione iniziale di questo elemento è molto più bassa. Un esempio di tale effetto è, apparentemente, la dissoluzione selettiva del nichel dagli acciai austenitici. È noto che gli acciai di questa classe sono generalmente soggetti a corrosione intergranulare nei metalli liquidi e questo effetto è particolarmente pronunciato quando si testano acciai in piombo e bismuto. Se prendiamo in considerazione che il nichel è un elemento orofilo nelle leghe di ferro, questo effetto trova una spiegazione.
Il secondo caso di corrosione intergranulare di leghe a dissoluzione selettiva è possibile con una distribuzione uniforme di un elemento facilmente solubile nella matrice. La condizione che fornisce la distruzione locale della lega lungo i confini del grano, in questo caso, è una maggiore velocità di diffusione dell'elemento facilmente solubile lungo i confini del grano rispetto al loro volume. La corrosione intergranulare degli acciai al cromo osservata nel bismuto liquido è apparentemente associata alla diffusione dominante del cromo, poiché, secondo i dati, non è orofila nelle leghe a base di ferro. In alcune leghe, l'elemento facilmente solubile può essere orofilo e avere un coefficiente più elevato di diffusione al contorno, che dovrebbe portare a un aumento significativo della corrosione intergranulare della lega in un metallo liquido.
Nel caso di interazione chimica del metallo liquido con il componente o i componenti della lega, si possono osservare anche intense fratture intergranulari a causa dei motivi di cui sopra.
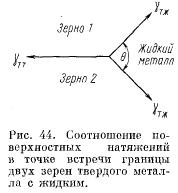
3. La distruzione di metalli solidi lungo i confini del grano in un mezzo di metallo liquido può avvenire ad un certo rapporto tra l'energia superficiale libera del confine di due granuli e l'energia libera dell'interfaccia metallo solido-liquido.
Considerare la condizione di equilibrio della tensione superficiale nel punto di incontro del confine di due granuli con un metallo liquido (Fig. 44). Indichiamo con γmt la tensione superficiale del confine di due grani e γm con la tensione superficiale del confine di ciascun grano con metallo liquido (assumiamo che γm non dipenda dall'orientamento del grano). Inoltre, sia θ l'angolo diedro tra le superfici di contatto di due granuli vicini con un mezzo di metallo liquido. Quindi la condizione di equilibrio, secondo lo schema di Fig. 44 volontà
Pertanto, a seconda del rapporto tra i valori di tensione superficiale, il rilievo superficiale del metallo solido nel punto di uscita del bordo del grano sarà diverso. Se la condizione di equilibrio è soddisfatta da un piccolo angolo acuto, in questo caso è necessario osservare la corrosione intergranulare. Inoltre, con una diminuzione dell'angolo diedro, la corrosione intergranulare si intensificherà. A θ \u003d 0, il mezzo penetrerà in profondità nel metallo solido lungo i confini del grano e si dividerà in grani separati. Nell'altro caso estremo, a θ \u003d 180 °, non ci sarà corrosione intergranulare. L'intervallo angolare di 90 ° ≤θ≤180 ° può essere considerato come il caso della formazione di piccole scanalature lungo i bordi del grano, che si trovano sulla superficie lucida di un metallo solido dopo una breve dissoluzione in un metallo liquido. Ovviamente, il limite inferiore (90 °) è condizionato, poiché anche ad angoli diedrici inferiori, la corrosione intergranulare è piccola. Apparentemente, 0 dovrebbe essere considerato un intervallo di valori particolarmente pericoloso di 0. In considerazione dell'estrema complessità della determinazione sperimentale dell'energia di superficie libera dei solidi e dell'energia dell'interfaccia di metallo solido-liquido, queste quantità sono note solo per pochissimi materiali. Non esistono inoltre metodi sufficientemente affidabili per il loro calcolo teorico. Pertanto, le considerazioni di cui sopra non possono essere applicate alle combinazioni di metalli di interesse nel nostro caso. Come esempio dell'effetto descritto, indichiamo la penetrazione intergranulare del bismuto nel rame e l'assenza di danni ai bordi del grano quando il rame è immerso nel piombo. Considerando la bagnatura quasi completa del rame da parte del bismuto (l'angolo del bordo è vicino allo zero) e la scarsa bagnatura da parte del piombo, la differenza nell'effetto di questi metalli liquidi diventa evidente. Aggiungendo zinco e stagno al bismuto, che aumentano l'energia dell'interfaccia rame - bismuto, è stata eliminata la corrosione intergranulare del rame a 600 ° C.
Va notato che nel caso si verifichino simultaneamente vari tipi di corrosione, i valori delle energie superficiali del confine di due granuli e del confine interfase possono cambiare significativamente nel tempo, il che provocherà una corrispondente variazione dell'angolo diedrico. L'energia del confine di due granuli può cambiare a causa della corrosione selettiva o della diffusione del confine di un metallo liquido. L'energia interfacciale può cambiare il suo valore a causa della formazione di una soluzione solida o di un composto intermetallico sulla superficie del metallo, nonché a causa di un cambiamento nella composizione del mezzo metallico liquido.
La corrosione intergranulare, dovuta a un certo rapporto di energie superficiali, può verificarsi sia nel processo di dissoluzione che dopo la saturazione della soluzione mediante trasferimento di energia della massa.
4. Si osserva una distruzione intensiva di metalli solidi lungo i confini del grano quando vi sono impurità nel metallo liquido. L'esempio più caratteristico è la corrosione intergranulare dei materiali nel sodio liquido, che contiene una significativa miscela di ossigeno. Quindi, gli acciai inossidabili di cromo e cromo-nichel e le leghe a base di nichel subiscono corrosione intergranulare nel sodio con una miscela di 0,5% in peso di ossigeno a 700 ° C.
La ragione di questo effetto dell'ossigeno è l'interazione chimica dell'ossigeno o degli ioni ossido di sodio con componenti di lega che si trovano in zone intergranulari. A causa dei piccoli volumi in cui avviene questa interazione e della piccola quantità di prodotti di reazione, i processi di corrosione intergranulare nei metalli liquidi con impurità non sono ancora stati studiati.
5. La corrosione intergranulare può anche essere osservata nell'interazione dei metalli alcalini con ossidi, solfuri, fosfuri e carburi, che si trovano in metalli solidi principalmente lungo i confini del grano. Tali processi saranno discussi nel prossimo capitolo. Uno dei difetti degli acciai austenitici-martensitici e austenitici-ferritici è la loro tendenza a saldare a surriscaldamento e infragilimento della zona di influenza. Ciò è causato dalla crescita del grano dovuta al surriscaldamento della fase di ferrite formata vicino alla zona di fusione. L'infragilimento è anche facilitato dalla conversione dell'austenite ricca di carbonio (l'austenite ad alta temperatura viene nuovamente arricchita con carbonio) in martensite con raffreddamento della saldatura. Va tenuto presente che nelle giunzioni saldate di acciai austenitici-ferritici e austenitici-martensitici, è possibile l'evoluzione dell'idrogeno ai confini del grano. Per evitare ciò, il giunto saldato viene temperato per 1-2 ore a una temperatura di 150 ° C.
Gli acciai e le leghe altamente legati, di norma, hanno un coefficiente di espansione lineare aumentato di 1,5 volte quando riscaldato e un coefficiente di conducibilità termica ridotto di 1,5-2 volte rispetto agli acciai a basso tenore di carbonio. La maggior parte di questi acciai sono inclini alla formazione di crepe calde o fredde durante la saldatura, il che complica il processo di garantire la qualità dei giunti saldati con le proprietà richieste. Durante la saldatura ad arco di acciai altolegati, le superfici metalliche devono essere protette da schizzi di metallo e scorie su di esso, poiché, danneggiando la superficie, possono causare corrosione o concentrazione di stress che indebolisce la struttura. Per proteggere dagli schizzi di saldatura, viene applicato un rivestimento protettivo sulla superficie metallica adiacente alla giuntura (vernice siliconica, primer VL-02, VL-023, ecc.).
Gli acciai martensitici ad alto contenuto di cromo (20X13, 14X17H2, ecc.), Il martensitico-ferritico (12X13, 14X12H2MF, ecc.) Sono acciai da indurimento inclini alla formazione di crepe fredde. In misura minore, questi includono acciai della classe ferritica (12X17, 08X17T, 08X18T1, ecc.). Per prevenire le crepe, viene utilizzato il riscaldamento preliminare o simultaneo, che è particolarmente necessario con l'aumento del contenuto di carbonio nell'acciaio e il suo spessore. Dopo la saldatura, gli acciai martensitici, martensitico-ferritici e talvolta ferritici sono sottoposti a bonifica ad una temperatura di 680-720 ° С e resistenti al calore (20X13, 12X13, ecc.) Ad una temperatura di 730-750 ° С. Il rinvenimento migliora la struttura, le proprietà meccaniche e la resistenza alla corrosione.
Va tenuto presente che la resistenza alla corrosione degli acciai senza titanio o niobio diminuisce gradualmente quando riscaldata a più di 500 ° C; pertanto, questi elementi vengono introdotti nell'acciaio e ulteriormente legati con molibdeno, vanadio e altri additivi, ad esempio acciaio martensitico 18X1ShNFB; martensitico-ferritico 18X12VMBFR; ferritico 15X25T e altri Per la saldatura di acciai martensitici, martensitico-ferritici e ferritici, vengono utilizzati elettrodi, le cui aste e rivestimenti forniscono un metallo saldato che è vicino nella composizione chimica al metallo base, ad esempio l'acciaio martensitico del grado 15X11 Navy è saldato con elettrodi E12X11NVMF del marchio KTI 10; acciaio martensitico-ferritico di grado 12X13 con elettrodi E12X13 di grado UONII-13 / SHZ, ecc. Se le strutture in acciaio di questa classe funzionano sotto carico statico e non si impongono requisiti di alta resistenza alle saldature, la saldatura può essere eseguita con elettrodi austenitici o austenitici-ferritici, ad esempio l'acciaio ferritico 15Kh25T è saldato con elettrodi OZL-20 E02Kh20N14G2M2 e il tempera dopo la saldatura può essere omesso.
Per la saldatura, viene utilizzata una modalità a basso apporto di calore per prevenire la crescita del grano e l'infragilimento della zona interessata dal calore. Il rivestimento degli elettrodi utilizzato per la saldatura di acciai ad alto contenuto di cromo non deve contenere composti organici che formano gas e la protezione del gas deve essere eseguita a causa della dissociazione dei carbonati e della conseguente CO (monossido di carbonio). Come nella saldatura di acciai legati di media lega, i requisiti per la qualità dell'assemblaggio e della pulizia dei metalli prima della saldatura rimangono gli stessi e sono persino temprati. Gli acciai ad alto contenuto di cromo delle classi considerate sono anche saldati in un mezzo di argon da un elettrodo di tungsteno. In questo modo, si consiglia di collegare parti con uno spessore fino a 5-6 mm con il riscaldamento; non è necessario un successivo trattamento termico. Si consiglia di saldare le giunture delle radici di acciaio più spesso con un elettrodo di tungsteno, che garantisce una buona formazione del rullo inverso, gli strati rimanenti della giuntura vengono eseguiti mediante saldatura manuale ad arco elettrico o in altro modo.
Gli acciai austenitici al cromo-nichel sono particolarmente sensibili all'aumento di carbonio e zolfo, così come altri elementi che formano eutettici fusibili.
CORROSIONE INTER-CRISTALLO
Insieme ai tipi considerati di corrosione durante la saldatura di acciai, si distingue anche la corrosione intercristallina (strutturale).
Corrosione intergranulare Viene chiamato il processo di distruzione fisico-chimica di un metallo lungo i confini della cristallite (grano) sotto l'influenza di un mezzo aggressivo, in cui un mezzo aggressivo penetra all'interno del metallo lungo i bordi del grano, rompendo il legame del metallo tra i granuli. L'applicazione anche di un carico insignificante a un tale metallo porta alla sua distruzione lungo i confini del grano. La corrosione intergranulare è più suscettibile agli acciai inossidabili austenitici, ma ciò può verificarsi anche in acciai ad alto contenuto di cromo, nonché saldature di classi ferritiche, semi-ferritiche e martensitiche.
Gli acciai austenitici, ad esempio l'acciaio 12Kh18N9T, diventano soggetti a corrosione intergranulare dopo un riscaldamento relativamente lungo nell'intervallo di temperature 450-850 ° C.Questa tendenza dipende da un gran numero di fattori e in particolare dalla composizione chimica dell'acciaio, dalla durata della sua permanenza a temperature critiche.
L'effetto del carbonio sulla resistenza alla corrosione dell'acciaio tipo 18-9 inizia a influenzare quando il suo contenuto è superiore allo 0,02-0,03%. Tuttavia, questo contenuto critico può essere aumentato diminuendo il tempo di mantenimento a temperature critiche o una velocità di riscaldamento e raffreddamento più elevata.
Di tutte le teorie esistenti sulla causa della corrosione intergranulare degli acciai austenitici, la teoria di precipitazione del carburo di cromo lungo i confini del grano, accompagnato dall'esaurimento del cromo nelle sezioni metalliche adiacenti ai confini del grano. L'austenite in acciaio austenitico di alta lega è una solida soluzione di cromo, nichel, manganese, carbonio e altri elementi in ferro. Il carbonio ha una solubilità limitata nell'austenite; a temperatura ambiente, il contenuto di carbonio stabile nella soluzione solida di austenite non supera lo 0,02-0,03%. Con un contenuto di carbonio più elevato nell'acciaio e il suo rapido raffreddamento (tempra), viene fissato in austenite sotto forma di una soluzione solida instabile supersaturata. In questo caso, l'acciaio è immune alla corrosione intergranulare (Fig. 1).
Tuttavia, il successivo riscaldamento del metallo nell'intervallo di temperature critiche porta al rilascio di carbonio in eccesso dalla soluzione solida al limite del grano sotto forma di carburi di cromo Cr4C.
Come risultato della separazione dei carburi ricchi di cromo, il contenuto di cromo negli strati limite dei grani austenitici scende al di sotto del 12% ed è insufficiente per mantenere la resistenza alla corrosione sotto l'influenza di mezzi aggressivi. Il diverso contenuto di cromo nel grano stesso e il suo strato limite sotto l'azione di un mezzo aggressivo (elettrolita) porta alla comparsa di micropunti galvanici, dove il grano stesso funge da catodo e strati limite impoveriti di cromo come anodo, che si correla, causando un'intensa corrosione intergranulare in queste sezioni di grano. .
Fig. 1. Diagramma della distribuzione del cromo sul grano dell'acciaio austenitico, soggetto a corrosione intergranulare: a- in uno stato stabilizzato (nessuna corrosione); b- dopo il riscaldamento in un intervallo di temperatura critica e se esposto a un ambiente aggressivo (presenza di corrosione): 1 - forma condizionata di grano austenitico; 2 - carburi di cromo ai bordi del grano; 3 - sezioni di confine unite da chrome; 4 - linee di distribuzione del cromo sul grano austenitico.
In fig. La Figura 2 mostra la dipendenza della corrosione intergranulare dell'acciaio dalla temperatura e dal tempo. La curva illustra la relazione tra la temperatura di riscaldamento dei giunti saldati in acciaio di tipo 18-9 e la loro tendenza alla corrosione intergranulare.
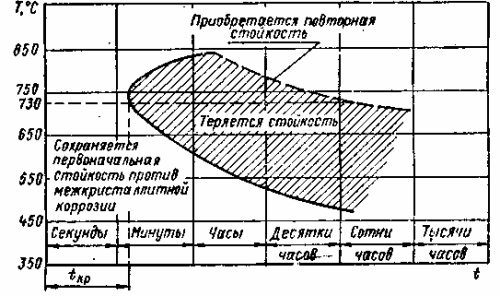
Fig. 2. La dipendenza della tendenza dell'acciaio austenitico alla corrosione intergranulare dalla temperatura e la durata della permanenza di questo acciaio a una data temperatura (tcr è il tempo di stabilità minima dell'austenite)
Come conseguenza di questa dipendenza, quando la temperatura del riscaldamento dell'acciaio aumenta a 730 ° C, il tempo critico per l'acciaio a diventare incline alla corrosione intergranulare diminuisce da poche ore a frazioni di minuto. Al raggiungimento di 800-850 ° C, la suscettibilità alla corrosione intergranulare non si verifica affatto. Ciò è spiegato dalle diverse velocità di due processi reciprocamente opposti: precipitazione del carburo di cromo e diffusione del cromo dalla parte centrale del grano di austenite alla sua periferia. All'aumentare della temperatura da 450 a 730 ° C, la velocità di deposizione di carbonio dalla soluzione supersaturata e la formazione di carburi di cromo procedono più velocemente della velocità di diffusione del cromo. Di conseguenza, l'acciaio diventa più suscettibile alla corrosione intergranulare in un tempo più breve. Un ulteriore aumento della temperatura da 730 a 850 ° C porta ad una sempre maggiore accelerazione della diffusione del cromo: anche dalle regioni centrali dei grani di austenite, l'esaurimento locale del cromo delle regioni al contorno dei grani non procede più rapidamente delle basse temperature. Inoltre, a queste temperature, già influisce il processo di coagulazione e dissoluzione dei carburi nell'austenite. Per lo stesso motivo, un'esposizione più lunga dell'acciaio a una determinata temperatura porta al ripristino della resistenza temporaneamente persa alla corrosione intergranulare (linea tratteggiata) e ad una temperatura di 850 ° C e superiore, non si verifica affatto la suscettibilità alla corrosione intergranulare.
Un aumento del contenuto di carbonio negli acciai austenitici intensificherà la formazione di carburi di cromo e aumenterà la tendenza alla corrosione intergranulare. In misura minore, la tendenza alla corrosione intergranulare è influenzata da elementi austenitizzanti: nichel e azoto; con un aumento del contenuto di questi elementi negli acciai austenitici, per ridurre la tendenza dell'acciaio alla corrosione, il contenuto di carbonio in esso contenuto dovrebbe essere ridotto.
Un aumento della concentrazione di cromo nell'acciaio austenitico riduce il grado di deplezione del cromo nelle regioni di confine e aumenta la resistenza dell'acciaio alla corrosione. L'introduzione del molibdeno nell'acciaio aumenta la resistenza alla corrosione dell'acciaio, poiché inibisce il processo di precipitazione del carburo di cromo e anche perché è un ferritizzatore attivo. "E l'acciaio con una struttura austenitico-ferritica (3-5% di ferrite) è meno soggetto alla corrosione intergranulare rispetto puramente austenitico, poiché si osservano la raffinatezza del grano e un aumento del numero di grani nel metallo, il che porta ad un aumento della lunghezza totale della superficie del grano e la quantità di carbonio rilasciata sotto forma di carburi diventa molto più piccola.
La ferrite contiene più cromo che austenite, quindi, nonostante l'esaurimento del cromo nella precipitazione dei carburi, nella ferrite rimane abbastanza cromo per resistere alla corrosione intergranulare. I grani ferritici si trovano all'interno dei grani austenitici e una piccola parte di essi si trova ai bordi ", il che impedisce l'influenza di un ambiente aggressivo sui confini dei grani di austenite.
Il titanio e il niobio entrano negli acciai austenitici per sopprimere gli effetti dannosi del carbonio. Questi elementi, che hanno una maggiore affinità per il carbonio rispetto al cromo, formano carburi (TiC, NbC), prevenendo la formazione e la precipitazione dei carburi di cromo Cr4C. Il contenuto richiesto di titanio e niobio nell'acciaio è:
Ti \u003d (5-4-6) C;
Nb \u003d (8-10) C,
dove C è il contenuto di carbonio dell'acciaio austenitico.
Titanio e niobio sono ferritizzatori attivi e ciò contribuirà anche a ridurre la tendenza alla corrosione intergranulare.
I diagrammi strutturali possono essere utilizzati per stabilire la microstruttura del metallo di saldatura di acciaio al cromo-cromo.
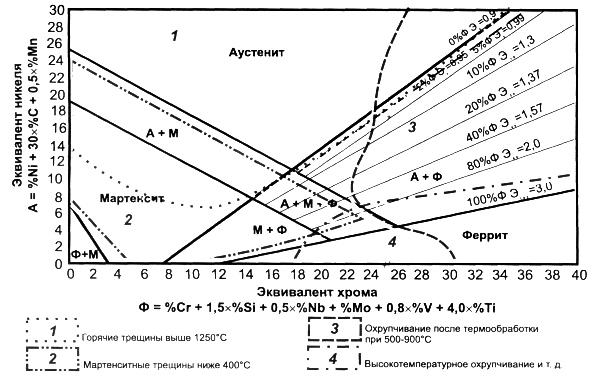
Come risultato di studi a lungo termine, è stato possibile stabilire l'efficacia dell'azione sulla struttura della saldatura di uno o un altro elemento rispetto all'azione delle principali impurità leganti degli acciai austenitici: il principale elemento di riduzione della ferrite del cromo e il principale elemento di formazione di austenite del nichel. Sulla base dei dati ottenuti e dell'azione degli elementi principali “come unità, abbiamo costruito il diagramma strutturale di Scheffler per le saldature (Fig. 3), in cui l'ordinata è l'equivalente del nichel e l'ascissa è l'equivalente del cromo.
Abbraccio e corrosione intergranulare
La corrosione intergranulare è caratterizzata dalla distruzione selettiva lungo i confini dei cristalliti metallici (grani) (Fig. 5.91). Questo tipo di corrosione è soggetto ad acciai inossidabili, in particolare austenitici, e ad alcune leghe non ferrose. La corrosione intergranulare è caratteristica degli acciai al cromo-nichel nelle condizioni di raffreddamento delle piante dopo la rigenerazione del catalizzatore, alcuni elementi dell'attrezzatura durante la purificazione del gas monoetanolamina.
Per natura e meccanismo di danneggiamento del materiale, la corrosione dei coltelli dovrebbe anche essere classificata come corrosione intergranulare - distruzione della zona interessata dal calore che confina con la giuntura di saldatura degli elementi strutturali da nichel-cromo austenitico e altri acciai ad alta lega. In apparenza, i contorni della frattura intergranulare assomigliano a un'incisione con un coltello affilato. La corrosione dei coltelli si diffonde ad alta velocità in profondità nel metallo ed è sostanzialmente dipendente dalla tecnologia di saldatura.
Fig. 5.91. Corrosione intergranulare di acciaio 12X18H10T dall'interno tubo senza saldatura 0108x6 mm ad una distanza di (a) e vicino (b) alla zona di frattura del tubo di idrogenazione dell'installazione di Pyrocondensate, x 200
La tendenza alla corrosione intergranulare è determinata secondo GOST 6032-72.
Le apparecchiature chimiche e petrolchimiche in acciaio inossidabile sono spesso soggette a corrosione intergranulare. Scorre in modo particolarmente intenso negli elementi delle apparecchiature soggette a deformazione plastica: fondi ellittici e sferici, curve, gomiti, giunti saldati, ecc.
Abbastanza spesso, la corrosione intergranulare negli acciai inossidabili di tipo X18H10 si verifica nelle bobine dei forni a tubi utilizzati per riscaldare i prodotti di cracking catalitico dell'olio. Le bobine vengono lavate con fumi con una temperatura fino a 1200 ° C nella parte di radiazione e fino a 700 ° C nella convezione. I gas idrocarburi con un contenuto dell'1,2-4,5% S sono usati come combustibile nella fornace. Nei fumi, insieme a CO e N0, S03 è contenuto fino a 1426 mg / m3.
Un'analisi delle cause della corrosione intergranulare mostra che il suo aspetto è associato all'influenza di un mezzo di acido solforico che si verifica all'avvio e all'arresto del forno. Le frequenti interruzioni delle materie prime, che causano un aumento della frequenza di arresti e avviamenti dei forni, contribuiscono allo sviluppo della corrosione intergranulare. L'anidride solforica, combinata con il vapore acqueo, forma acido solforico depositato sui tubi sotto forma di solfati igroscopici.
Secondo i dati, nel giunto saldato della bobina (con un diametro di 219 mm e uno spessore della parete di 10 mm) della parte di radiazione del forno, dopo 2520 ore di funzionamento, è stato rilevato un passaggio di mezzo nello spazio del forno. Nel sedimento sulla bobina, il contenuto di S042- ha raggiunto il 22,12%. Dopo aver rimosso il rinforzo della saldatura di montaggio, una rete di crepe è visibile su tutta la superficie del metallo di saldatura. Inoltre, l'apertura della fessura non ha superato 0,3 mm e la lunghezza era 1,5-3 mm. La profondità della corrosione intergranulare continua sulla superficie interna del metallo di base della bobina del forno convenzionale ha raggiunto 1,1-1,3 mm.
La corrosione intergranulare è pericolosa perché in presenza di sollecitazioni di saldatura residue e cicli di avvio / arresto termico, si sviluppa in incrinature da corrosione da sollecitazione.
La causa della corrosione intergranulare degli acciai inossidabili austenitici è associata alla formazione di precipitati granulometrici di carburi arricchiti in cromo. Alle alte temperature, gli acciai inossidabili di composizione classica (18% Cr, 9% Ni) sono in grado di dissolvere un gran numero di elementi interstiziali (C e N). Tuttavia, al di sotto di 900 ° C, la solubilità di questi elementi diminuisce drasticamente. Nel trattamento tradizionale dell'acciaio per una soluzione solida dopo l'estinzione 
Fig. 5.92. La precipitazione dei carburi di cromo Cr23C6 ai bordi della grana e della sottotraccia in acciaio 08Kh18N10T dopo riscaldamento a 650 ° C, 100 h. TEM x 16000
contenuta in una soluzione solida supersaturata una quantità significativa di carbonio e azoto. Come risultato della successiva azione termica a 450–700 ° С, si formano precipitati M23C6 arricchiti di cromo al limite del grano (Fig. 5.92). In queste condizioni, le sezioni di grano adiacenti ai precipitati di confine del grano risultano impoverite in cromo e sono soggette a dissoluzione in alcune soluzioni acquose.
Nei tubi dei surriscaldatori realizzati in acciaio inossidabile austenitico 12X18H10T con una temperatura del vapore di 570 ° C, la ridistribuzione del cromo si verifica a causa del surriscaldamento esterno alla superficie del collo. In queste aree, i carburi ad alto contenuto di cromo si formano con l'esaurimento simultaneo del volume del grano del bordo inferiore al 12% da parte del cromo, causando l'ossidazione dell'acciaio. Di conseguenza, la resistenza della parete del tubo nella sezione macro diminuisce drasticamente e inizia la frattura intergranulare, a partire dalla superficie di riscaldamento.
Le temperature più pericolose sono 500-550 ° C, a cui l'acciaio inossidabile di tipo X18H10T, indipendentemente dalla composizione chimica e dalla temperatura di indurimento, acquisisce una tendenza alla corrosione intergranulare (sensibilizza). Nell'acciaio sensibilizzato, la corrosione intercristallina è particolarmente evidente durante gli arresti durante l'idrotrattamento.
Viene proposto un semplice schema per la formazione di un foro di corrosione (depressione) sull'acciaio. Il tasso di ossidazione su una superficie metallica esposta può essere superiore di diversi ordini di grandezza rispetto a una superficie rivestita con un film passivante protettivo. a
in determinate condizioni, il contenuto di ossigeno nella soluzione all'interno del pozzo viene notevolmente ridotto dalla reazione catodica. Per questo motivo, un aumento della concentrazione di ioni metallici in soluzione non è bilanciato da un aumento della concentrazione di OH- nella reazione
2Н20 + 02 + 4е - "40Н",
e la soluzione mantiene una carica positiva in eccesso.
Gli ioni cloruro hanno un effetto particolarmente intenso sulla tendenza ad effetti corrosivi selettivi con la formazione di vaiolatura. I cloruri metallici idrolizzano l'acqua, portando a una diminuzione del pH della soluzione:
M "C1- + H2O - M OH- + H + + C1".
Un pH inferiore e una maggiore attività dello ione cloruro nella soluzione all'interno della cavità (fossa) causano un ulteriore aumento del tasso di ossidazione dei metalli. Questa crescita provoca un ulteriore aumento dell'afflusso di ioni cloruro nella fossa e il processo diventa autocatalitico.
Gli esami periodici condotti con test ad ultrasuoni hanno mostrato che in quattro serbatoi saldati con un volume di 40 m3 in acciaio X18H9 per lo stoccaggio di composti di acido nitrico, il grado più elevato di corrosione intergranulare è rivelato ai giunti delle saldature longitudinali e circonferenziali. Questa corrosione si sviluppa solo nella zona di contatto del metallo con la fase vapore-gas del prodotto in lavorazione. La corrosione peptica e del coltello esiste nel metallo a contatto con le fasi del vapore e del liquido del prodotto in lavorazione. In questo caso, si osserva il più forte aumento dei difetti operativi per i serbatoi in climi caldi (Fig. 5.93, a). La profondità dei difetti aumenta monotonamente con una velocità quasi costante di (8-9) 10 5 m / anno per i serbatoi in un clima temperato e (24-35) 10 "5 m / anno per i serbatoi che operano in una zona a clima caldo (Fig. 5.93, b) .
Il fenomeno della rottura per corrosione sotto sforzo degli acciai inossidabili in un mezzo contenente cloruro è caratterizzato dallo sviluppo di fratture da parte del meccanismo della fragile scissione transcristallina. Questo modello di frattura è stato notato nello studio dell'acciaio 12Kh18N10T dopo aver testato la rottura della corrosione in una soluzione acquosa al 30% di MgCl2. Con una diminuzione del livello delle tensioni da 0,7 a 0,2 circa 0,2 nella frattura, la frazione di sfaccettature di una fragile scissione transcristallina con una rete di fessure secondarie aumenta in modo significativo. Le sfaccettature scheggiate hanno uno schema rubicondo caratteristico dei metalli con un reticolo ccn. 
Fig. 5.93. Variazione dei tassi medi di corrosione intergranulare (a) e profondità dei difetti (b) nei serbatoi operati in climi caldi (o) e temperati ()
Una caratteristica distintiva del motivo ruscello in un metallo con un reticolo fcc è un cambiamento nella direzione dei gradini di scollatura non solo al limite del grano, ma anche nei volumi interni dei grani. Sulla superficie delle sfaccettature, compaiono gli zigzag - sporgenze di un motivo a strisce. Questo cambiamento nella direzione del modello di ruscello è dovuto all'intersezione del piano di frattura del piccolo angolo e dei confini gemelli.
